
Periyodik tablo, kimyasal elementlerin sınıflandırılması için geliştirilmiş tablodur. Dilimizde periyodik tablo, periyodik cetvel, periyodik çizelge, elementler tablosu gibi birçok şekilde isimlendirilmiştir. Bu tablo bilinen bütün elementlerin artan atom numaralarına göre sıralanışıdır. Periyodik cetvelden önce de bu yönde çalışmalar yapılmış olmakla birlikte, mucidi genelde Rus kimyager Dmitri Mendeleyev kabul edilir. 1869'da Mendeleyev atomları artan atom ağırlığına göre sıraladığında belli özelliklerin tekrarlandığını fark etti. Özellikleri tekrarlanan elementleri alt alta yerleştirdi ve buna grup adını verdi.

Helyum, sembolü He ve atom numarası 2 olan kimyasal element. Periyodik cetvelin birinci periyot 8A grubunda yer alan bir gazdır. Kokusuz, renksiz bir gazdır ve yanmaz.

Elektron dizilimi, atom fiziği ve kuantum kimyasında, bir atom ya da molekülün elektronlarının atomik ya da moleküler orbitallerdeki dağılımıdır. Örneğin Neon atomunun elektron dizilimi 1s2 2s2 2p6 olarak gösterilir.
Alkali metaller periyodik tablonun birinci grubunda yer alan metallerdir. Fransiyum dışında hepsi, yumuşak yapıda ve parlak görünümdedir.
Alkalinler ya da Toprak Alkali Metaller:
Periyodik tablonun baştan ikinci (2A) grubunda yer alan elementlerdir.

Geçiş metalleri veya bazı kimyacıların tabiriyle ağır metaller; sertlikleri, yüksek yoğunlukları, iyi ısı iletkenlikleri ve yüksek erime-kaynama sıcaklıklarıyla tanınırlar. Özellikle sertlikleri nedeniyle saf halde ya da alaşım halinde yapı malzemesi olarak kullanılırlar.
Halojenler, periyodik tablonun 7A grubunda bulunan, tepkimeye eğilimli ametallerdir. Bu gruptaki elementlerin hepsinin elektronegatifliği yüksektir. Elektron alma eğilimi en yüksek olan elementlerdir. Doğada elementel olarak değil, mineraller halinde bulunurlar. Element halinde 2 atomlu moleküllerden oluşurlar. Oda koşullarında flor ve klor gaz, brom sıvı, iyotsa katı haldedir. Erime ve kaynama noktaları grupta aşağıdan yukarıya doğru azalır. Zehirli ve tehlikeli elementler olarak bilinirler. Halojenler metallerle reaksiyona girerek iyonik tuzları oluştururlar.
Periyodik tabloda dikey sütunlara grup denir. Aynı grupta olan elementlerin kimyasal özellikleri benzerdir. Yukarı doğru dikeyce çıktıkça özellik yoğunlaşır ve belirginleşir. Bir A grubuna ait elementin son katmanında kaç elektron varsa grup sıralaması da odur. Örneğin, berilyum (Be) atomunun son katmanında 2 elektron vardır ve bu atom 2A grubunun elementi olur.
Lantanitler, geçiş metallerinin bir alt serisini oluştururlar. 57 ile 71 atom numaraları arasındaki elementleri kapsar. 17 nadir toprak elementinin 15 tanesi lantanit grubundandır. Bu nedenle lantanitler nadir toprak elementleri olarak da isimlendirilmiştir.
Ametal, metal özelliği göstermeyen elementlerdir. Isıyı ve elektrik akımını iletmek gibi metallere özgü özellikleri göstermezler. Ayrıca kendi aralarındaki ortak özellikleri yok denecek kadar azdır. Genellikle karbon, azot, fosfor, oksijen, kükürt, selenyum, flor, klor, brom, iyot ve soy gaz elementlerine ametal denir.
Skandiyum grubu veya 3. grup elementleri, periyodik tablonun 3. grubunda yer alan elementlerdir. Bu elementlerin en dış elektron katmanlarında üçer elektron vardır.

Baryum (Yunanca'da βαρυς = ağır), sembolü Ba olan kimyasal bir elementtir. Ağır manasına gelen "barys" kelimesinden türemiştir. İngilizcede Barite ağırlık yoğunluk manasında kullanılmaktadır. Baryum elementinin atom numarası 56 olup Periyodik tablonun 6. sırasında ve 2. grubunda bulunur. 2. grupta bulunması özelliğinden dolayı Baryum bir toprak alkali metalidir. Baryum ilk defa 1774 yılında İsveçli kimyacı Carl Wilhelm Sheele tarafından tanımlanmıştır. Baryum element halinde beyaz-gri metalik rengindedir fakat yüksek reaktivitelikten dolayı element halinde bulunmaz. Baryum'un hemen hemen bütün bileşikleri ise zehirlidir. Metalik Ba yakıldığında elma yeşili bir renk verir. Metalik halde saklanması çok zordur. Aktif bir element olduğu için su, hava ve asitlerle kolayca reaksiyon verir. Toprak alkali grup içerisinde doğada en yaygın bulunan element Kalsiyum(Ca)dur. Bu sınıftaki metallerin özellikleri birbirine benzemesine karşın bilhassa Kalsiyum, Stronsiyum, Baryum diğerlerinden ayrılır. Bu üç element adi derecede suyu ayrıştırarak Hidrojen açığa çıkarır ve Hidroksit(OH) oluştururlar. Bu Hidroksitler de ısıtıldığında su kaybederek Oksit haline dönmektedirler. Karbonatları ısı karşısında kolay ayrışmasına karşın Baryum Karbonat (BaCO3) en zor ayrışanıdır. Sülfatları suda hemen hemen hiç erimez.
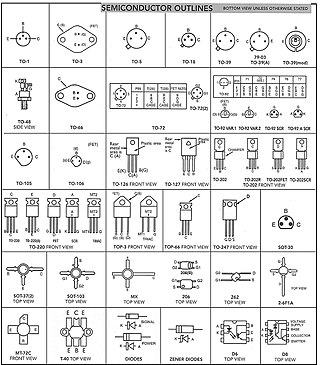
Yarı iletken üzerine yapılan mekanik işin etkisiyle iletken özelliği kazanabilen, normal şartlar altında yalıtkan olan maddelerdir.
Zayıf metal veya post geçiş metali, periyodik tablonun p blokunda yer alan metalik elementlerdir. Metaloidlerle geçiş metalleri arasında bulunurlar. Geçiş metallerinden daha fazla, alkali metaller ve toprak alkali metallerinden daha az elektro-pozitiftirler. Ergime ve kaynama sıcaklıkları genellikle geçiş metallerinkilerden daha düşük olup daha yumuşaktırlar.

Terbiyum, atom numarası 65, atom ağırlığı 159 olan, çok ender bulunan bir element.

İterbiyum (Yb), sembolü ile bilinen, elektron dizilişlerinde f orbitalinde elektron barındıran kimyasal bir element. Bu element grup 3 elementlerine ve 6. periyot elementlerine ait olan bir lantanittir.

Kimyasal bağ, atomların veya iyonların molekülleri, kristalleri ve diğer yapıları oluşturmak üzere birleşmesidir. Bağ, iyonik bağlar'da olduğu gibi zıt yüklü iyonlar arasındaki elektrostatik kuvvetten veya kovalent bağ'larda olduğu gibi elektronların paylaşılmasından veya bu etkilerin bazı kombinasyonlarından kaynaklanabilir. Açıklanan kimyasal bağların farklı mukavemetleri vardır: kovalent, iyonik ve metalik bağlar gibi "güçlü bağlar" veya "birincil bağlar" ve dipol-dipol etkileşimleri, London dağılım kuvveti ve hidrojen bağı gibi "zayıf bağlar" veya "ikincil bağlar" vardır.

Azot Grubu, periyodik tablodaki gruplardan biridir. Bu grubun genel özellikleri aşağıdaki şekilde tanımlanır;
- Azot grubu şeklinde adlandırılırlar
- Azot (N), Fosfor (P), Arsenik (As), Antimon (Sb) ve Bizmut (Bi) elementlerinden oluşur
- En son elektron kabuklarında 5 elektron bulunur ve son yörüngeleri np3 ile sonlanır
- Bileşiklerinde genellikle -3 değerliklerini alırlar
- Azot ve fosfor ametal, arsenik ve antimon yarı metal, bizmut metaldir.
- Sulu çözeltileri asidiktir.

Nadir toprak elementleri ya da kısaca NTE, lantanitlerle birlikte itriyum ve skandiyum elementlerinin oluşturduğu bir grubu kapsamaktadır. Lantanitler atom numaraları 57'den 71'e kadar olan ve kimyasal olarak benzer elementlerin oluşturduğu bir gruptur. Atom numarası 39 olan itriyum ve atom numarası 21 olan skandiyum da lantanitlerle benzer kimyasal özellikleri nadir toprak elementlerinin içine dâhil edilmiştir. Yerkabuğunda diğer minerallere oranla daha fazla bulunmadıkları sanıldığından dolayı bu ismi almışlardır.
Madenî para metali, periyodik tablonun 1B grubunda yer alan kimyasal elementlerdir. Bu elementlerin en dış elektron katmanlarında dörder elektron vardır.









