Karbon
 Karbonun iki allotropu olan grafit (sol) ve elmas (sağ) | ||||||||||||||||||||||||||
| Allotroplar | grafit, elmas ve diğerleri | |||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Görünüş | grafit: siyah, metalik görünümlü elmas: berrak | |||||||||||||||||||||||||
| Standart atom ağırlığı Ar, std(C) | [12,0096, 12,0116] geleneksel: 12,011 | |||||||||||||||||||||||||
| Periyodik tablodaki yeri | ||||||||||||||||||||||||||
| ||||||||||||||||||||||||||
| Atom numarası (Z) | 6 | |||||||||||||||||||||||||
| Grup | 14. grup (karbon grubu) | |||||||||||||||||||||||||
| Periyot | 2. periyot | |||||||||||||||||||||||||
| Blok | p bloku | |||||||||||||||||||||||||
| Elektron dizilimi | [He] 2s2 2p2 | |||||||||||||||||||||||||
| Kabuk başına elektron | 2, 4 | |||||||||||||||||||||||||
| Fiziksel özellikler | ||||||||||||||||||||||||||
| Faz (SSB'de) | katı | |||||||||||||||||||||||||
| Süblimleşme noktası | 3915 K (3642 °C, 6588 °F) | |||||||||||||||||||||||||
| Yoğunluk (OS) | amorf: 1,8–2,1 g/cm3[1] 2,267 g/cm3 3,515 g/cm3 | |||||||||||||||||||||||||
| Üçlü nokta | 4600 K, 10.800 kPa[2][3] | |||||||||||||||||||||||||
| Erime entalpisi | grafit: 117 kJ/mol | |||||||||||||||||||||||||
| Molar ısı kapasitesi | grafit: 8,517 J/(mol·K) elmas: 6,155 J/(mol·K) | |||||||||||||||||||||||||
| Atom özellikleri | ||||||||||||||||||||||||||
| Yükseltgenme durumları | -4, -3, -2, -1, 0, +1,[4] +2, +3,[5] +4[6] hafif asidik | |||||||||||||||||||||||||
| Elektronegatiflik | Pauling ölçeği: 2,55 | |||||||||||||||||||||||||
| İyonlaşma enerjileri |
| |||||||||||||||||||||||||
| Kovalent yarıçapı | sp3: 77 pm sp2: 73 pm sp: 69 pm | |||||||||||||||||||||||||
| Van der Waals yarıçapı | 170 pm | |||||||||||||||||||||||||
| Diğer özellikleri | ||||||||||||||||||||||||||
| Kristal yapı | Grafit: Basit hekzagonal (siyah) | |||||||||||||||||||||||||
| Kristal yapı | Elmas: Yüzey merkezli elmas kübik (berrak) | |||||||||||||||||||||||||
| Genleşme | elmas: 0,8 µm/(m·K) (25 °C'de)[7] | |||||||||||||||||||||||||
| Isı iletkenliği | grafit: 119–165 W/(m·K) elmas: 900–2300 W/(m·K) | |||||||||||||||||||||||||
| Elektrik direnci | grafit: 7,837 Ω·m[8] | |||||||||||||||||||||||||
| Manyetik düzen | diyamanyetik[9] | |||||||||||||||||||||||||
| Manyetik alınganlık | -5,9×10-6 cm3/mol[10] | |||||||||||||||||||||||||
| Young modülü | elmas: 1050 GPa[7] | |||||||||||||||||||||||||
| Kayma modülü | elmas: 478 GPa[7] | |||||||||||||||||||||||||
| Hacim modülü | elmas: 442 GPa[7] | |||||||||||||||||||||||||
| Poisson oranı | elmas: 0,1[7] | |||||||||||||||||||||||||
| Mohs sertliği | grafit: 1–2 elmas: 10 | |||||||||||||||||||||||||
| CAS Numarası |
| |||||||||||||||||||||||||
| Tarihi | ||||||||||||||||||||||||||
| Keşif | Mısırlılar ve Sümerler (MÖ 3750)[12] | |||||||||||||||||||||||||
| Bir element olarak tanıyan | Antoine Lavoisier[11] (1789) | |||||||||||||||||||||||||
| Ana izotopları | ||||||||||||||||||||||||||
| ||||||||||||||||||||||||||
Karbon, doğada yaygın bulunan ametal kimyasal elementtir. Evrende bolluk bakımından altıncı sırada yer alan karbon, kızgın yıldızlarda hidrojenin termonükleer yanmasında temel rol oynar. Dünyada hem doğal halde, hem de başka elementlerle bileşik halinde bulunan karbon, ağırlık olarak Dünya'nın yerkabuğunun yaklaşık %0,2'sini oluşturur. En arı (katışıksız) biçimleri elmas ve grafittir; daha düşük arılık derecelerinde maden kömürünün, kok kömürünün ve odun kömürünün bileşeni olarak bulunur. Atmosferin yaklaşık % 0,05'ini oluşturan ve bütün doğal sularda erimiş olarak bulunan karbon dioksit, kireç taşı ve mermer gibi karbonat mineralleri, kömürün, petrolün ve doğalgazın başlıca yapıtaşları olan hidrokarbonlar, en bol bulunan bileşikleridir.
Karbon, bilinen elementlerin en çok yönlü olanıdır. Bileşiklerin %94'ü (4 milyondan çoğu) karbon içerir. Yaşamın dayandığı temel işlevleri yerine getirmek için yeterli çeşitlilikte ve karmaşıklıkta düzenlemeler oluşturarak başka elementlerle birleşme yeteneği, yalnızca karbonda vardır. Belirli karbon bileşikleri, canlılardaki maddenin yaklaşık %18'ini oluşturur (geri kalanı çoğunlukla sudur). Bu bileşikler, canlı hücrelerin planı olarak, hücre yapımında kullanılan yapıtaşları olarak işlev görürler.
Yakıt işlevi gören başka karbon bileşikleri de, yeşil bitkilerde ışıl birleşimle sürekli olarak yenilenir. Organizma öldüğü zaman, çevreyle karbon alışverişi durur ve geriye kalan radyoaktif karbon-14 izotopu miktarı, biyolojik kökenli maddelerin yaşını belirlemekte kullanılabilir.
Kalkınmış ülkelerin ekonomilerinin büyük bir bölümü, karbon içeren yakıtların, plastiklerin, kimyasal maddelerin, dokumaların ve ilaçların işlenmesine ve üretimine dayanır. Karbon temelli sentetik bileşiklerin üretilmesi ve kullanılması, birçok ülkede yaşama düzeyini derinlemesine etkilemiştir.
Özellikleri
Simgesi C, atom numarası 6, atom ağırlığı 12,011 olan karbon, periyodik tablonun 14. grubunda silisyum, germanyum, kalay ve kurşun elementleriyle birlikte yer alır. Bu elementlerin en hafifi ve en az metalik olanıdır. Periyodik çizelgedeki başka birçok grubun tersine, 14. grup elementleri, kimyasal bakımdan birbirinden çok farklıdır; grubu temsil edici davranışı en fazla gösteren de karbondur.
Karbonun en bol bulunan izotopu, doğal karbonun % 98,89'unu oluşturan karbon-12'dir. Tam olarak 12 dalton (atom kütlesi birimi) değerinde olan bu izotop, atom ağırlığı konusunda uluslararası standart olarak kullanılır. Doğal karbonun % 1,11'ini oluşturan karbon-13, ikinci kararlı izotoptur. Karbonun beş radyoaktif izotopu bilinmektedir; bunlardan karbon-14 (yarılanma süresi 5 730 yıl) en kararlı ve en yararlı olanıdır. Bağlar. Serbest karbon atomunun 1s kabuğunda iki elektron, 2s ve 2p kabuklarındaysa bağ oluşturmaya hazır dört değerlik elektronu bulunur. Metallerden ve ametallerin birçoğundan farklı olarak, karbonda bağ oluşumu genellikle iyonik değil, kovalent (ortaklaşa) niteliktedir. Bunun nedenlerinden biri, karbonun atom sayısının küçük olması, bu nedenle de, atom çekirdeğine yakın olan değerlik elektronlarını çok sıkı tutmasıdır. Ayrıca, bir karbon atomunun kararlı bir iyon haline gelmesi için dört elektron alması ya da yitirmesi gerekir: Bu da oldukça büyük enerji isteyen bir olaydır.
Ortaklaşa bağlanmada, her karbon atomu, değerlik elektronlarını karşılıklı olarak başka atomlarla paylaşır. Karbon bileşiklerinin çoğunda, bitişik bir atom, 1-3 arasında elektron verir; buna karşılık karbon da eşit sayıda elektron katkısı yapar ve tek, çift ya da üçlü bağ oluşur.
Kömürler
Odun kömürü
Ana başlık: Odun kömürü
Odun kömürü hafif, gözenekli siyah ya da koyu gri renkli bir maddedir; odunun havasız ortamda yakılmasıyla elde edilir. (Karbonun bir başka allotropu olan odun kömürüne ilişkin ayrıntılı bilgi kömür maddesinde verilmiştir.)
Kemik kömürü
Odun kömürünün katışıklı bir türü de, yalnızca yüzde 10 oranında karbon içeren kemik kömürüdür. Kemik kömürü, hayvan kemiklerinin iyice kırılıp havasız ortamda yakılmasıyla elde edilir. Kemik kömürü herhangi bir sıvı ile ısıtıldığında, sıvını rengini yok eder, bu nedenle sanayide renk giderici olarak kullanılır. Örneğin, şeker bu yolla arıtılır. Çay kemik kömürü ile kaynatıldığında tamamen renksiz hale gelir.
Karbon karası
Karbon karası ise gazyağı, terebentin, benzen ya da mum gibi maddelerin havasız az ortamlarda yandıklarında çıkardıkları istir. Karbon karası katışıksız, yumuşak, siyah renkli bir tozdur; yağla karıştırılarak matbaa mürekkebi, boya ve ayakkabı cilasında kullanılır. Ayrıca otomobil ve bisiklet lastiklerinin yapımında, aşınmaya karşı daha dayanıklı kılmak amacıyla karbon karasından yararlanılır.
Kok kömürü
Ana başlık: Kok kömürü
Kok kömürü, kömürün havasız ortamda, yüksek sıcaklıklarda yakılmasıyla elde edilir. Kok kömüründeki karbon oranı yaklaşık %90'dır. Karbon elementi gerek kömür, antrasit ve kok kömürü olarak, gerek bileşik halde bulunduğu selüloz ve petrol olarak çok önemli bir yakıttır. Karbon ve oksijen bileşikleri birbirleriyle çok kolay birleşir. Çinko, demir, kalay ya da kurşun oksitler gibi metal oksitleri karbon ile birlikte ısıtıldığında, karbon metal oksitteki oksijenle birleşir ve geriye katışıksız metal kalır. Bu indirgenme tepkimesinden sanayide yararlanılır.
Karbon allotropları
Ana madde: Karbon allotropları


Aynı maddenin değişik kristal biçimlerine allotrop denir; allotrop sözcüğü değişik biçim anlamında Yunanca iki sözcükten gelir. Elmas ve grafit, karbonun allotroplarıdır. Elmasta her karbon atomu, dört başka karbon atomuna bağlanarak üç boyutlu katı bir yapı oluşturur; grafitte ise karbon atomları, üst üste yığılmış geniş, yassı levhalar oluşturacak biçimde, iki boyutlu düzlemde birbirlerine bağlanmıştır. Bu levhalar birbirlerinin üzerinden kolayca kayar; grafitin iyi bir yağlayıcı olma özelliği de bundan kaynaklanır. Grafitin kâğıt üzerinde iz bırakmasının nedeni de, bu ince atom levhalarının grafitten ayrılarak kağıdın üzerinde birikmesidir. Elmas ve grafit dışında karbonun ayrıca altıgen elmas gibi doğal, camsı karbon, fullerenler kümelenmiş elmas nanoçubukları, karbon nanoköpüğü, doğrusal asetilenik karbon (LAC) gibi yapay allotropları da vardır. Karbonun belirgin, kendilerine özgü bir yapısı ya da biçimi olmayan allotropuna amorf karbon denir. Kömür bu biçimdedir.
Elmas
Ana başlık: Elmas

Arı elmas, bilinen en sert doğal maddedir. Renksiz ve saydam olmasına karşın, başka minerallerle arılığı bozulduğu zaman, pastel renklerden mat siyaha kadar uzanan çeşitli renklerde bulunabilir. Elmas, kimyasal bakımdan eylemsizdir; ama yüksek sıcaklıklarda havada yanması sağlanabilir. Bilinen ısıyı ileten en iyi malzemedir ve elektrik yalıtkanıdır. 1955'e kadar, yanardağ kökenli doğal yataklar tek elmas kaynağıyken, o tarihten bu yana aletlerde ve pikap iğnelerinde kullanılan elmaslar, grafitin yüksek basınçlara ve sıcaklıklara uğratılmasıyla yapay olarak üretilmektedir (mücevher niteliğinde elmaslar bu yolla elde edilemez).
Elmasın özellikleri, bütünüyle birbirine kenetlenmiş dörtyüzlü karbon atomlarının oluşturduğu kristal yapısından kaynaklanır; bu atomların her biri, en yakın dört komşusuna ortaklaşa bağlanmıştır. Karbon-karbon bağının olağanüstü dayanıklılığı ve ortaklaşa bağlarla kenetlenmiş yapısı, elmasın sert ve eylemsiz olmasını sağlayan nedenlerdir.
Grafit
Ana başlık: Grafit

Grafit, karbonun yaygın bir allotropudur. Yumuşak, yağlı, kâğıtta iz bırakan, siyah renkli bir katı maddedir. Grafitte her bir karbon atomu aynı düzlemde bulunan diğer üç atoma altıgen halkalar oluşturacak şekilde bağlanır. Oluşan ağ iki boyutludur ve bu şekilde meydana gelen tabakalar birbirine zayıf Van der Waals kuvveti ile bağlanır. Bu yüzden, tabakala birbirlerinin üzerinde kolayca kayar. Grafit, yağ haline getirilip makinelerde, çalışan parçaların birbirine sürtünürken aşınmasını azaltmak ya da engellemek amacıyla yağlayıcı olarak kullanılır. Kurşun kalemlerin içindeki uç da, içine kil katılarak biraz sertleştirilmiş grafittir. Grafitin elde edildiği başlıca yerler Sri Lanka, Sibirya, Kuzey Amerika ve Meksika'dır. Grafit, kok kömürünün çok yüksek sıcaklıklarda işlenmesiyle yapay olarak da üretilebilir. Grafit çok yüksek sıcaklıklara dayanabilir, ayrıca çok iyi bir elektrik iletkenidir. Bu nedenle, çamaşır makinesi ve elektrikli süpürge gibi aygıtlardaki elektrik motorlarının fırçaları grafitten yapılır. Son dönemlerde, uzay kapsüllerinin ısı kalkanlarının yapımında da grafitten yararlanılmaya başlanmıştır.
Fullerenler
Ana başlık: Fulleren

Karbonun yapay allotropları olan Fullerenler, grafit benzeri yapılara sahiptir fakat grafit gibi saf altıgen değil, aynı zamanda beşgen ve hatta bazen yedigen kristaller de içerir. Bu yapı, altıgen kristallerden oluşan ana düzlemin kıvrılarak küreler, elipsoidler ve silindirler oluşturmasına yol açar. Fullerenlerin yapıları ve özellikleri nanomalzemeler alanında dev bir araştırma konusudur. "Fullerene" adı, bazı fullerenlerin benzediği jeodezik kubbeler tasarlayan Amerikalı mimar Richard Buckminster Fuller'e ithafen verilmiştir. Buckyball denen yapılar, üçgen karbon yapılarının küresel biçimlerde kapanmasından oluşan oldukça büyük moleküllerdir. En çok bilinen en basit buckyball molekülü, futbol topu benzeri yapısıyla C60 buckminsterfullerendir.[13] Karbon nanotüpler boş silindir şeklinde bir yapıya sahiptir.[14][15] Nanotomurcuklar ise, buckyball yapıların nanotüplerin dış duvarına kovalent bağla bağlanmasından oluşan nanotüp/buckyball melez yapısında malzemelerdir.[16]
Karbon bileşikleri
Karbonun oluşturduğu sayılamayacak kadar çok bileşik vardır. Karbon; karbon dioksit, kalsiyum karbonat (kireç taşı) gibi inorganik bileşiklerin yapısına katılabildiği gibi asıl olarak organik bileşiklerde bulunur. Hidrokarbonlar, alkoller, eterler, karboksilli asitler, aminler bunlardan yalnızca birkaçıdır.
Hidrokarbonlar
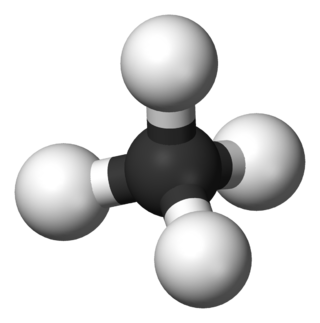
En basit hidrokarbon, bataklık gazı da denilen metan gazıdır; bu maddenin temel yapısı, ortadaki bir karbon atomunu çevreleyen dört hidrojen atomundan oluşur. Sibirya'da ya da Kuzey Denizi'nde yer altından çıkarılan doğal gazın başlıca bileşiği metan gazıdır. Metanın kimyasal formülü CH4 biçimindedir. Eğer dört karbon atomu birbirine bağlanırsa bütan gazı oluşur. Bütanın kimyasal formülü de C4H10'dur. Mutfaklarda kullanılan tüp gaz, bütan gazıdır. Metandaki hidrojen atomlarının yerine klor atomları geçirilirse, bir zamanlar önemli bir anestezik olan kloroform bileşikleri ve değerli bir kimyasal çözücü olan karbon tetraklorür oluşur. Metan molekülüne bir oksijen atomu bağlanırsa, ortaya bir tür alkol çıkar.
Karbon ile oksijenin oluşturduğu iki basit bileşik vardır: Karbon dioksit (CO2) ve karbon monoksit (CO). Her ikisi de gaz halindedir; ilki havada bulunur ikincisi ise çok zehirlidir.
Dünyanın pek çok yerindeki petrol yataklarından çıkarılan ham petrol, rafineriler de işlenerek, değişik uzunluktaki karbon zincirinden oluşan maddeler elde edilir; bu maddelere petrol türevleri denir. Ağır, kalın ya da ince bütün yağlar hidrokarbondur.
Karbon atomlarının hidrojenle doyurulmamış, yani tümüyle doldurulmamış olduğu hidrokarbon dizileri de vardır. bu dizilerin birinde karbon atomları birbirine çift bağ ile bağlanmıştır; bu tür hidrokarbonların en basit örneği etilen'dir. Üç bağlı karbon atomlarını içeren doymamış hidrokarbonlar dizisinin ilk üyesi de asetilen gazıdır.
Kömürün damıtılmasıyla elde edilen kalın, siyah renkli bir sıvı olan kömür katranından da önemli bir hidrokarbon dizisi oluşturulur. Bu dizinin ilk ve en basit üyesi benzendir. Benzen, bir halka biçiminde birbirine bağlanmış altı karbon atomu içerir. Bu dizide bulunan pek çok hidrokarbon, bitkilerden salınanlara benzeyen kokular yaydıklarından aromatik hidrokarbonlar olarak adlandırılırlar. Parfümler, en az bir benzen halkası içerir. Güvelere karşı kullanılan naftalin, birbiriyle birleşmiş iki halkadan oluşur.
Alkoller
Mono alkoller, CnH2n+1OH genel formülüne sahip, karbon atomuna doğrudan bağlı -OH (hidroksil) grubu bulunduran organik moleküllere denir. En basit üyesi metil alkoldür (CH3OH).
Kaynakça
- ^ Lide, D. R., (Ed.) (2005). CRC Handbook of Chemistry and Physics. CRC Press. ISBN 0-8493-0486-5.
- ^ Haaland, D (1976). "Graphite-liquid-vapor triple point pressure and the density of liquid carbon". Carbon. 14 (6): 357-361. doi:10.1016/0008-6223(76)90010-5.
- ^ Savvatimskiy, A (2005). "Measurements of the melting point of graphite and the properties of liquid carbon (a review for 1963–2003)". Carbon. 43 (6): 1115-1142. doi:10.1016/j.carbon.2004.12.027.
- ^ "Fourier Transform Spectroscopy of the Electronic Transition of the Jet-Cooled CCI Free Radical" (PDF). Erişim tarihi: 2007-12-06.
- ^ "Fourier Transform Spectroscopy of the System of CP" (PDF). Erişim tarihi: 2007-12-06.
- ^ "Carbon: Binary compounds". Erişim tarihi: 2007-12-06.
- ^ a b c d e Properties of diamond 17 Nisan 2012 tarihinde Wayback Machine sitesinde arşivlendi., Ioffe Institute Database
- ^ "Material Properties- Misc Materials". www.nde-ed.org. 6 Ocak 2004 tarihinde kaynağından arşivlendi. Erişim tarihi: 12 Kasım 2016.
- ^ Magnetic susceptibility of the elements and inorganic compounds 12 Ocak 2012 tarihinde Wayback Machine sitesinde arşivlendi., in Handbook of Chemistry and Physics 81st edition, CRC press.
- ^ Weast, Robert (1984). CRC, Handbook of Chemistry and Physics. Boca Raton, Florida: Chemical Rubber Company Publishing. ss. E110. ISBN 978-0-8493-0464-4.
- ^ Senese, Fred (9 Eylül 2000). "Who discovered carbon?". Frostburg State University. 5 Mart 2001 tarihinde kaynağından arşivlendi. Erişim tarihi: 24 Kasım 2007.
- ^ "History of Carbon and Carbon Materials - Center for Applied Energy Research - University of Kentucky". Caer.uky.edu. 23 Şubat 2009 tarihinde kaynağından arşivlendi. Erişim tarihi: 12 Eylül 2008.
- ^ H. W. Kroto, J. R. Heath, S. C. O'Brien, R. F. Curl ve R. E. Smalley (1985). "C60: Buckminsterfullerene". Nature. Cilt 318. s. 162-163. doi:10.1038/318162a0.
- ^ Ebbesen, TW, (Ed.) (1997). Carbon nanotubes—preparation and properties. Boca Raton, Florida: CRC Press.
- ^ MS Dresselhaus, G Dresselhaus, Ph Avouris, (Ed.) (2001). "Carbon nanotubes: synthesis, structures, properties and applications". Topics in Applied Physics. Cilt 80.
- ^ Nasibulin, Albert G. (2007). "A novel hybrid carbon material". Nature Nanotechnology. Cilt 2. s. 156–161. doi:10.1038/nnano.2007.37.