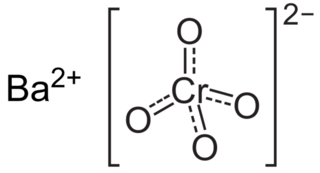Potasyum, bir kimyasal elementtir. Simgesi K ve atom numarası 19 dur. Potasyum adını izole edildiği Potas olarak da bilinen potasyum karbonattan almıştır. Potasyum yumuşak, gümüş-beyaz renkli alkali bir metaldir. Doğada deniz suyunda ve pek çok mineralde diğer elementlere bağlı olarak bulunur. Havada hızla oksitlenir ve suya karşı da çok aktiftir. Potasyum, pek çok açıdan sodyuma kimyasal olarak benzese de yaşayan organizmalarda, özellikle de hayvan hücrelerinde, sodyumdan farklı muamele görür. Kandaki seviyesinin düşük olmasına hipokalemi, yüksek olmasına hiperkalemi denir.

Ateş, yüksek sıcaklık ve çoğunlukla alev veren hızlı yanma olayıdır. Eski Türkçe od ve Farsça nâr sözcüğü de zaman zaman aynı anlamda kullanılır. Ateş, insan yaşamının vazgeçilmez unsurlarındandır ve kontrol altına alınması, medeniyetin ortaya çıkmasına olanak sağlamıştır.

Sodyum karbonat, (çamaşır sodası, kristal soda ve soda külü olarak da bilinir) Na2CO3 formülüne sahip değişik hidratları olan bir inorganik bileşiktir. Bütün formları beyaz, suda çözünür tuzlardır. Tüm formları güçlü bir alkali tada sahiptir ve suda orta derecede alkali çözeltiler verir. Tarihsel olarak sodyum bakımından zengin göl sularından veya sodyum bakımından zengin topraklarda yetişen bitkilerin küllerinden çıkarıldı. Bu sodyum açısından zengin bitkilerin külleri, potas üretmek için kullanılan odun küllerinden belirgin şekilde farklı olduğundan, "soda külü" olarak anıldı. Günümüzde ise, Solvay işlemi ile sodyum klorür ve kireç taşından büyük miktarlarda üretilmektedir.

Stronsiyum, Sr sembollüne sahip, atom numarası 38 olan, toprak alkali metaller grubundan gümüşümsü beyaz renkli bir kimyasal element. Oda sıcaklığında katı olan elementin atom ağırlığı 87,62 g/mol'dür. Stronsiyum, kimyasal olarak son derece reaktif olup, hava ile temas ettiği takdirde sarı rengine döner. Element sölestin ve strontianit minerallerinde bulunur. Elementin nükleer fisyon sonucunda oluşan 90Sr izotopu radyoaktiftir ve 28,90 yıllık bir yarılanma ömrüne sahiptir.

Zirkonyum metali ilk olarak 1789 yılında Martin Heinrich Klaproth tarafından keşfedilmiştir. 1824 yılında ise Jons Jakob Berzelius tarafından izole edilmiştir.

Tulyum, atom numarası 69, atom ağırlığı 168,9, yoğunluğu 9,3 olan, yaklaşık 1500 °C'de eriyen nadir element.

Kireç, kireç taşının çeşitli derecelerde (850-1450 °C) pişirilmesi sonucu elde edilen, suyla karıştırıldığında, tipine göre havada veya suda katılaşma özelliği gösteren, beyaz renkli, inorganik esaslı bir bağlayıcı madde türüdür.
Nitrik asit, HNO3 kimyasal formülüne sahip oldukça aşındırıcı bir inorganik asittir. Kezzap olarak da bilinir. Saf hâldeki bileşik renksizdir. Ancak uzun süre bekleyen eski asitler azot oksitleri ve suya ayrışması nedeniyle sarı renge dönebilme özelliğindedirler. Piyasada bulunan nitrik asitlerin çoğu % 68'lik bir konsantrasyona sahiptir. Çözelti, %86'dan fazla HNO3 içerdiğinde, dumanlı nitrik asit olarak adlandırılır. Mevcut azot dioksit miktarına bağlı olarak, dumanlı nitrik asit ayrıca %86’nın üzerindeki konsantrasyonlarda kırmızı dumanlı nitrik asit veya %95’in üzerindeki konsantrasyonlarda beyaz dumanlı nitrik asit olarak tanımlanır.
Kalsiyum oksit (CaO) ya da sönmemiş kireç geniş bir kullanım alanı bulunan bir çeşit kimyasal bileşiktir. Beyaz renkli, aşındırıcı ve alkalik bir katıdır. Sanayide kireç taşlarını yüksek sıcaklıklarda eriterek karbondioksidin uzaklaştırılmasıyla elde edilir. Suyla reaksiyona girerse oksitlenir ve kalsiyum hidroksidi oluşturur.
Hafniyum(IV) Oksit HfO2 şeklinde formüle edilen inorganik bir bileşiktir.

Kimyasal madde, kimyevî madde veya kısaca kimyasal, sabit bir kimyasal bileşimi ve karakteristik özelliklere sahip bir madde türüdür. Bu kimyasal bağlar bozulmadan, fiziksel ayırma yöntemleri ile bileşenlerine ayrılmaz. Bu kimyasallar katı, sıvı veya gaz hâlinde olurlar.

Yükseltgen madde bir yükseltgenme-indirgenme (redoks) reaksiyonunda başka bir türden bir elektron alan element ya da bileşiktir. Yükseltgen maddelerin elektron kazandıklarından dolayı indirgendikleri söylenebilir.

Potasyum ferrosiyanür formülü K4[Fe(CN)6] • 3H2O olan bir kimyasal bileşiktir. Potasyum ferrosiyanür metal kompleks bileşiğinin [Fe(CN)6]4− potasyum tuzudur. Bu tuz limon sarısı monoklinik kristallerden oluşmuştur.

Potasyum kromat, kimyasal formülü K2CrO4 olan inorganik bir bileşiktir. Bu sarı katı madde, kromat anyonunun potasyum tuzudur. Sodyum kromat endüstriyel öneme sahip iken potasyum kromat daha çok laboratuvarlarda kullanılır. Potasyum kromat, kanserojen sınıfında bir madde olup kategori 2 kapsamında değerlendirilmektedir.

Sodyum kromat Na2CrO4 formülüne sahip bir inorganik bileşiktir. Tetra-, hekza- ve dekahidratlar oluşturabilen sarı higroskopik bir katı olarak bulunur. Cevherlerinden krom özütlemesinde bir ara maddedir.
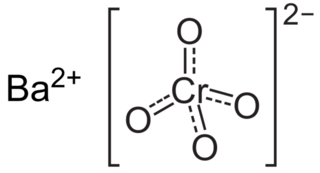
Baryum kromat, BaCrO4 formülüne sahip sarı renkli, kum gibi toz bir maddedir. Bilinen bir oksitleyici maddedir ve baryum iyonlarının bir sonucu olarak ısıtıldığında yeşil bir alev üretir.
Katı hâl kimyası, bazen malzeme kimyası olarak da adlandırılır, katı faz malzemelerinin, özellikle, ancak sadece moleküler olmayan katıların sentezi, yapısı ve özelliklerinin incelenmesidir. Bu nedenle, katı hal fiziği, mineraloji, kristalografi, seramik, metalurji, termodinamik, malzeme bilimi ve elektronik ile yeni malzemelerin sentezine ve karakterizasyonuna odaklanan güçlü bir örtüşmeye sahiptir. Katılar, ana partiküllerinin düzenlenmesinde mevcut olan düzenin doğasına göre kristal veya amorf olarak sınıflandırmak mümkündür.

Islak kimya, materyalleri analiz etmek için gözlem gibi klasik yöntemleri kullanan bir analitik kimya biçimidir. Analizlerin çoğu sıvı fazda yapıldığından ıslak kimya olarak adlandırılır. Islak kimya, laboratuvar tezgâhlarında birçok test yapıldığından, tezgâh kimyası olarak da bilinir.
Kromik asit terimi genellikle, katı krom trioksit de dahil olmak üzere çeşitli bileşikler içerebilen bir dikromata konsantre sülfürik asit eklenerek yapılan bir karışım için kullanılır. Bu tür kromik asit, cam için bir temizleme karışımı olarak kullanılabilir. Kromik asit ayrıca trioksitin anhidrit olduğu H2CrO4 moleküler türlerine de atıfta bulunabilir. Kromik asit, +6 (veya VI) oksidasyon durumunda krom içerir. Güçlü ve aşındırıcı bir oksitleyici ajandır.

Kalsiyum permanganat, mor kristal bir katıdır. Dezenfektan ve koku giderici olarak, Su arıtmada ve diğer birçok kullanım alanı vardır.