Patlayıcı madde, hararet veya şok tesiri ile kimyasal değişikliğe uğrayan, yüksek derecede ısı, çok hacimde gaz meydana getiren, katı, sıvı veya gaz hâlindeki kimyasal maddelerdir.

Kimyasal bileşik, kimyasal bağlarla bir arada tutulan birden fazla kimyasal elementin atomlarını içeren birçok özdeş molekülden oluşan kimyasal maddedir. Dolayısıyla tek bir elementin atomlarından oluşan bir molekül bileşik değildir. Bir bileşik, diğer maddelerle etkileşimi içerebilen kimyasal reaksiyonla farklı bir maddeye dönüştürülebilir. Bu süreçte atomlar arasındaki bağlar kırılabilir ve/veya yeni bağlar oluşabilir.
Toluen tinerin karakteristik kokusuna sahip renksiz, suda çözünmeyen bir sıvıdır. Toluen, bir fenil grubuna bağlı CH3'ten oluşan mono-substituent benzen türevidir. Bundan dolayı toluenin IUPAC sistematik adı metil benzendir. Toluen bir aromatik hidrokarbondur. Ayrıca TNT (trinitrotoluen) patlayıcı madde yapımında kullanılır.

Klorik asit (HClO3), klorun bir oksoasiti ve klorat tuzlarının formal öncülüdür. Güçlü bir asit (pKa ≈1) ve oksitleyici ajandır.

Kalsiyum karbonat, halk arasında kireç taşı olarak bilinen bir tür kimyasal bileşiktir. Bileşik formülü CaCO3 şeklindedir. Bu bileşik doğada en fazla eski kayaçlarda ve deniz kabuklarında bulunur. Kalsiyum karbonat, antiasitlerin bir üyesi olsa da, fazlası biyolojik olarak zararlıdır.

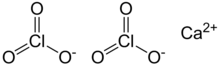
Klorat, ClO3− formülüyle gösterilen bir kimyasal kök. Bileşiklerinde daima bir adet elektron alır. Kloratlar, genel olarak klorik asitin tuzu olarak bilinirler. Klorat molekülleri organik bileşikleri kolayca oksitleyeceğinden dolayı kimyasal olarak zararlı bir maddedir. Geçmişte birçok patlayıcı ve havai fişekte kullanılan klorat, günümüzde yerini perklorata bırakmıştır.

Sodyum perklorat formülü NaClO4 olan bir kimyasal bileşiktir. Perklorik asitin sodyum tuzu olan bu bileşik diğer perkloratlar gibi kuvvetli bir oksitleyicidir. Sodyum perkloratın çözünürlüğü diğer perklorat tuzları içinde en yüksek olanıdır. Beyaz kristallerden oluşan ve higroskopik özellikte olan sodyum perklorat suda ve alkolde oldukça çok çözünür. Genellikle monohidrat form halinde bulunur ve rombik bir kristal yapısına sahiptir. Standart oluşum entalpisi −382.75 kJ mol−1 dir.

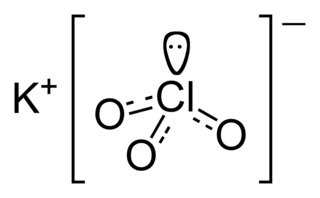
Potasyum perklorat formülü KClO4 olan bir kimyasal bileşiktir. Diğer perkloratlar gibi, bu tuz da güçlü bir oksitleyici olup potansiyel olarak birçok organik maddeyle reaksiyona girer. Havai fişek, mühimmat kapsülleri ve primer patlayıcılarda yaygın bir oksitleyici olarak kullanılan katı ve renksiz kristallerden oluşan bu madde çeşitli şekilde itici yakıtlar, flaş bileşimleri, yıldızlar ve maytaplarda da kullanılmaktadır. Daha yüksek performanslı amonyum perklorat yerine çoğu kez ikame edilerek katı yakıtlı roket itici yakıtı olarak da kullanılmıştır. KClO4 alkali metal perkloratlar içerisinde en düşük çözünürlüğe sahiptir (25 °C'deki 100 ml. suda 1.5 gr.).
Potasyum klorat formülü KClO3 olan bir kimyasal bileşiktir. Klorik asitin potasyum tuzu olan bu bileşik diğer kloratlar gibi kuvvetli bir oksitleyicidir.

Baryum klorat formülü Ba(ClO3)2 olanbeyaz kristal yapıya sahip bir kimyasal bileşiktir. Tüm çözünür baryum bileşikleri gibi tahriş edici ve zehirlidir. Klorik asitin baryum tuzu olan bu bileşik diğer kloratlar gibi kuvvetli bir oksitleyicidir. Bazen piroteknikte yeşil bir renk üretmek için kullanılır. Klorik asit üretiminde de kullanılır.

Sodyum klorat NaClO3 kimyasal formülüne sahip bir inorganik bileşiktir. Suda kolayca çözünür, beyaz kristal bir tozdur. Higroskopiktir. Sodyum klorat 300 °C’nin üzerinde ayrışarak oksijen ve sodyum klorür ortaya çıkar. Özellikle, çok parlak kâğıt imal etmek için ağartma hamurundaki uygulamalara yönelik olarak yılda birkaç yüz milyon ton üretilmektedir.

Baryum perklorat formülü Ba(ClO4)2 olan bir kimyasal bileşiktir. Perklorik asitin baryum tuzu olan bu bileşik diğer perkloratlar gibi kuvvetli bir oksitleyicidir. Piroteknik endüstrisinde kullanılır.
Magnezyum klorat formülü Mg(ClO3)2 olan bir kimyasal bileşiktir. Klorik asitin magnezyum tuzu olan bu bileşik diğer kloratlar gibi kuvvetli bir oksitleyicidir.
Kalsiyum iyodat formülü Ca(IO3)2 olan bir kalsiyum bileşiğidir. Kalsiyum iyodat un katkı maddesi olarak kullanılır. Bir oksitleyici olan kalsiyum iyodat losyon ve merhemlere antiseptik ve deodorant olarak da katılır. Ayrıca, tavuk yeminde katkı maddesi olarak da kullanılabilmektedir.

Sodyum iyodat, (NaIO3) iyodik asitin sodyum tuzudur. Sodyum iyodat oksitleyici madde olduğundan, yanıcı maddeler ya da indirgeyici maddelerle temas ettiğinde alev almalarına sebep olabilir.

Yükseltgen madde bir yükseltgenme-indirgenme (redoks) reaksiyonunda başka bir türden bir elektron alan element ya da bileşiktir. Yükseltgen maddelerin elektron kazandıklarından dolayı indirgendikleri söylenebilir.

Dumansız barut, karabarutun aksine ateşlendiğinde önemsiz miktarda duman üreten ve ateşli silahlar ve top (silah)larda kullanılan bazı itici yakıtlara verilen addır. Dumansız barutun ilk üretildiği yıllarda "Balistit" ve "Kordit" gibi tescilli adları olmasına karşın günümüzde bu terimler pek kullanılmamaktadır.

Gümüş klorat (AgClO3) beyaz tetragonal kristaller formundadır. Tüm kloratlar gibi suda çözünür ve oksitleyici bir maddedir. Basit bir metal tuzu olarak, temel inorganik kimya deneylerinde kullanılan yaygın bir kimyasaldır. Işığa duyarlıdır, bundan dolayı oldukça koyu renkli kapalı kaplarda saklanmalıdır.

İyodik asit, HIO3, beyaz veya kirli beyaz bir katı madde olarak elde edilebilir. Suda çok iyi çözünür, ancak klorik asit veya bromik asidin aksine saf halde bulunur. İyodik asit +5 oksidasyon durumunda iyot içerir ve halojenlerin saf halde en stabil okso-asitlerinden biridir. İyot asidi dikkatle ısıtıldığında pentoksit iyice dehidre olur. Daha sonraki ısıtmada, iyot pentoksit ayrıca iyot, oksijen ve düşük iyot oksitleri karışımı vererek ayrışır.

Sodyum kromat Na2CrO4 formülüne sahip bir inorganik bileşiktir. Tetra-, hekza- ve dekahidratlar oluşturabilen sarı higroskopik bir katı olarak bulunur. Cevherlerinden krom özütlemesinde bir ara maddedir.