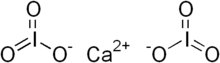Flor, atom numarası 9, atom ağırlığı 19, yoğunluğu 1,265 olan, kokusu ozonu andıran, kahverengimsi sarı renkte, halojenler grubunun ilk elementidir. 1529 yılında Georgius Agricola, kalsiyum florür bileşiğini tanımlamıştır. İlk defa 1886 yılında Henri Moissan tarafından izole edilmiştir.

Kalsiyum, toprak alkalileri grubundan metalik bir element. Sembolü "Ca"dır. İsmi Latincede “kireç” anlamına gelen “calx” sözcüğünden gelmektedir. İlk defa 1808'de Humphry Davy tarafından kalsiyum hidroksitten elektroliz yoluyla elde edilmiştir.

İyot, sembolü I, atom numarası 53 olan bir elementtir. Kimyasal olarak iyot halojenlerin en az reaktif olanı, astatin'den sonra en elektropozitif olanıdır. İyot başlıca tıpta, fotoğrafçılıkta ve boya imalatında kullanılır. Çoğu canlının eser miktarda iyota gereksinimi vardır.
İnorganik kimya veya anorganik kimya; organik olmayan, yani karbon-hidrojen bağı içermeyen bileşiklerin özelliklerini ve kimyasal davranışlarını inceleyen kimya dalı. Anorganik ve organik kimyayı birleştiren organometalik bileşikler, organometalik kimya adında başka bir dalı oluşturur.

Lutesyum, atom numarası 71, atom ağırlığı 174,967 olan, iterbiyumun çözüşmesi ile oluşan, renksiz tuzlar veren, henüz uygulama alanı olmayan çok ender bir element. Sembolü Lu.

Kimyasal bileşik, kimyasal bağlarla bir arada tutulan birden fazla kimyasal elementin atomlarını içeren birçok özdeş molekülden oluşan kimyasal maddedir. Dolayısıyla tek bir elementin atomlarından oluşan bir molekül bileşik değildir. Bir bileşik, diğer maddelerle etkileşimi içerebilen kimyasal reaksiyonla farklı bir maddeye dönüştürülebilir. Bu süreçte atomlar arasındaki bağlar kırılabilir ve/veya yeni bağlar oluşabilir.

Tahta, ağaçların gövdelerini ve dallarını meydana getiren sert bir maddedir. İnşaat malzemesi, kâğıt ve yakıt yapımında ham madde olarak kullanılmaktadır. Ayrıca tahta yalıtkan bir maddedir. Tahtanın biraz ıslatılmış hâli ise iletken olur. Böylelikle elektrik çarpmaları gibi durumlarda kuru tahtadan yararlanılabilir.
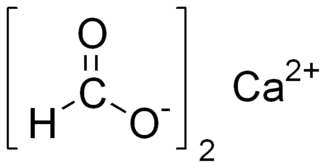
Kalsiyum format, Ca(HCOO)2, formik asitin kalsiyum tuzudur. Görünümü beyaz toz olan bu madde, yüksek sıcaklıkta bozunur. Molekül ağırlığı 130.12 g/mol, yoğunluğu 20 °C'de 1.15 g/cm³ ve sudaki çözünürlüğü 20 °C'de 16 g/100g su olarak verilmiştir.
Kalsiyum oksit (CaO) ya da sönmemiş kireç geniş bir kullanım alanı bulunan bir çeşit kimyasal bileşiktir. Beyaz renkli, aşındırıcı ve alkalik bir katıdır. Sanayide kireç taşlarını yüksek sıcaklıklarda eriterek karbondioksidin uzaklaştırılmasıyla elde edilir. Suyla reaksiyona girerse oksitlenir ve kalsiyum hidroksidi oluşturur.

İyodat, kimyasal formülü IO3− olan bir iyodik asit tuzudur. İyodat anyonunda iyot üç oksijen atomuna bağlıdır. İyodatın moleküler geometrisi üç köşeli piramittir.

Tofu, Japonya, Tayland ve Çin'de yenilen soya ile yapılan tipik Uzak Doğu yemeğidir.

Kalsiyum karbonat, halk arasında kireç taşı olarak bilinen bir tür kimyasal bileşiktir. Bileşik formülü CaCO3 şeklindedir. Bu bileşik doğada en fazla eski kayaçlarda ve deniz kabuklarında bulunur. Kalsiyum karbonat, antiasitlerin bir üyesi olsa da, fazlası biyolojik olarak zararlıdır.

Sodyum iyodat, (NaIO3) iyodik asitin sodyum tuzudur. Sodyum iyodat oksitleyici madde olduğundan, yanıcı maddeler ya da indirgeyici maddelerle temas ettiğinde alev almalarına sebep olabilir.
Kalsiyum klorat kimyasal formülü Ca(ClO3)2 olan bir bileşiktir. Klorik asitin kalsiyum tuzudur. Potasyum klorat gibi, kuvvetli bir oksitleyici olan bu bileşik, piroteknik formülasyonlarda kullanılabilir. Kalsiyum klorat kuvvetle ısıtıldığında ya da organik madde gibi indirgeyici maddelerle karıştırıldığında patlayabilir.

Hipoiyodöz asit, HOI kimyasal formülü ile gösterilen inorganik bir bileşiktir. Sulu bir iyot çözeltisinin cıva veya gümüş tuzları ile işlenmesi durumunda oluşur. Disproporsiyonlaşma ile hızla ayrışır:
- 5 HOI → HIO3 + 2I2 + 2H2O

İyodöz asit, HIO2 formülüne sahip kimyasal bileşiktir. Tuzları iyoditler olarak adlandırılır; oldukça kararsızdır ve hiçbir zaman izole edilmemiştir. Moleküler iyot ve iyodatlara hızlı şekilde ayrışır.

İyodik asit, HIO3, beyaz veya kirli beyaz bir katı madde olarak elde edilebilir. Suda çok iyi çözünür, ancak klorik asit veya bromik asidin aksine saf halde bulunur. İyodik asit +5 oksidasyon durumunda iyot içerir ve halojenlerin saf halde en stabil okso-asitlerinden biridir. İyot asidi dikkatle ısıtıldığında pentoksit iyice dehidre olur. Daha sonraki ısıtmada, iyot pentoksit ayrıca iyot, oksijen ve düşük iyot oksitleri karışımı vererek ayrışır.

Potasyum iyodat (KIO3) bir kimyasal bileşiktir. K+ ve IO3− iyonlarından oluşur. Potasyum iyodat oksitleyici bir maddedir ve bu nedenle yanıcı maddelerle temas ettiğinde yangına neden olabilir. Suda ve sülfürik asitte çözünür; alkolde çözünmez.

Buz çözme, yani diğer adıyla anti Icıng yüzeydeki kar, buz veya donu temizleme işlemidir. Buzlanmayı önleme, sadece buzdan arınmakla kalmayan, aynı zamanda yüzeyde kalan ve belirli bir süre boyunca buzun yeniden oluşmasını geciktiren veya mekanik olarak çıkarmayı kolaylaştırmak için buzun yüzeye yapışmasını önleyen kimyasal maddelerin uygulanmasıdır.
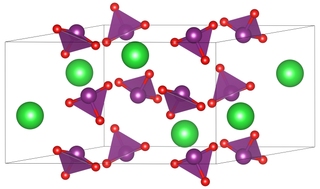
Baryum iyodat, kimyasal formülü Ba(IO3)2 olan inorganik bir kimyasal bileşiktir. Beyaz, granül bir maddedir.