
Rubidyum, Rb sembolü ile gösterilen, 37 atom numarasına sahip alkali metaller grubundan bir kimyasal element. 1861 yılında Gustav Kirchhoff ve Robert Bunsen tarafından Almanya'da keşfedilmiştir. Kimyasal açıdan potasyum ve sezyumun özelliklerine benzer özellikler gösterir ama potasyuma oranla çok ender bulunur. Oda sıcaklığında gümüşi beyaz renkli, yumuşak ve parlak bir katıdır. Kuru havada bile çok çabuk yükseltgenir, bu yüzden açık havada saklanamaz. Suyu şiddetle ayrıştırır ve ortaya çıkan hidrojeni tutuşturur.

Kireç taşı genellikle mercan, foraminifera ve yumuşakçalar gibi deniz canlılarının iskelet parçalarından oluşan bir karbonat tortul kayaçtır. Başlıca maddeleri kalsiyum karbonatın farklı kristal formları olan kalsit ve aragonit minerallerdir. Yakından ilişkili bir kaya, yüksek oranda mineral dolomit içeren dolomittir. Eski USGS yayınlarında, dolomit magnezyum kireç taşı olarak anılırdı, artık magnezyum eksikliği olan dolomitler veya magnezyum açısından zengin kalkerler olarak ayrılmıştır.

Kalsit, kimyasal formülü CaCO3 olan kristalleşmiş kalsiyum karbonat. Saydam, beyaz, sarı, rustik yeşil ve mavimsi renkte olabilir. Sertliği 3, özgül ağırlığı 2.71'dir. Soğuk ve seyreltik hidroklorik asitte (tuz ruhu) şiddetli bir köpürme ile ayrışır. Çakı ile çizilir. CO2'li sularda çözünerek Ca(HCO3)2 yapar.

Kalsiyum, toprak alkalileri grubundan metalik bir element. Sembolü "Ca"dır. İsmi Latincede “kireç” anlamına gelen “calx” sözcüğünden gelmektedir. İlk defa 1808'de Humphry Davy tarafından kalsiyum hidroksitten elektroliz yoluyla elde edilmiştir.

Sodyum karbonat, (çamaşır sodası, kristal soda ve soda külü olarak da bilinir) Na2CO3 formülüne sahip değişik hidratları olan bir inorganik bileşiktir. Bütün formları beyaz, suda çözünür tuzlardır. Tüm formları güçlü bir alkali tada sahiptir ve suda orta derecede alkali çözeltiler verir. Tarihsel olarak sodyum bakımından zengin göl sularından veya sodyum bakımından zengin topraklarda yetişen bitkilerin küllerinden çıkarıldı. Bu sodyum açısından zengin bitkilerin külleri, potas üretmek için kullanılan odun küllerinden belirgin şekilde farklı olduğundan, "soda külü" olarak anıldı. Günümüzde ise, Solvay işlemi ile sodyum klorür ve kireç taşından büyük miktarlarda üretilmektedir.

Kral suyu, asitlerin az etki ettiği ya da etki etmediği altın ve platin gibi metallerle tepkimeye girebilen kuvvetli bir asit çözeltisidir. Hidroklorik asit ve nitrik asitin 3:1 oranında karıştırılmasıyla oluşur. Ebu Musa Câbir bin Hayyan tarafından bulunduğu tahmin edilmektedir.

Redoks atomların oksidasyon durumlarının değiştiği bir tür kimyasal reaksiyondur. Redoks reaksiyonları, kimyasal türler arasında elektronların fiili veya biçimsel aktarımı ile karakterize edilir, çoğunlukla bir tür oksidasyona, diğer türler indirgemeye uğrar. Elektronun çıkarıldığı kimyasal türlerin indirgenmiş olduğu söyleniyor. Başka bir deyişle:
- Oksidasyon, elektronların bir atom ya da molekülden ayrılmasını sağlayan kimyasal tepkimedir.
- Redüksiyon, bir atomun elektron almasını sağlayan kimyasal tepkimedir.
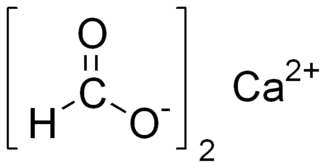
Kalsiyum format, Ca(HCOO)2, formik asitin kalsiyum tuzudur. Görünümü beyaz toz olan bu madde, yüksek sıcaklıkta bozunur. Molekül ağırlığı 130.12 g/mol, yoğunluğu 20 °C'de 1.15 g/cm³ ve sudaki çözünürlüğü 20 °C'de 16 g/100g su olarak verilmiştir.

Kireç, kireç taşının çeşitli derecelerde (850-1450 °C) pişirilmesi sonucu elde edilen, suyla karıştırıldığında, tipine göre havada veya suda katılaşma özelliği gösteren, beyaz renkli, inorganik esaslı bir bağlayıcı madde türüdür.

Alçı taşı, kalsiyum sülfat dihidrattan oluşan yumuşak bir sülfat mineralidir ve kimyasal formül CaSO4 · 2H2O'dur. Alçıtaşı ayrıca selenitin yarı saydam kristalleri olarak kristalleşir. Aynı zamanda bir evaporit minerali ve anhidritin hidrasyon ürünü olarak oluşur. İçinde su bulunan kalsiyum sülfat minerali, tek veya ikiz sütunlar hâlinde billûrlanır. Alçı billurlarına kil ve marn içinde veya tuzlu ve alçılı dağların boşluklarında rastlanır.
Kalsiyum oksit (CaO) ya da sönmemiş kireç geniş bir kullanım alanı bulunan bir çeşit kimyasal bileşiktir. Beyaz renkli, aşındırıcı ve alkalik bir katıdır. Sanayide kireç taşlarını yüksek sıcaklıklarda eriterek karbondioksidin uzaklaştırılmasıyla elde edilir. Suyla reaksiyona girerse oksitlenir ve kalsiyum hidroksidi oluşturur.
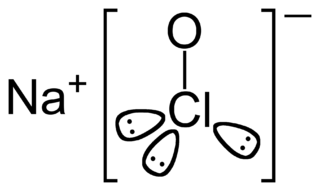
Sodyum hipoklorit, (NaClO) bir tür tuzdur. Günlük hayatta beyazlatıcı çamaşır sularında kullanılmaktadır. Oda koşullarındaki klor ile sabunlardaki sodyum hidroksit tepkimeye sokularak üretilmektedir.

Hidroksit, kimya biliminde, oksijen ve hidrojen atomları içeren diatomik anyonun adıdır. Genellikle bir bazın parçalanması sonucu ortaya çıkar. Bilinen en basit diatomik iyonlardan biridir.
Kalsiyum hipoklorit, Ca(ClO)2 formülüyle gösterilen bir hipoklorit tuzudur. Günlük hayatta su arıtım ve havuz temizleme sistemleri ve sıvı çamaşır suyunda kullanılmaktadır.

Kalsiyum karbonat, halk arasında kireç taşı olarak bilinen bir tür kimyasal bileşiktir. Bileşik formülü CaCO3 şeklindedir. Bu bileşik doğada en fazla eski kayaçlarda ve deniz kabuklarında bulunur. Kalsiyum karbonat, antiasitlerin bir üyesi olsa da, fazlası biyolojik olarak zararlıdır.

Asetat genellikle sulu çözeltiler içinde bulunan negatif iyon ya da anyon. Kimyasal formülü C2H3O2-,CH3CO2- veya CH3COO- şeklinde ifade edilir. Asetik asidin tuzu veya esteridir. Sanayide yılda 5 milyar kilogram asetik asit asetat üretiminde kullanılır. Doğada, asetat sentez için en yaygın yapı taşıdır. Örneğin, yağ asitleri büyüyen yağ asidi için asetat iki karbon atomu bağlanarak üretilir.

Baryum asetat (Ba(C2H3O2)2) baryum(II) ve asetik asitin tuzu.

Buz çözme, yani diğer adıyla anti Icıng yüzeydeki kar, buz veya donu temizleme işlemidir. Buzlanmayı önleme, sadece buzdan arınmakla kalmayan, aynı zamanda yüzeyde kalan ve belirli bir süre boyunca buzun yeniden oluşmasını geciktiren veya mekanik olarak çıkarmayı kolaylaştırmak için buzun yüzeye yapışmasını önleyen kimyasal maddelerin uygulanmasıdır.

Kalsiyum nitrat, (Norveç güherçilesi) olarak da adlandırılır. Ca(NO3)2 formülüne sahip bir inorganik bileşiktir. Bu renksiz tuz havadan nem çeker ve genellikle bir tetrahidrat olarak bulunur. Esas olarak gübrelerde bileşen olarak kullanılırsa da başka uygulamalarda da kullanılır. Nitrokalsit, çiftlik gübresinin ahır veya mağaralarda olduğu gibi kuru bir ortamda beton veya kireç taşı ile temas ettiği yerlerde bir çiçeklenme olarak oluşan hidratlı bir kalsiyum nitrat olan bir mineralin adıdır. Kalsiyum amonyum nitrat dekahidrat ve kalsiyum potasyum nitrat dekahidrat dahil çeşitli ilgili tuzları bilinmektedir.

Suyun sertliği veya sert su, yüksek mineral içeriğine sahip sudur. Suyun sertliği, büyük ölçüde kalsiyum ve magnezyum karbonatlar, bikarbonatlar ve sülfatlardan oluşan kireç taşı veya alçıtaşı birikintilerinden su sızdığında oluşur.





















