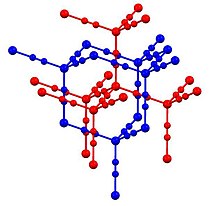
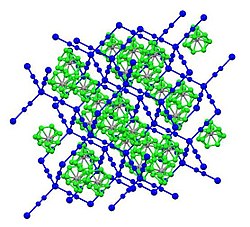
Siyanür, bir karbon ve ona üçlü bağ ile bağlanmış bir azot içeren C≡N grubuna sahip kimyasal bileşiklere verilen addır. Bu grup aynı zamanda siyano grubu olarak da bilinir. Organik ve inorganik çeşitleri bulunan siyanürler özellikle endüstride kullanılmaları için üretilmektedir. İnorganik siyanüre örnek olarak çok zehirli potasyum siyanür, organik siyanüre örnek olarak da düşük toksisiteli asetonitril verilebilir. Her siyanür yüksek oranda zehirli değildir.

Karbon, doğada yaygın bulunan ametal kimyasal elementtir. Evrende bolluk bakımından altıncı sırada yer alan karbon, kızgın yıldızlarda hidrojenin termonükleer yanmasında temel rol oynar. Dünyada hem doğal halde, hem de başka elementlerle bileşik halinde bulunan karbon, ağırlık olarak Dünya'nın yerkabuğunun yaklaşık %0,2'sini oluşturur. En arı (katışıksız) biçimleri elmas ve grafittir; daha düşük arılık derecelerinde maden kömürünün, kok kömürünün ve odun kömürünün bileşeni olarak bulunur. Atmosferin yaklaşık % 0,05'ini oluşturan ve bütün doğal sularda erimiş olarak bulunan karbon dioksit, kireç taşı ve mermer gibi karbonat mineralleri, kömürün, petrolün ve doğalgazın başlıca yapıtaşları olan hidrokarbonlar, en bol bulunan bileşikleridir.

Kükürt, simgesi S, atom numarası 16 olan, limon sarısında ametal, yalın katı bir elementtir.

Gümüş, elementlerin periyodik tablosunda simgesi Ag olan, beyaz, parlak, değerli bir metalik element. Atom numarası 47, atom ağırlığı 107,87 gramdır. Erime noktası 961,9 °C, kaynama noktası 1950 °C ve özgül ağırlığı da 10,5 g/cm³'tür. Çoğu bileşiklerinde +1 değerliklidir. Günümüzde Dünya'da 55 yıllık gümüş rezervi kaldığı tahmin ediliyor. Yeni gümüş rezervleri keşfedilmezse 2078 yılında Dünya'daki gümüş rezervlerinin tükenebileceği tahmin ediliyor. En çok gümüş üretimi yapan ülkeler Meksika, Çin, Peru Şili ve Avustralya'dır.

Çinko, sembolü Zn, atom numarası 30 olan kimyasal bir elementtir. Oda sıcaklığında hafif kırılgan bir metaldir ve oksidasyon giderildiğinde parlak gri bir görünüme kavuşur. Periyodik tablonun 12. (IIB) grubunun ilk elementidir. Bazı açılardan çinko kimyasal olarak magnezyuma benzer: her iki element de yalnızca bir normal oksidasyon durumu (+2) gösterir ve Zn2+ ve Mg2+ iyonları benzer boyuttadır. Çinko, Dünya kabuğundaki en bol bulunan 24. element olup beş kararlı izotopu vardır. En yaygın çinko cevheri, bir çinko sülfür minerali olan sfalerittir.

Kadmiyum, kimyasal simgesi Cd olan, gümüş beyazlığında, elektrik, seramik, pil ve akü sanayisinde kullanılan yumuşakça, kanserojen, toksik bir ağır metal element. Kadmiyum, çinko bileşikleriyle beraber doğada kadmiyum sülfür olarak bulunur. Çinko, kurşun ve bakırın yan ürünü olarak üretilir.

Arsenik sembolü As atom numarası 33 olan elementtir. Arsenik, çoğu mineralde, genellikle kükürt ve metallerle bir arada veya saf bir element kristali olarak bulunur. Arsenik bir metaloiddir. Çeşitli allotroplara sahiptir, ancak yalnızca metalik bir görünüme sahip gri form endüstri için önemlidir.

Organik kimya, organik bileşiklerin ve organik maddelerin yani karbon atomlarını içeren çeşitli formlardaki maddelerin yapısını, özelliklerini ve reaksiyonların bilimsel çalışmasını içeren, kimyanın bir alt dalıdır. Yapının incelenmesi yapısal formüllerini belirler. Özelliklerin incelenmesi, fiziksel ve kimyasal özellikleri ve davranışlarını anlamak için kimyasal reaktivitenin değerlendirilmesidir. Organik reaksiyonların incelenmesi doğal ürünlerin, ilaçların ve polimerlerin kimyasal sentezini ve bireysel organik moleküllerin laboratuvarda ve teorik çalışma yoluyla incelenmesidir.

Asetilen (etin), bir tür hidrokarbondur. Üçlü bağ taşır ve formülü C2H2 şeklindedir. Alkin sınıfının ilk üyesidir.
Ağır metal, metalik özellikler gösteren elementlerden oluşan, açık ve tam bir tanımlaması yapılmamış olan grupta bulunan elementlere verilen addır. Bu grubun içinde geçiş metalleri, bazı yarı metaller, lantanitler ve aktinitler bulunur. Bazıları yoğunluk, bazıları atomik sayı ya da atomik ağırlık, bazıları da kimyasal özellikler ya da toksisite üzerine dayanan birçok tanımlama önerilmiştir. Tutarsız tanımlamalar ve tutarlı bir bilimsel temeli olmaması nedeniyle IUPAC’ın bir teknik raporunda ağır metal teriminin "anlamsız ve yanlış yönlendirici" olduğu belirtilmiştir. Duruma göre ağır metaller karbondan hafif elementleri içerdiği gibi en ağır metallerin bazılarını dışarıda tutabilir.

Sülfürik(VI) asit ya da halk arasında bilinen ismi ile zaç yağı, H2SO4, güçlü bir mineral asididir. Olası kâşifi 8. yüzyıl simyacısı Cabir bin Hayyan tarafından yenime uğratıcı, renksiz ve yoğunluğu yüksek sıvı olarak tanımlanmıştır. Suda her konsantrasyonda çözünebilir. Büyük ölçüde korozif oluşu, güçlü asidik yapısından ve dehidrasyon özelliğinden kaynaklanmaktadır.
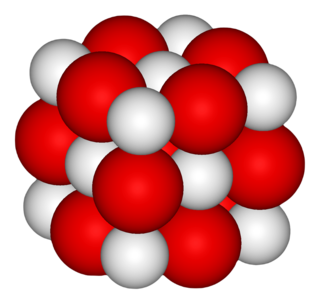
Kalsiyum oksit (CaO) ya da sönmemiş kireç geniş bir kullanım alanı bulunan bir çeşit kimyasal bileşiktir. Beyaz renkli, aşındırıcı ve alkalik bir katıdır. Sanayide kireç taşlarını yüksek sıcaklıklarda eriterek karbondioksidin uzaklaştırılmasıyla elde edilir. Suyla reaksiyona girerse oksitlenir ve kalsiyum hidroksidi oluşturur.

Silisyum dioksit veya silika, oksijen ve silisyum içeren kimyasal bileşik. Kimyasal formülü SiO2'dir. 16. yüzyıldan beri bilinmektedir. Cam, beton, fayans, porselen gibi birçok maddede kullanılmaktadır. SiO2, daha çok herhangi bir malzeme yerine, kristalin formları (polimorf) şeklinde bulunmaktadır. Kuvars, topaz ve ametist gibi 17 farklı kristal formu vardır.

Potasyum ferrosiyanür formülü K4[Fe(CN)6] • 3H2O olan bir kimyasal bileşiktir. Potasyum ferrosiyanür metal kompleks bileşiğinin [Fe(CN)6]4− potasyum tuzudur. Bu tuz limon sarısı monoklinik kristallerden oluşmuştur.

Çinko siyanür, Zn(CN)2 formüllü ile gösterilen bir inorganik bileşiktir. Esas olarak çinko kaplamada kullanılan beyaz renkli bir katıdır, ancak organik bileşiklerin sentezi için daha özel uygulamalara da sahiptir.
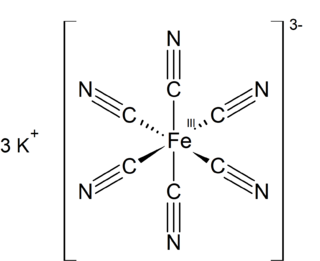
Potasyum ferrisiyanür K3[Fe(CN)6] formülü ile gösterilen inorganik bileşiktir. Bu parlak kırmızı tuz, oktahedral olarak koordine edilmiş [Fe(CN)6]3− iyonu içerir. Suda çözünür ve çözeltisi bir miktar yeşil-sarı flüoresans gösterir. 1822 yılında Leopold Gmelin tarafından keşfedilmiştir ve başlangıçta ultramarin boyalarının üretiminde kullanılmıştır.
2-Nitrotoluen veya orto-nitrotoluen CH3C6H4NO2 formülüne sahip bir organik bileşiktir. α (−9.27 °C) ve β (−3.17 °C) olarak iki formda kristalleşen soluk sarı bir sıvıdır. Esas olarak, çeşitli boyaların üretiminde bir ara madde olan o-toluidinin öncül maddesisir.

Antimon trisülfür (Sb2S3) doğada kristal stibnit minerali ve amorf yapılı kırmızı metastibnit minerali olarak bulunur. emniyet kibritlerinde, askeri mühimmatlarda, patlayıcı maddelerde ve havai fişeklerde kullanılmak için üretilmektedir. Ayrıca yakut renkli cam üretiminde ve plastiklerde alev geciktirici olarak kullanılır. Tarihsel olarak stibnit formu, 16. yüzyılda üretilen resimlerde gri bir pigment olarak kullanılmıştır. 1.8-2.5 eV direkt bant aralığına sahip bir yarı iletkendir. Uygun katkılama ile, p ve n tipi malzemeler üretilebilir.

Baryum klorür, BaCl2 formüllü inorganik bir bileşik'tir. Bu bileşik baryum'un suda-çözünen en yaygın tuzlarından biridir. Diğer baryum tuzlarının çoğu gibi, baryum klorür beyaz toz halinde ve zehirlidir. Alevde sarı-yeşil renk verir. Ayrıca higroskopiktir, ilk önce dihidrat BaCl2(H2O)2' ye dönüşür.

Disiyanoasetilen, C
4N
2 kimyasal formülüne sahip bir karbon ve azot bileşiğidir. Alternatif üçlü ve tek kovalent bağlarla N≡C−C≡C−C≡N doğrusal bir moleküler yapıya sahiptir. İki hidrojen atomunun siyanür grupları ile değiştirildiği asetilen olarak görülebilir.