Alkali metaller periyodik tablonun birinci grubunda yer alan metallerdir. Fransiyum dışında hepsi, yumuşak yapıda ve parlak görünümdedir.

Sodyum, periyodik cetvelde Na simgesi ile gösterilen ve atom numarası 11 olan element. Sodyum yumuşak ve kaygan bir metal olup alkali metaller grubuna aittir. Doğal bileşiklerin içinde bol miktarda bulunur. Yüksek oranda reaktiftir, sarı bir alevle yanar, su ile şiddetli reaksiyon verir ve havada hızla oksitlenir. Dolayısıyla, vazelin, gazyağı gibi hava ve su ile temasını kesecek bir ortamda saklanması gerekir.

Kalsiyum, toprak alkalileri grubundan metalik bir element. Sembolü "Ca"dır. İsmi Latincede “kireç” anlamına gelen “calx” sözcüğünden gelmektedir. İlk defa 1808'de Humphry Davy tarafından kalsiyum hidroksitten elektroliz yoluyla elde edilmiştir.

Klor, VIIA grubunda bulunan hafif, keskin kokulu, yeşilimsi sarı renkli, tahriş edici ve zehirleyici bir gaz. Havadan 2,5 kat ağır olan klor ilk zamanlar bir bileşik olarak kabul ediliyordu. Klor ilk olarak 1774 yılında Carl Wilhelm Scheele tarafından keşfedildi. 1810 yılında ise bugünkü ismi Humphry Davy tarafından verildi.
Kararsız bir asit olan tiyosülfat asidinden türeyen S2O3−2 formülüne sahip olan eksi yüklü bir kök. Bir maddede tiyosülfat iyonunun olup olmadığını anlamak için madde üzerine asit ilave edilir. Eğer çözeltide bulunma, yani serbest kükürt meydana gelmesi olursa maddede tiyosülfat vardır. Ayrıca, kendine has kokusuyla kükürt dioksit gazı da meydana gelir. Bu olaylar tiyosülfatın kararsız olduğunu da gösterir:
- 2H + S2O2-3 → H2S2O3 → S + H2O + SO2

Üre (Latince Urea Pura), organik bir bileşik. Formülü H2N-CO-NH2'dir. Karbonik asidin diamidi olan üre aynı zamanda karbamik asidin de amidi olduğundan karbamid adı ile de bilinir.
İnorganik kimya veya anorganik kimya; organik olmayan, yani karbon-hidrojen bağı içermeyen bileşiklerin özelliklerini ve kimyasal davranışlarını inceleyen kimya dalı. Anorganik ve organik kimyayı birleştiren organometalik bileşikler, organometalik kimya adında başka bir dalı oluşturur.

Çamaşır suyu, genellikle etken madde olarak sodyum hipoklorit (NaClO) içeren ağartma, temizlik ve hijyen amacıyla kullanılan kimyasal maddedir.

Kimyasal bileşik, kimyasal bağlarla bir arada tutulan birden fazla kimyasal elementin atomlarını içeren birçok özdeş molekülden oluşan kimyasal maddedir. Dolayısıyla tek bir elementin atomlarından oluşan bir molekül bileşik değildir. Bir bileşik, diğer maddelerle etkileşimi içerebilen kimyasal reaksiyonla farklı bir maddeye dönüştürülebilir. Bu süreçte atomlar arasındaki bağlar kırılabilir ve/veya yeni bağlar oluşabilir.
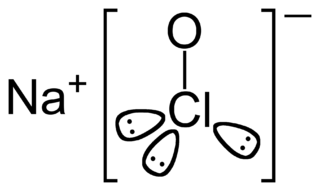
Sodyum hipoklorit, (NaClO) bir tür tuzdur. Günlük hayatta beyazlatıcı çamaşır sularında kullanılmaktadır. Oda koşullarındaki klor ile sabunlardaki sodyum hidroksit tepkimeye sokularak üretilmektedir.

Sodyum bikarbonat ya da soda kimyasal formülü NaHCO3 olan bir kimyasal bileşiktir. Kabartma tozu olarak da bilinir. Sodyum tuzlarından birisidir. Antiasit özelliği vardır. Kabartma tozu olarak da kullanılır. Suda çözünür. Beyaz katı kristal tozdur. Sodyum karbonat'ı andıran hafif alkali tadı vardır. Salin solüsyonu bileşiminde de kullanılır.

Lityum hipoklorit (LiClO) saydam, renksiz ve berrak bir tür tuz çeşididir. Bu madde çoğu yerde havuz sterilizasyonu için ve kimi maddeler için ayrıştırıcı madde olarak kullanılmaktadır.
Kalsiyum hipoklorit, Ca(ClO)2 formülüyle gösterilen bir hipoklorit tuzudur. Günlük hayatta su arıtım ve havuz temizleme sistemleri ve sıvı çamaşır suyunda kullanılmaktadır.

Kalsiyum karbonat, halk arasında kireç taşı olarak bilinen bir tür kimyasal bileşiktir. Bileşik formülü CaCO3 şeklindedir. Bu bileşik doğada en fazla eski kayaçlarda ve deniz kabuklarında bulunur. Kalsiyum karbonat, antiasitlerin bir üyesi olsa da, fazlası biyolojik olarak zararlıdır.

Hipokloröz asit, HOCl formülüne sahip bir zayıf asittir.

Potasyum ferrosiyanür formülü K4[Fe(CN)6] • 3H2O olan bir kimyasal bileşiktir. Potasyum ferrosiyanür metal kompleks bileşiğinin [Fe(CN)6]4− potasyum tuzudur. Bu tuz limon sarısı monoklinik kristallerden oluşmuştur.
Halojenür, bir kısmı halojen atom diğer kısmı ise halojenden daha az elektronegatif radikal veya element olan ikili bileşik. Uygun koşullar altında alkali metalleri halojenler ile direkt birleşerek genel formülü MX(X = F, Cl, Br veya I) olan halojenürleri oluştururlar. Çoğu tuz halojenürdür. Oda sıcaklığında bütün alkali metalleri beyaz katı halinde halojenürler oluştururlar.
Lityum hidroksit  formülüne sahip inorganik alkali metal bileşiğidir. Lityum hidroksit kuvvetli bir baz olmasına rağmen alkali metal bazlarının en zayıf olanıdır.
formülüne sahip inorganik alkali metal bileşiğidir. Lityum hidroksit kuvvetli bir baz olmasına rağmen alkali metal bazlarının en zayıf olanıdır.

Buz çözme, yani diğer adıyla anti Icıng yüzeydeki kar, buz veya donu temizleme işlemidir. Buzlanmayı önleme, sadece buzdan arınmakla kalmayan, aynı zamanda yüzeyde kalan ve belirli bir süre boyunca buzun yeniden oluşmasını geciktiren veya mekanik olarak çıkarmayı kolaylaştırmak için buzun yüzeye yapışmasını önleyen kimyasal maddelerin uygulanmasıdır.

Sodyum kromat Na2CrO4 formülüne sahip bir inorganik bileşiktir. Tetra-, hekza- ve dekahidratlar oluşturabilen sarı higroskopik bir katı olarak bulunur. Cevherlerinden krom özütlemesinde bir ara maddedir.


















