Kimya, maddenin yapısını, özelliklerini, birleşimlerini, etkileşimlerini, tepkimelerini araştıran ve uygulayan bilim dalıdır. Kimya bilmi daha kapsamlı bir ifadeyle maddelerin özellikleriyle, sınıflandırılmasıyla, atomlarla, atom teorisiyle, kimyasal bileşiklerle, kimyasal tepkimelerle, maddenin hâlleriyle, moleküller arası ve moleküler kuvvetlerle, kimyasal bağlarla, tepkime kinetiğiyle, kimyasal dengenin prensipleriyle vb konularla ilgilenir. Kimyanın en önemli dalları arasında analitik kimya, anorganik kimya, organik kimya, fizikokimya ve biyokimya sayılır.

Fisyon, kütle numarası çok büyük bir atom çekirdeğinin parçalanarak kütle numarası küçük iki veya daha fazla çekirdeğe dönüşmesi olayıdır. Fisyon reaksiyonlarında radyoaktif elementler kullanılır ve tepkimeler için bir ilk enerjiye ihtiyaç vardır. Reaksiyon sonucunda kararsız çekirdekler ve nötron oluşur. Oluşan nötronların her biri yeni bir uranyum atomu ile tepkimeye girer. Bu esnada açığa çıkan nötronlar ortamdan uzaklaştırılmazsa tepkime zincirleme olarak devam eder.

Aldehitler, yapılarında karbonil grubuna bağlı bir hidrojenin olduğu organik bileşiklerdir. Düşük karbonlu aldehitler polar moleküller olup düşük ve yoğun fazlarda hidrojen bağı içermezler. Aynı karbon sayılı ketonlara göre kaynama noktası aldehitlerde daha yüksektir.

Benzen, aren veya aromatik hidrokarbonlar olarak adlandırılan organik bileşikler sınıfının en basit üyesidir. Renksiz, yanıcı, kaynama noktası 80,1 °C, erime noktası 5,5 °C olan bir sıvıdır. Moleküler formülü C6H6'dır. Benzen, endüstriyel bakımdan değerli olduğu gibi yapısı bakımından da kimya çalışmalarında önemlidir. Kan hücrelerini öldürme etkisi olduğundan kanser yapıcı bileşikler arasına girer.
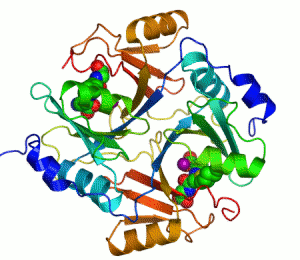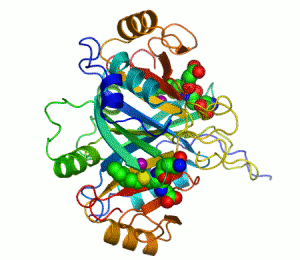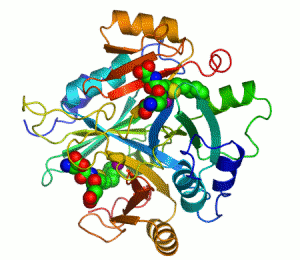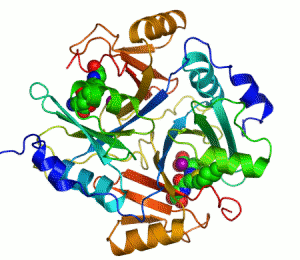
Enzimler, kataliz yapan biyomoleküllerdir. Neredeyse tüm enzimler protein yapılıdır. Enzim tepkimelerinde, bu sürece giren moleküllere substrat denir ve enzim bunları farklı moleküllere, ürünlere dönüştürür. Bir canlı hücredeki tepkimelerin neredeyse tamamı yeterince hızlı olabilmek için enzimlere gerek duyar. Enzimler substratları için son derece seçici oldukları için ve pek çok olası tepkimeden sadece birkaçını hızlandırdıklarından dolayı, bir hücredeki enzimlerin kümesi o hücrede hangi metabolik yolakların bulunduğunu belirler.
Kimyada bir dehidrasyon veya kondenzasyon tepkimesi, tepkiyen moleküllerden su kaybının meydana geldiği bir kimyasal tepkimedir. Dehidrasyon tepkimeleri eliminasyon tepkimelerinin bir alt grubudur. Hidroksil grubu (-OH) kolay ayrılan bir grup olmadığı için bir Bronsted asit katalizörü hidroksil grubunu protonlaştırıp daha kolay ayrılan bir -OH2+ grubu oluşturur. Selülozlar Bu gruba dahil değildirler.

Sülfürik(VI) asit ya da halk arasında bilinen ismi ile zaç yağı, H2SO4, güçlü bir mineral asididir. Olası kâşifi 8. yüzyıl simyacısı Cabir bin Hayyan tarafından yenime uğratıcı, renksiz ve yoğunluğu yüksek sıvı olarak tanımlanmıştır. Suda her konsantrasyonda çözünebilir. Büyük ölçüde korozif oluşu, güçlü asidik yapısından ve dehidrasyon özelliğinden kaynaklanmaktadır.
Yasa ya da diğer adıyla kanun anayasal hukuk sisteminde, yetkili organlarca meydana getirilen hukuk kurallarıdır. Yasalar, tüzükler, yönetmelikler birer hukuk kuralıdır. Yürürlükte olan hukuk kurallarının tümüne mevzuat denir. Dar anlamında yasa, yasama organınca yapılan yasa adıyla gerçekleştirilen işlerdir. Hukuk karşılıklı hakları ifade eden üst mefhumdur, yasa ise bu hakları koruyan ve belirleyen kuralları ifade eder.

Krebs döngüsü, trikarboksilik asit döngüsü veya sitrik asit döngüsü, canlı hücrelerin besinleri yükseltgeyerek enerji elde etmesini sağlayan ve bütün yaşam biçimlerinde önemli bir yer tutan kimyasal süreçlerin son aşamasıdır. TCA devri olarak da bilinir. 1937'de Hans Adolf Krebs tarafından açıklığa kavuşturulan tepkimelerin hayvan, bitki, mikroorganizma ve mantar gibi birçok hücre türünde oluştuğu saptanmıştır.
Kimyasal reaktiflik, bir reaksiyonun meydana gelme eğilimiyle ilişkilidir. Kimyasal tepkimelerin gerçekleşmesini belirleyen faktörler termodinamik düzeyinde incelenir. Termodinamik olarak bir reaksiyon eğer tepkimenin ürünleri reaktanlara kıyasla daha düşük serbest enerji düzeyinde ise gerçekleşir. Diğer taraftan Reaktiflik ise genel olarak bir maddenin kimyasal değişikliklere ya da kimyasal tepkimelere girme eğilimine denir. Elementlerin atomik yapısı ve elektronlarının dizilişi elementlerin ve oluşturdukları moleküllerin reaktifliğinde önemli rol oynar. Soygazların örneğin kimyasal olarak çok az reaktiflik gösterdiği belirtilir. Dolayısıyla kimyasal bileşik oluşturmaları zordur. Bu durum soygazların tam dolu olan en dış elektron kabuğundan dolayıdır.
Kimyasal denge, asit ve baz kimyası, elektron aktarımı tepkimesi ve entropi gibi konular kimyasal reaktifliğin temel kavramlarıdır.

Richard Fred Heck, Amerikan kimyacı. 2010 yılı Nobel Kimya Ödülünü Japon kimyacılar Ei-ichi Negishi ve Suzuki Akira ile paylaşmaya layık görülmüştür. Bu ödülü kazanmasında organik molekül oluşturulmasında paladyumu katalizör olarak kullandığı çalışmalarının etkisi olmuştur.

Gibbs serbest enerjisi entalpiden, entropi ve mutlak sıcaklığın çarpımının çıkarılmasıyla elde edilen termodinamik bir değişkendir. Genel olarak kimyasal bir reaksiyonun enerji potansiyelinin işe dönüştürülebilmesiyle ilgilidir.

Cyril Norman Hinshelwood, İngiliz kimyager, Nikolay Semyonov ile birlikte 1956 yılı Nobel Kimya Ödülü sahibi akademisyen. Özellikle kimyasal tepkime mekanizmaları üzerine çalışmalarıyla tanınmıştır. Hidrojen'in yanması, oksijen'in su oluşturması gibi zincir tepkimelerin tepkime hızı ve mekanizmaları üzerine araştırmalar yapmıştır. Son dönem araştırmaları daha sonra antibiyotik araştırmalarında kullanılacak bakteriyel hücre duvarlarında meydana gelen kimyasal değişiklikler üzerine olmuştur.

Tepkime hızı, bir kimyasal tepkimenin gerçekleşme hızıdır. Belirli zaman aralığında, ürünlerin derişimindeki artma veya reaktantların derişimindeki azalma ile saptanır. Örneğin bir demir parçasının havadaki oksijenin etkisiyle paslanması yıllar alırken, bir kâğıdın yanması saniyeler içinde olur.
Çarpışma kuramı, kimyasal tepkimeleri açıklamak için kullanılan kuramdır. 1916'da Max Trautz, 1918'de William Lewis, birbirlerinden bağımsız olarak bu kuramı ortaya koydular. Kuram, tepkimelerin molekül çarpışmalarına dayandığını ve tepkimelerin neden farklı hızda gerçekleştiğini açıklar.
Biyolojik Termodinamik, hücrelerin, yapıların, organizmaların arasında veya içinde gerçekleşen enerji dönüşümlerini ve bu dönüşümlerin temelini oluşturan kimyasal süreçlerin işleyişini inceleyen kantitatif (sayısal) bir daldır. Biyolojik Termodinamik herhangi belirli bir fenotipik nitelikle özdeşleşen kazancın gerekli olan enerjiyle değişimine değip değmeyeceği sorusunu sorabilir.

Baryum asetat (Ba(C2H3O2)2) baryum(II) ve asetik asitin tuzu.
Azerbaycan'da bankacılık sisteminin faaliyeti "Banklar Hakkında" yasasıyla düzenlenmiştir.
Reaksiyon kinetiği olarak da bilinen kimyasal kinetik, kimyasal reaksiyonların hızlarını ve mekanizmalarını araştırmakla ilgilenen bir fiziksel kimya dalıdır. Bir sürecin gerçekleştiği yön ile ilgilenen ancak gerçekleşme hızları hakkında bir bilgi vermeyen termodinamik ile karıştırılmamalıdır. Kimyasal kinetik, deneysel koşulların kimyasal reaksiyonların hızı üzerine etkilerini, reaksiyon mekanizmaları ile geçiş hâllerinin verim bilgilerini ve kimyasal reaksiyonların karakteristiklerini tanımlayan matematiksel modellerin çıkarılmasını kapsayan bir bilim alanıdır.
Kimyasal tepkimelerde giren ve ürünün derişimlerinin sabit olması durumuna kimyasal denge olarak adlandırılmaktadır.










