
Rubidyum, Rb sembolü ile gösterilen, 37 atom numarasına sahip alkali metaller grubundan bir kimyasal element. 1861 yılında Gustav Kirchhoff ve Robert Bunsen tarafından Almanya'da keşfedilmiştir. Kimyasal açıdan potasyum ve sezyumun özelliklerine benzer özellikler gösterir ama potasyuma oranla çok ender bulunur. Oda sıcaklığında gümüşi beyaz renkli, yumuşak ve parlak bir katıdır. Kuru havada bile çok çabuk yükseltgenir, bu yüzden açık havada saklanamaz. Suyu şiddetle ayrıştırır ve ortaya çıkan hidrojeni tutuşturur.

Sodyum, periyodik cetvelde Na simgesi ile gösterilen ve atom numarası 11 olan element. Sodyum yumuşak ve kaygan bir metal olup alkali metaller grubuna aittir. Doğal bileşiklerin içinde bol miktarda bulunur. Yüksek oranda reaktiftir, sarı bir alevle yanar, su ile şiddetli reaksiyon verir ve havada hızla oksitlenir. Dolayısıyla, vazelin, gazyağı gibi hava ve su ile temasını kesecek bir ortamda saklanması gerekir.

Potasyum, bir kimyasal elementtir. Simgesi K ve atom numarası 19 dur. Potasyum adını izole edildiği Potas olarak da bilinen potasyum karbonattan almıştır. Potasyum yumuşak, gümüş-beyaz renkli alkali bir metaldir. Doğada deniz suyunda ve pek çok mineralde diğer elementlere bağlı olarak bulunur. Havada hızla oksitlenir ve suya karşı da çok aktiftir. Potasyum, pek çok açıdan sodyuma kimyasal olarak benzese de yaşayan organizmalarda, özellikle de hayvan hücrelerinde, sodyumdan farklı muamele görür. Kandaki seviyesinin düşük olmasına hipokalemi, yüksek olmasına hiperkalemi denir.

Gümüş, elementlerin periyodik tablosunda simgesi Ag olan, beyaz, parlak, değerli bir metalik element. Atom numarası 47, atom ağırlığı 107,87 gramdır. Erime noktası 961,9 °C, kaynama noktası 1950 °C ve özgül ağırlığı da 10,5 g/cm³'tür. Çoğu bileşiklerinde +1 değerliklidir. Günümüzde Dünya'da 55 yıllık gümüş rezervi kaldığı tahmin ediliyor. Yeni gümüş rezervleri keşfedilmezse 2078 yılında Dünya'daki gümüş rezervlerinin tükenebileceği tahmin ediliyor. En çok gümüş üretimi yapan ülkeler Meksika, Çin, Peru Şili ve Avustralya'dır.

Brom (Br), Antoine Balard tarafından 1826 yılında keşfedilen halojen ametal. Yunanca dışkı gibi koku anlamındaki bromosdan gelmiştir.

Klor, VIIA grubunda bulunan hafif, keskin kokulu, yeşilimsi sarı renkli, tahriş edici ve zehirleyici bir gaz. Havadan 2,5 kat ağır olan klor ilk zamanlar bir bileşik olarak kabul ediliyordu. Klor ilk olarak 1774 yılında Carl Wilhelm Scheele tarafından keşfedildi. 1810 yılında ise bugünkü ismi Humphry Davy tarafından verildi.

Tuz, kimyada, bir asitle bir bazın tepkimeye girmesi neticesinde meydana gelen maddedir. Tuz, asitteki eksi yüklü iyonla (anyon) bazdaki artı yüklü iyondan (katyon) meydana gelir. Asitle baz arasındaki nötralleşme tepkimesi esnasında tuz ve su açığa çıkar. Erimiş tuz veya çözelti halindeki tuzların çoğu eksi ile artı yüklü iyonlarına ayrışır ve elektriği iletir. Tuz adı ayrıca sofra tuzu veya sodyum klorür (NaCl) için de kullanılır.

Sezyum, atom numarası 55 olan, alkali metaller grubuna ait bir kimyasal element. Element oda sıcaklığında katı olsa da 28 °C'de erimektedir. Sezyuma doğada ender rastlanır. Gümüşümsü altın renklidir ve metalik yapıdadır. Element, Robert Wilhelm Bunsen ve Gustav Kirchoff tarafından 1860 yılında mineral suyunda keşfedildi.
Bilinen inorganik ve organometalik bileşiklerin elementlere göre sıralanmış listesidir. Sıralama elementlerin kısaltmalarının alfabetik sırasına göredir.
Haloalkanlar, bir ya da daha fazla halojen içeren alkanlardan türetilen bir kimyasal bileşikler grubudur. Ayrım genellikle yapılmamasına rağmen, halokarbonlar genel sınıfın bir alt kümesi olarak kabul edilirler. Haloalkanlar yaygın şekilde ticari olarak kullanılmaktadır ve birçok kimyasal ve ticari isim altında bilinmektedirler. Bunlar; alev geciktiriciler, yangın söndürücüler, soğutucular, iticiler, çözücüler ve farmasötik maddeler olarak kullanılmaktadır. Ticari olarak yaygın kullanımı nedeniyle, birçok halokarbonların aynı zamanda ciddi kirleticiler ve toksinler olduğu gösterilmiştir. Örneğin, kloroflorokarbonların ozon tabakasının incelmesine yol açtığı gösterilmiştir. Metil bromür tartışmalı fümiganttır. Sadece klor, brom ve iyot içeren haloalkanlar ozon tabakasına tehdit oluşturmaktadır. Florlu uçucu haloalkanlar ise teoride sera gazları aktivitesine sahiptir. Metil iyodür, doğal olarak oluşan bir maddedir ve ozon tabakasına zarar verici özellikleri yoktur. Bu nedenle Amerika Birleşik Devletleri Çevre Koruma Ajansı tarafından ozon tabakasına zarar verici gaz olmadığı bildirilmiştir. Haloalkan veya alkil halojenürler " RX" genel formülü ile gösterilirler. Burada R; bir alkil ya da yer değiştirmiş bir alkil grubudur ve X; bir halojendir.

Gümüş halid bir halojen ve gümüş elementi arasında oluşabilecek bileşiklerden biri. Özellikle, brom, klor, iyot ve flordan her biri sırasıyla gümüş bromür (AgBr), gümüş klorür (AgCl), gümüş iyodür (AgI) ve gümüş florürün her 3 formunu da oluşturmak için gümüş ile tepkime verebilir.
Gümüş bromür (AgBr), yumuşak, soluk sarı, suda çözünmeyen bu tuz diğer gümüş halideler içinde geçerli olan ışığa duyarılık özelliği ile bilinir. Bu özellik gümüş halidlerin modern fotoğrafik malzemelerin temelini oluşturmalarına sebebiyet vermiştir. AgBr fotoğraf filmelerinde sıkça kullanılır ve bazılarınca Torino Kefeni yapımında kullanılmıştır. Bu tuz doğal olarak bromaritit minerali hâlinde bulunabilir.

Gümüş klorür AgCl formüllü bileşik. Bu beyaz kristal katı sudaki düşük çözünürlüğü ile bilinir. Bu özelliği Tl+ ve Pb2+ klorürlerinin özelliklerini anımsatır. Aydınlanma veya ısıtma ile gümüş klorür, bazı numunelerde girimsi veya morumsu renklenme ile varlığı anlaşılan, gümüş ve klora dönüşür. AgCl doğal olarak kloraririt minerali halinde bulunur.

Sodyum bromür, NaBr formülüne sahip inorganik bir bileşiktir. Yüksek erime noktasına sahip beyaz kristal yapısıyla sofra tuzuna benzemektedir. Genellikle bromür iyonu kaynağı olarak çeşitli alanlarda kullanılmaktadır.

Kalay(II) klorür ya da stanit klorür, SnCl2 formülüne sahip, beyaz kristal halinde bir katıdır. Kararlı bir dihidrat oluşturur, ancak sulu çözeltileri, özellikle sıcaksa, hidrolize uğrama eğilimindedir. SnCl2 yaygın bir şekilde indirgeyici madde (bir asit çözeltisi içinde) olarak ve kalay kaplamada elektrolitik banyolarda kullanılır. Kalay (II) klorür, diğer kalay klorür (kalay(IV) klorür (SnCl4) ile karıştırılmamalıdır.

İyodik asit, HIO3, beyaz veya kirli beyaz bir katı madde olarak elde edilebilir. Suda çok iyi çözünür, ancak klorik asit veya bromik asidin aksine saf halde bulunur. İyodik asit +5 oksidasyon durumunda iyot içerir ve halojenlerin saf halde en stabil okso-asitlerinden biridir. İyot asidi dikkatle ısıtıldığında pentoksit iyice dehidre olur. Daha sonraki ısıtmada, iyot pentoksit ayrıca iyot, oksijen ve düşük iyot oksitleri karışımı vererek ayrışır.

Bir Grignard reaktifi veya Grignard bileşiği, X'in bir halojen ve R'nin normalde bir alkil veya aril olduğu organik bir grup olduğu genel formül R−Mg−X'e sahip kimyasal bir bileşiktir. İki tipik örnek, metilmagnezyum klorür Cl−Mg−CH
3 ve fenilmagnezyum bromür (C
6H
5)−Mg−Br'dir. Organomagnezyum bileşiklerinin bir alt sınıfıdır.
Demir (III) klorür FeCl
3 formüllü inorganik bir bileşiktir. Kristal bir katı olmasının yanı sıra görüş açısına bağlı olarak farklı renklerle gözlemlenebilir; koyu yeşil, mor-kırmızı. Sulu formu da katı formu da fiziksel görünüm olarak koyu kahverengi rengindedir.

Baryum klorür, BaCl2 formüllü inorganik bir bileşik'tir. Bu bileşik baryum'un suda-çözünen en yaygın tuzlarından biridir. Diğer baryum tuzlarının çoğu gibi, baryum klorür beyaz toz halinde ve zehirlidir. Alevde sarı-yeşil renk verir. Ayrıca higroskopiktir, ilk önce dihidrat BaCl2(H2O)2' ye dönüşür.
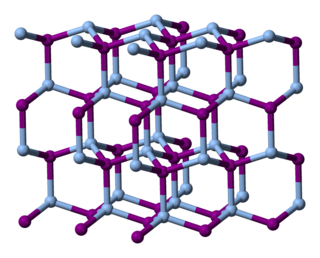
Gümüş iyodür, AgI formülüne sahip bir inorganik bileşiktir. Bileşik parlak sarı bir katıdır, ancak numuneler neredeyse her zaman gri bir renk veren metalik gümüş safsızlıkları içerir. Gümüş bulaşması, AgI'nin yüksek düzeyde ışığa duyarlı olması nedeniyle ortaya çıkar. Bu özellik gümüş esaslı fotoğrafçılık'ta kullanılır. Gümüş iyodür ayrıca antiseptik olarak ve bulut tohumlama için de kullanılır.















