
İdeal gaz yasası, sadece teoride olan ideal gazların durumları hakkında denklemler sağlayan bir yasadır. Bir miktar gazın durumu; basıncı, hacmi ve sıcaklığına göre belli olur. Bu denklem aşağıdaki gibidir:

- P paskal olarak basınç,
- V kübik metre olarak hacim,
- n gazın mol sayısı,
- R gaz sabiti
- T Kelvin olarak sıcaklık

Termodinamik çevrim, bir veya daha çok hal değişimi gerçekleştiren, iş veya enerji üreterek veya enerjiyi transfer ederek ilk haline dönen bir çalışma akışkanı içeren çevrimlerdir. Tabloda termodinamik çevrimlerin listesi verilmiştir.
Benzinli motorda, yanma sabit hacimde gerçekleşir, dizel motorda ise yanma sabit basınçta gerçekleşir. Karma çevrimde ise günümüz modern dizel motorlarında olduğu gibi, yanmanın ilk aşaması sabit hacime yakın, son aşaması ise sabit basınca yakın gerçekleşmektedir. Bu yüzden ısının bir miktarının sabit hacimde, geri kalan kısmının da sabit basınçta sisteme verildiği bu çevrime karma çevrim denir.

Fizik, fiziksel kimya ve mühendislikte akışkanlar dinamiği, akışkanların akışını tanımlayan akışkanlar mekaniğinin bir alt disiplinidir. Aerodinamik ve hidrodinamik dahil olmak üzere çeşitli alt disiplinleri vardır. Akışkanlar dinamiğinin, uçaklardaki kuvvetlerin ve momentlerin hesaplanması, boru hatları boyunca petrolün Kütle akış hızının belirlenmesi, hava durumu modellerinin tahmin edilmesi, uzaydaki bulutsuların anlaşılması ve fisyon silahı patlamasının modellenmesi dahil olmak üzere geniş bir uygulama yelpazesi vardır.

Navier-Stokes denklemleri, ismini Claude-Louis Navier ve George Gabriel Stokes'tan almış olan, sıvılar ve gazlar gibi akışkanların hareketini tanımlamaya yarayan bir dizi denklemden oluşmaktadır.

Genleşme, sıcaklığı artırılan bir cismin uzunluk ya da hacminin değişmesi olayıdır.
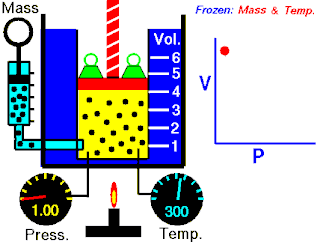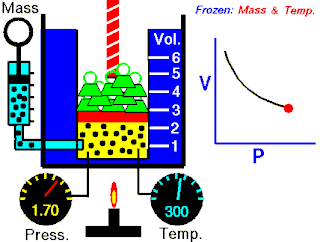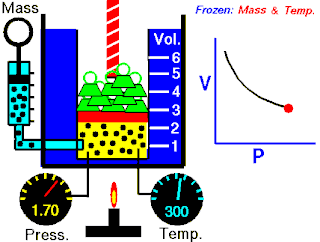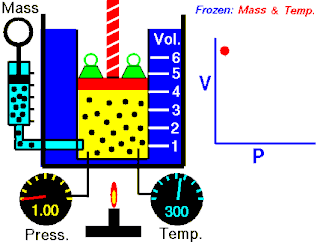
Boyle yasası, gaz yasalarından biridir. 1662'de İrlandalı doğa filozofu Robert Boyle tarafından ilk defa basılmıştır. Yasa, Richard Towneley ve Henry Power tarafından Boyle'ın önüne getirilmiş ve Boyle da deneyleri yapıp sonuçları basmıştır. Robert Gunther ve bazı diğer otoritelere göre, deneyin aparatını hazırlayan Boyle'ın asistanı Robert Hooke, yasayı formülize eden insan olabilir. Hooke'un matematik konusundaki becerileri Boyle'ı aşıyordu. Hooke ayrıca, deneyler için gerekli olan vakum pompalarını da icat etmiştir. Fransız fizikçi Edme Mariotte (1620-1684), Boyle'dan bağımsız olarak formülü 1676'da bulmuştur. Bu nedenle de bu yasa, Mariotte ya da Mariotte-Boyle yasası olarak da isimlendirilebilir.
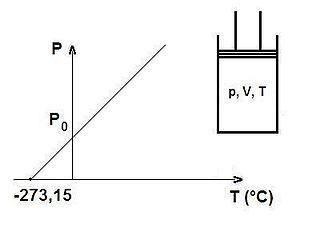
Charles yasası, gaz yasalarından biridir. Bu yasaya göre, sabit basınçta, herhangi bir miktardaki ideal gazın hacminin azalıp çoğalması, aynı oranda sıcaklığının da azalıp çoğalmasını etkiler.

Gay-Lussac yasası, Fransız kimyacı Joseph Louis Gay-Lussac'ın adıyla anılır. Gay-Lussac'a mal edilen, iki tane gaz yasası vardır. İkisi de aynı isimle anılırlar. En ünlü deneyi gazlarla yaptığı sıcaklık değişiminin inciler üzerindeki basınç değişimini dedesi Mark Lussac ile yapmıştır.
Avogadro yasası ya da Avogadro hipotezi, Amedeo Avogadro'nun 1811'de bulduğu bir gaz yasasıdır. Bu yasa, eşit hacimdeki gazların; eşit sıcaklık ve eşit basınçta aynı sayıda parçacık ya da molekül sayısına sahip olduğunu öne sürer. Buna göre, belirli bir hacimdeki gazın bulundurduğu molekül sayısı, gazın kütle ya da boyutundan bağımsızdır. Örnek olarak, aynı hacimdeki hidrojen ve nitrojen verilebilir. Buna göre, hidrojen de nitrojen de, aynı hacim, aynı basınç ve aynı sıcaklıkta aynı molekül sayısına sahiptir.
Bir ideal gaz karışımında hacmi olan her gazın kendine ait bir kısmi basıncı vardır.
Kinetik teori veya gazların kinetik teorisi, gazların basınç, sıcaklık, hacim gibi makroskobik özelliklerini moleküler bileşim ve hareketlerine bağlı olarak açıklayan teoridir. Esas olarak, teori Isaac Newton'un kanısının tersine basıncın moleküller arası statik itmeden kaynaklanmadığını, bunun yerine belli hızlarda hareket eden moleküller arası çarpışmalardan kaynaklandığını söyler. Kinetik teori aynı zamanda kinetik-moleküler teori veya çarpışma teorisi olarak da bilinir.
Graham difüzyon yasası, İskoç fiziksel kimyacı Thomas Graham tarafından bulunan gazların difüzyon hareketini açıklayan yasadır.

Amagat yasası ya da kısmi hacimler yasası, ideal gazların karışımını açıklayan gaz yasalarından biridir. Bu yasaya göre; bir gaz karışımının hacmi, karışımı oluşturan gazların aynı koşullarda ayrı ayrı kaplayacakları hacimlerin toplamına eşittir.

Joule genişlemesi termodinamikte (ısıdevinimsel) geri dönülmez (tersinemez) bir süreçtir. Burada ısısal olarak yalıtılmış bölmeli kabın bir tarafına belli bir hacimde gaz konur, kalan diğer tarafı ise boşaltılmıştır. Kabın ortasındaki engel kaldırılır ve bir taraftaki gaz tüm kaba yayılır.

Termodinamik'in üçüncü yasası bazen ‘mutlak sıfır sıcaklığında dengede olan sistemlerin özelliklerine ilişkin’ olarak şu şekilde tanımlanır:
Fizikte, foton gazı, fotonların gaz benzeri birikmesidir ki hidrojen ve neon gibi sıradan gazlarla basınç, sıcaklık, entropi gibi benzer özelliklere sahiptir. Foton gazının dengedeki en yaygın örneği siyah cisim ışımasıdır.

İki izobarik yüzey arasındaki kalınlık, h tabakasının ortalama sanal sıcaklığına ilişkin bir denklemi verir.
Termodinamikte izovolümetrik süreç veya izometrik süreç olarak da adlandırılan izokorik süreç kapalı sistem hacminin sabit kalması demektir. İzokorik bir süreç, kapalı, elastik olmayan bir kabın içeriğinin ısıtılması veya soğutulması ile örneklendirilebilir. Kapalı sistem kabın içeriğinin dışarıya karşı izole olmasıdır. Kap deforme olmaz ve hacmi termodinamik süreç boyunca sabit kalırsa bu bir izokorik süreç örneğidir.


































