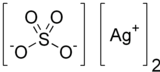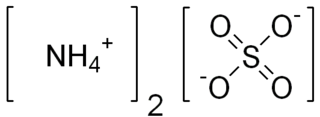Gümüş, elementlerin periyodik tablosunda simgesi Ag olan, beyaz, parlak, değerli bir metalik element. Atom numarası 47, atom ağırlığı 107,87 gramdır. Erime noktası 961,9 °C, kaynama noktası 1950 °C ve özgül ağırlığı da 10,5 g/cm³'tür. Çoğu bileşiklerinde +1 değerliklidir. Günümüzde Dünya'da 55 yıllık gümüş rezervi kaldığı tahmin ediliyor. Yeni gümüş rezervleri keşfedilmezse 2078 yılında Dünya'daki gümüş rezervlerinin tükenebileceği tahmin ediliyor. En çok gümüş üretimi yapan ülkeler Meksika, Çin, Peru Şili ve Avustralya'dır.

Kral suyu, asitlerin az etki ettiği ya da etki etmediği altın ve platin gibi metallerle tepkimeye girebilen kuvvetli bir asit çözeltisidir. Hidroklorik asit ve nitrik asitin 3:1 oranında karıştırılmasıyla oluşur. Ebu Musa Câbir bin Hayyan tarafından bulunduğu tahmin edilmektedir.
İnorganik kimya veya anorganik kimya; organik olmayan, yani karbon-hidrojen bağı içermeyen bileşiklerin özelliklerini ve kimyasal davranışlarını inceleyen kimya dalı. Anorganik ve organik kimyayı birleştiren organometalik bileşikler, organometalik kimya adında başka bir dalı oluşturur.
Elektrokimya, kimya biliminin bir alt dalı olup elektronik bir iletken ile iyonik bir iletken (elektrolit) arayüzeyinde gerçekleşen reaksiyonları inceler. Elektrokimyada amaç kimyasal enerji ve elektrik enerjisi arasındaki değişimi incelemektir.

Sülfürik(VI) asit ya da halk arasında bilinen ismi ile zaç yağı, H2SO4, güçlü bir mineral asididir. Olası kâşifi 8. yüzyıl simyacısı Cabir bin Hayyan tarafından yenime uğratıcı, renksiz ve yoğunluğu yüksek sıvı olarak tanımlanmıştır. Suda her konsantrasyonda çözünebilir. Büyük ölçüde korozif oluşu, güçlü asidik yapısından ve dehidrasyon özelliğinden kaynaklanmaktadır.
Nitrik asit, HNO3 kimyasal formülüne sahip oldukça aşındırıcı bir inorganik asittir. Kezzap olarak da bilinir. Saf hâldeki bileşik renksizdir. Ancak uzun süre bekleyen eski asitler azot oksitleri ve suya ayrışması nedeniyle sarı renge dönebilme özelliğindedirler. Piyasada bulunan nitrik asitlerin çoğu % 68'lik bir konsantrasyona sahiptir. Çözelti, %86'dan fazla HNO3 içerdiğinde, dumanlı nitrik asit olarak adlandırılır. Mevcut azot dioksit miktarına bağlı olarak, dumanlı nitrik asit ayrıca %86’nın üzerindeki konsantrasyonlarda kırmızı dumanlı nitrik asit veya %95’in üzerindeki konsantrasyonlarda beyaz dumanlı nitrik asit olarak tanımlanır.

Küprik sülfat ya da sadece bakır sülfat olarak da bilinen Bakır (II) sülfat, kimyasal formülü CuSO4 olan bir kimyasal bileşiktir. Bu tuzun hidrasyon derecelerine bağlı olarak bir dizi farklı bileşikleri mevcuttur. Susuz formu soluk yeşil ya da grimsi beyaz bir toz olmasına karşın en çok bilinen pentahidrat (CuSO4•5H2O) formu, parlak mavi renktedir. Çok az miktardaki CuSO4•5H2O çevreye çok zehirlidir, gözleri ve cildi tahriş eder ve yutulduğunda zararlı da olabilir. Oktahedral moleküler geometriye ve paramanyetik özelliğe sahip olan bakır (II) sülfat ekzotermik olarak suda çözünürek [Cu(H2O)6]2+ kompleksini oluşturur. Bakır (II) sülfat "mavi vitriyol", "göztaşı" ve "göktaşı" olarak da bilinmektedir.

Kükürtlü asit, sülfüröz asit ya da sülfürik(IV) asit formüllü H2SO3 olan bir kimyasal bileşiktir.
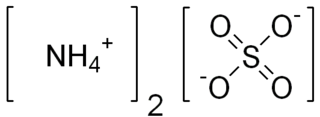
Amonyum sülfat, (NH4)2SO4 formülüne ve çok sayıda ticari kullanıma sahip bir inorganik tuzdur. Toprak gübresi olarak yaygın bir şekilde kullanılır. %21 azot ve %24 kükürt içerir.

Her yıl düzenlenen Grammy Ödülleri'nin En İyi Erkek Pop Vokal Performansı kategorisindeki ödülü 1966'dan 2011'e kadar verilmekteydi. 2012 yılında bu kategori kaldırılarak yerine En İyi Solo Pop Performansı ödülü verilmeye başlandı.

Sodyum bisülfat, diğer bir adı sodyum hidrojen sülfat (NaHSO4) olan bu kimyasal madde asit tuz karakterlidir. Kuru halde iken güvenli bir şekilde nakledilebilir ve depolanabilir. Susuz formu higroskopiktir. Sodyum bisülfat suda hidroliz olarak asidik çözelti verir. 1 Molarlık çözeltisinin pH değeri 1 den küçüktür. Sodyum bisülfat yavaşça ısıtılırsa suyunu kaybederek sodyum pirosülfata dönüşür.
- 2NaHSO4 → Na2S2O7 + H2O

Potasyum sülfat, formülü K2SO4 olan, yanmaz, suda çözünebilen beyaz kristal yapıda bir potasyum tuzudur. Genellikle potasyum ve kükürt kaynağı olarak gübrelerde kullanılır.
Kimyasal reaktiflik, bir reaksiyonun meydana gelme eğilimiyle ilişkilidir. Kimyasal tepkimelerin gerçekleşmesini belirleyen faktörler termodinamik düzeyinde incelenir. Termodinamik olarak bir reaksiyon eğer tepkimenin ürünleri reaktanlara kıyasla daha düşük serbest enerji düzeyinde ise gerçekleşir. Diğer taraftan Reaktiflik ise genel olarak bir maddenin kimyasal değişikliklere ya da kimyasal tepkimelere girme eğilimine denir. Elementlerin atomik yapısı ve elektronlarının dizilişi elementlerin ve oluşturdukları moleküllerin reaktifliğinde önemli rol oynar. Soygazların örneğin kimyasal olarak çok az reaktiflik gösterdiği belirtilir. Dolayısıyla kimyasal bileşik oluşturmaları zordur. Bu durum soygazların tam dolu olan en dış elektron kabuğundan dolayıdır.
Kimyasal denge, asit ve baz kimyası, elektron aktarımı tepkimesi ve entropi gibi konular kimyasal reaktifliğin temel kavramlarıdır.
Gümüş bromür (AgBr), yumuşak, soluk sarı, suda çözünmeyen bu tuz diğer gümüş halideler içinde geçerli olan ışığa duyarılık özelliği ile bilinir. Bu özellik gümüş halidlerin modern fotoğrafik malzemelerin temelini oluşturmalarına sebebiyet vermiştir. AgBr fotoğraf filmelerinde sıkça kullanılır ve bazılarınca Torino Kefeni yapımında kullanılmıştır. Bu tuz doğal olarak bromaritit minerali hâlinde bulunabilir.

Kalay(II) klorür ya da stanit klorür, SnCl2 formülüne sahip, beyaz kristal halinde bir katıdır. Kararlı bir dihidrat oluşturur, ancak sulu çözeltileri, özellikle sıcaksa, hidrolize uğrama eğilimindedir. SnCl2 yaygın bir şekilde indirgeyici madde (bir asit çözeltisi içinde) olarak ve kalay kaplamada elektrolitik banyolarda kullanılır. Kalay (II) klorür, diğer kalay klorür (kalay(IV) klorür (SnCl4) ile karıştırılmamalıdır.

Hidrojen iyodür (HI) iki atomlu bir molekül ve hidrojen halojenürdür. Sulu çözeltisi, güçlü bir asit olan hidroiyodik asit veya hidriyodik asit olarak bilinir. Bununla birlikte, hidrojen iyodür ve hidroiodik asit, birincisinin standart koşullar altında bir gaz olması, diğerinin ise söz konusu gazın sulu bir çözeltisi olması bakımından farklıdır. Birbirine dönüştürülebilir. HI, organik ve inorganik sentezlerde birincil iyot kaynaklarından biri ve bir indirgeyici madde olarak kullanılır.
Permanganik asit, HMnO4 formülüne sahip bir inorganik bileşiktir. Bu güçlü oksoasit, dihidrat olarak izole edilmiştir. Permanganat tuzlarının konjugat asididir. Çok az sayıda yayın konusu olup, karakterizasyonu ve kullanımları çok sınırlıdır.

Bromöz asit, HBrO2 formülüne sahip bir inorganik bileşiktir. Konjugat bazının -bromitlerinin- tuzları izole edilmiş olmasına rağmen, kararsız bir bileşiktir. Asidik çözeltide, bromitler broma ayrışır.

Nikel sülfat NiSO
4 formülüne sahip bir metal bileşiğidir. Nikel sülfat hidratsız formu oda sıcaklığında sarımsı bir renge sahipken hekzahidrat ve heptahidrat hâli mavi bir renge sahiptir, bakır sülfat rengini andırır. Suda çok iyi çözünür.
Bu, çok sayıda saygın video oyunu gazetecisinin veya dergisinin tüm zamanların en iyileri arasında saydığı video oyunlarının bir listesidir. Burada listelenen oyunlar, editör kadroları tarafından seçilen, farklı yayınlardan en az altı ayrı "tüm zamanların en iyi/en büyük" listesine dahil edilmiştir.