Formik asit
| |||
 | |||
| Adlandırmalar | |||
|---|---|---|---|
Tercih edilen IUPAC adı Formik asit[1] | |||
Sistematik IUPAC adı Methanoic acid[1] | |||
Diğer adlar İzokarbonöz asit Karbonöz asit Formilik asit Metilik asit Hidrojenkarboksilik asit Hidroksi(okso)metan Metakarbonoik asit Oksokarbinik asit Oksometanol Hidroksimetilen oksit karınca asidi | |||
| Tanımlayıcılar | |||
CAS numarası | |||
3D model (JSmol) | |||
| 1209246 | |||
| ChEBI | |||
| ChEMBL | |||
| ChemSpider | |||
| DrugBank | |||
| ECHA InfoCard | 100.000.527 | ||
| EC Numarası |
| ||
| E numaraları | E236 (koruyucular) | ||
| 1008 | |||
| KEGG | |||
PubChem CID | |||
| RTECS numarası |
| ||
| UNII | |||
CompTox Bilgi Panosu (EPA) | |||
| |||
| |||
| Özellikler | |||
| Kimyasal formül | CH2O2 | ||
| Molekül kütlesi | 46,03 g mol−1 | ||
| Görünüm | dumanlı renksiz sıvı | ||
| Koku | keskin | ||
| Yoğunluk | 1,220 g/mL | ||
| Erime noktası | 8,4 °C (47,1 °F; 281,5 K) | ||
| Kaynama noktası | 100,8 °C (213,4 °F; 373,9 K) | ||
| Çözünürlük (su içinde) | karışır | ||
| Çözünürlük | eter, aseton, etil asetat, gliserol, metanol ve etanol içinde karışır benzen, toluen ve ksilenler içinde az çözünür | ||
| log P | −0.54 | ||
| Buhar basıncı | 35 mmHg (20 °C)[2] | ||
| Asitlik (pKa) | 3.745[3] | ||
| Konjuge baz | Formate | ||
| -19,90×10-6 cm3/mol | |||
| Kırınım dizimi (nD) | 1.3714 (20 °C) | ||
| Akmazlık | 1.57 cP (268 °C) | ||
| Yapı | |||
| Planar | |||
| Dipol momenti | 1.41 D (gaz) | ||
| Termokimya | |||
Standart molar entropi (S⦵298) | 131.8 J/mol K | ||
Standart formasyon entalpisi (ΔfH⦵298) | −425.0 kJ/mol | ||
Standart yanma entalpisi (ΔcH⦵298) | −254.6 kJ/mol | ||
| Farmakoloji | |||
| QP53AG01 (DSÖ) | |||
| Tehlikeler | |||
| İş sağlığı ve güvenliği (OHS/OSH): | |||
| Ana tehlikeler | tahriş edici, korozif | ||
| GHS etiketleme sistemi: | |||
| Piktogramlar |  | ||
| İşaret sözcüğü | Danger | ||
| Tehlike ifadeleri | H314 | ||
| Önlem ifadeleri | P260, P264, P280, P301+P330+P331, P303+P361+P353, P304+P340, P305+P351+P338, P310, P321, P363, P405, P501 | ||
| NFPA 704 (yangın karosu) | |||
| Parlama noktası | 69 °C (156 °F; 342 K) | ||
Kendiliğinden tutuşma sıcaklığı | 601 °C (1.114 °F; 874 K) | ||
| Patlama sınırları | 14 –34%[] 18 –57% (90% solution)[2] | ||
| Öldürücü doz veya konsantrasyon (LD, LC): | |||
LD50 (medyan doz) | 700 mg/kg (fare, oral), 1100 mg/kg (sıçan, oral), 4000 mg/kg (köpek, oral)[4] | ||
LC50 (medyan konsantrasyon) | 7853 ppm (rat, 15 min) 3246 ppm (mouse, 15 min)[4] | ||
| NIOSH ABD maruz kalma limitleri: | |||
| PEL (izin verilen) | TWA 5 ppm (9 mg/m3)[2] | ||
| REL (tavsiye edilen) | TWA 5 ppm (9 mg/m3)[2] | ||
| IDLH (anında tehlike) | 30 ppm[2] | ||
| Güvenlik bilgi formu (SDS) | MSDS from JT Baker | ||
| Benzeyen bileşikler | |||
Benzeyen karboksilik asitler | Asetik asit Propiyonik asit | ||
Benzeyen bileşikler | Formaldehit Metanol | ||
| Aksi belirtilmediği sürece madde verileri, Standart sıcaklık ve basınç koşullarında belirtilir (25 °C [77 °F], 100 kPa). | |||
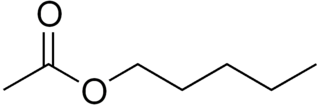
Formik asit, HCOOH, tek karbonlu karboksilik asittir. Metanoik asit olarak da bilinir. Formik asit, karbonil karbonuna bağlı alkil grubu içermemesiyle en basit karboksilli asit özelliği taşır. Hem aldehit hem de karboksilik asit özelliğine sahiptir.
Formik asit; su, metanol, etanol, aseton, eter gibi çözücülerde çok iyi çözünür.
Formik asitin diğer bir adı da karınca asididir. Doğada ilk olarak karıncaların salgılarında rastlanmış ve buradan çekilerek elde edilmiştir. Endüstriyel olarak formik asit metanol ve karbonmonoksitin tepkimesinden oluşan metil formatın sodyum metoksit eşliğinde su ile tepkimeye girmesiyle elde edilir.
Doğada formik asit
Doğada birçok karıncada savunma mekanizması olarak formik asit bulunur. Isırgan otunda temas edince deriyi yakan kimyasal formik asittir.
Güvenlik
%85'lik derişime sahip formik asit yanıcıdır. Formik asit düşük toksisiteye sahiptir. Konsantre formik asit cildi yakabilir. Formik asit, metil alkol zehirlenmelerinde formaldehit ile birlikte metanolün metabolitidir. Optik sinirleri hasarlayan şey formik asittir.
Kullanım alanları
Formik asitin en büyük kullanım alanı koruyucu ve antibakteriyel ajan olaraktır. Tekstilde kullanılır. Dericilikte koyulaştırma amacı ile de kullanılır.
Kaynakça
- ^ a b Favre, Henri A.; Powell, Warren H. (2014). Nomenclature of Organic Chemistry : IUPAC Recommendations and Preferred Names 2013 (Blue Book). Cambridge: The Royal Society of Chemistry. s. 745. doi:10.1039/9781849733069. ISBN 978-0-85404-182-4.
- ^ a b c d e NIOSH Pocket Guide to Chemical Hazards. "#0296". National Institute for Occupational Safety and Health (NIOSH).
- ^ Smith, Robert M.; Martell, Arthur E. (1989). Critical Stability Constants Volume 6: Second Supplement. New York: Plenum Press. s. 299. ISBN 0-306-43104-1.
- ^ a b "Formic acid". Immediately Dangerous to Life or Health Concentrations (IDLH). National Institute for Occupational Safety and Health. 4 Aralık 2014. 19 Mart 2015 tarihinde kaynağından arşivlendi. Erişim tarihi: 26 Mart 2015.