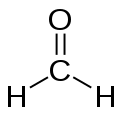
Formaldehit
 | |
 | |
 | |
| Adlandırmalar | |
|---|---|
Methanal | |
Sistematik IUPAC adı Metanal | |
Diğer adlar | |
| Tanımlayıcılar | |
CAS numarası | |
3D model (JSmol) | |
| 3DMet | |
| 1209228 | |
| ChEBI | |
| ChEMBL | |
| ChemSpider | |
| DrugBank | |
| ECHA InfoCard | 100.000.002 |
| EC Numarası |
|
| E numaraları | E240 (koruyucular) |
| 445 | |
| KEGG | |
| MeSH | Formaldehyde |
PubChem CID | |
| RTECS numarası |
|
| UNII | |
| UN numarası | 2209 |
CompTox Bilgi Panosu (EPA) | |
| |
| |
| Özellikler | |
| Görünüm | Renksiz gaz |
| Yoğunluk | 0.8153 g/cm³ (−20 °C)[1] |
| Erime noktası | -92 °C |
| Kaynama noktası | -19 °C [1] |
| Çözünürlük (su içinde) | 400 g dm−3 |
| log P | 0.350 |
| Asitlik (pKa) | 13.3 |
| Baziklik (pKb) | 0.7 |
| Yapı | |
| Trigonal planar | |
| Tehlikeler | |
| NFPA 704 (yangın karosu) | |
| Parlama noktası | 64 °C (147 °F) |
| Patlama sınırları | 7–73% |
| Öldürücü doz veya konsantrasyon (LD, LC): | |
LD50 (medyan doz) | 100 mg/kg (oral, rat) |
| Benzeyen bileşikler | |
Benzeyen | Asetaldehit Propiyonaldehit Bütiraldehit |
Benzeyen bileşikler | metanol formik asit |
| Aksi belirtilmediği sürece madde verileri, Standart sıcaklık ve basınç koşullarında belirtilir (25 °C [77 °F], 100 kPa). | |
Formaldehit CH2O formülüne sahip bir organik bileşiktir. Aldehitlerin en basit üyesidir, diğer ismi Metanaldir. Karbonil grubunun boş olan iki bağına birer hidrojen bağlanmasıyla oluşur. Tüm gelişmiş canlılarda doğal olarak üretilir. Zehirli bir gazdır. Sulu çözeltisinin kendisine özgü, yakan bir kokusu vardır. Formaldehit, genellikle %37'lik sulu çözeltisi şeklinde taşınır veya depo edilir. Bu çözeltiye formalin denir. Formalinden, düşük basınç altında su buharlaşıp, ayrıldığı zaman, paraformaldehit meydana gelir. Bu bir polimer olup, formülü HO(CH2O)xH olan beyaz katı bir maddedir (x yaklaşık 30'dur). Bu polimer ısıtıldığı zaman, gaz formaldehite dönüşür. Bundan dolayı, gaz formaldehit elde etmek için, uygun bir kaynaktır. Saf formaldehitten, polimer ürünler elde edilebildiği gibi, fenol ve kazein ile de sentetik reçine ve plastikler imal edilmektedir.
Elde edilişi
Ticari olarak, metanol buharının hava oksijeni ile oksitlenmesinden veya doğal gazların uygun oksidasyonu ile elde edilir. Formaldehit, 1859 yılında Rus kimyager Aleksandr Butlerov (1828–1886) tarafından keşfedildi.[2]
Kullanım alanı

Formaldehit kimya endüstrisinde en yaygın olarak kullanılan ve üretilen maddelerden birisidir. Saf hâlde renksiz bir gazdır ve sıklıkla en fazla %37'lik olmak üzere sulu çözelti hâlinde kullanılır (formalin). Formalin çözeltilerinde bir miktar da metil alkol bulunmaktadır. Gerek gaz hâli gerekse sıvı çözeltisi kendisine özgü, hoşa gitmeyen bir kokuya sahiptir. Oksitleyen maddelerle hızla tepkimeye girer, yüksek derişimlerinde yanıcı bir sıvıdır. Hidroklorik asitle bis(klorometil) eter buharı oluşturacak şekilde tepkimeye girer, oluşan bu madde ise kanser yapıcı bir maddedir. Tıp laboratuvarlarda koruyucu sıvı ve sterilize edici madde olarak kullanılmaktadır. Başlıca reçine imalatında ve kimyasal üretim ara maddesi olarak kullanılmaktadır. Üre-formaldehit ve fenol-formaldehit reçineler köpük yalıtımı malzemelerinin, yapımında, sunta ve kontrplak imalinde tekstil ürünlerinin işlenmesinde ve ayrıca, formaldehit üre, fenol ve melamin reçinelerinin yapımında kullanılmaktadır.
Kişisel bakım ürünlerinde mikropların üremesini önlemek için koruyucu olarak kullanılır, bu dozu insan için tehlike arz etmez. Ayrıca bazı aşılarda da ölü hücreleri korumak için kullanılır.
Formaldehit zehirlenmesi
Formaldehit etkilenimi çoğu kez gaz hâlinde iken solunum yoluyla alınmasına bağlı olarak meydana gelir. Formaldehit soluyan kişilerde yorgunluk, uyuklama, baş ağrısı, baş dönmesi, deri döküntüleri gibi şikayetler görülür. Ancak sıvı formaldehit deri yoluyla da emilebilir. İşçiler, üretim sırasında, maddelerin işlenmesinde ve reçine imalatında etkilenebilir. Sağlık elemanları, eğitim görevlileri ve öğrenciler de formaldehit içerisinde saklanan ve hazırlanmasında formaldehit kullanılan materyallere bağlı olarak yüksek etkilenim riski altındadır. Tüketiciler inşaatta kullanılan bazı malzemelerden, kozmetiklerden, ev parkelerinden, ev mobilyalarından ve dokuma ürünlerinden yayılan formaldehitten etkilenebilirler. Ani formaldehit etkilenimi ölüme neden olabilir. Koku eşiği 1 ppm civarındadır. Koku duyusu yorgunluğuna bağlı olarak formaldehit kokusunu algılama eşiği zamanla yükselebildiğinden kokunun uyarıcı bir faktör olarak kabul edilmesi çok zordur. Uzun süreli olarak düşük dozlarda formaldehite maruziyet solunum güçlüğü, ekzema ve alerjik reaksiyonlara yol açabilir. Formaldehit insanlarda kanser yapıcı maddeler arasında sayılmaktadır. Burun ve akciğer kanseri ile bağlantılı, beyin kanseri ve lösemiyle de ilişkili olduğu düşünülmektedir. Havada 0,1 ppm bulunduğunda, gözlerin sulanmasına, öksürüğe, nefes darlığına, hırıltılı solunuma, deri döküntülerine, alerjik tepkilere, göz, burun ve boğazda yanmaya neden olur. Etkilenime bağlı olarak kusma ve ishale de yol açar. Duyarlığa yol açması nedeniyle daha sonraki etkilenimler aynı derişimde daha şiddetli reaksiyolara yol açabilir. 2 ppm konsantrasyonda gözlerde tahriş yapar, 20 ppm de tek bir etkilenimle bile korneada kalıcı matlaşmaya neden olur. 25 ppm üzerindeki etkilenimler öldürücü akciğer ödemi dahil çok şiddetli tepkilere yol açar.
Notlar
- ^ a b Formaldehyde (PDF) 13 Haziran 2018 tarihinde Wayback Machine sitesinde arşivlendi., SIDS Initial Assessment Report, International Programme on Chemical Safety
- ^ Butlerow, A (1859). Ueber einige Derivate des Jodmethylens [On some derivatives of methylene iodide]. Annalen der Chemie und Pharmacie. 111. ss. 242-252. 12 Ocak 2023 tarihinde kaynağından arşivlendi. Erişim tarihi: 27 Haziran 2015.
Kaynakça
- Rehber Ansiklopedisi
https://pubchem.ncbi.nlm.nih.gov/compound/Formaldehyde12 Nisan 2019 tarihinde Wayback Machine sitesinde arşivlendi.












