Fonksiyonel grup
Organik kimyada fonksiyonel grup, içinde bulundukları moleküllerin karakteristik kimyasal tepkimelerinden sorumlu belli atom gruplarıdır. Aynı fonksiyonel grup aynı veya benzer kimyasal tepkimere girer, ait olduğu molekülün büyüklüğünden bağımsız olarak.
Aşağıda en yaygın fonksiyonel grupların bir listesi bulunmaktadır. Bu formüllerde R ve R' sembolleri bir alkil grubunu temsil eder.
Temel biyolojide sözü geçen gruplar için temel fonksiyonel gruplar listesine bakınız.
| Kimyasal sınıf | Grup | Formül | Yapısal formül | Ön ek | Son ek | Örnek |
|---|---|---|---|---|---|---|
| Asil halojenür | Haloformil | RCOX |  | haloformil- | -oyl halojenür |  Asetil klorür (Etanoyl klorür) |
| Alkol | Hidroksil | ROH | hidroksi- | -ol |  Metanol | |
| Aldehit | Aldehit | RCHO |  | okso- | -al |  Asetaldehit (Etanal) |
| Alkan | Alkil | RH | alkil- | -an | 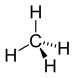 Metan | |
| Alken | Alkenil | R2C=CR2 | 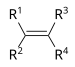 | alkenil- | -en | 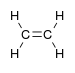 Etilen (Eten) |
| Alkin | Alkinil | RC≡CR' | alkinil- | -in | Asetilen (Etin) | |
| Amid | Karboksamid | RCONR2 |  | karboksamido- | -amid |  Asetamid (Etanamid) |
| Aminler | Birincil amin | RNH2 | amino- | -amin | 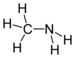 Metilamin (Metanamin) | |
| İkincil amin | R2NH |  | amino- | -amin | Dimetilamin | |
| Üçüncül amin | R3N | 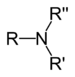 | amino- | -amine | 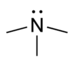 Trimetilamin | |
| 4° amonyum iyonu | R4N+ | 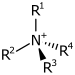 | amonyo- | -amonyum | 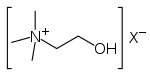 Kolin | |
| Azid | Azid | RN3 | azido- | alkil azid |  Fenil azid (Azidobenzen) | |
| Azo bileşikleri | Azo (Diimid) | RN2R' | azo- | -diazen | 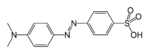 Metil turuncu (p-dimetilamino-azobenzensülfonik asit) | |
| Tolüen türevi | Benzil | RCH2C6H5 RBn | benzyl- | 1-(substituent)tolüen | Benzyl bromür (1-Bromotolüen) | |
| Karbonat | Karbonat ester | ROCOOR | alkil karbonat | |||
| Karboksilat | Karboksilate | RCOO− | 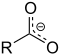
| karboksi- | -oat | Sodyum asetat (Sodyum etanoat) |
| Karboksilik asit | Karboksil | RCOOH | 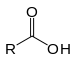 | karboksi- | -oik asit | 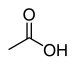 Asetik asit (Etanoik asit) |
| Siyanatlar | Siyanat | ROCN | Siyanato- | alkil siyanat | ||
| Tiosiyanat | RSCN | tiyosiyanato- | alkil tiyosiyanat | |||
| Disülfür | Disülfür | RSSR' | alkil alkil disülfür | Sistamin (2,2'-Ditiyobis(etilamin)) | ||
| Eter | Eter | ROR' | alkoksi- | alkil alkil eter | Dietil eter (Etoksietan) | |
| Ester | Ester | RCOOR' | alkil alkanoat | Etil bütirat (Etil bütanoat) | ||
| Haloalkan | Halo | RX |  | halo- | alkil halojenür | Kloroetan (Etil klorür) |
| Hidroperoksit | Hydroperoksi | ROOH | hidroperoksi- | alkil hidroperoksit | Metil etil keton peroksit | |
| İmin | birincil ketimin | RC(=NH)R' | 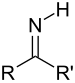 | imino- | -imin | |
| İkincil ketimin | RC(=NR)R' | 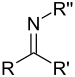 | imino- | -imin | ||
| birincil aldimin | RC(=NH)H |  | imino- | -imin | ||
| İkincil aldimin | RC(=NR')H | 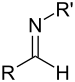 | imino- | -imin | ||
| İmid | İmid | RC(=O)NC(=O)R' | 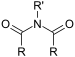 | imido- | -imid | |
| İsosiyanür | İzosiyanür | RNC | izosiyano- | alkil izosiyanür | ||
| İzosiyanatlar | İzosiyanat | RNCO | isosiyanato- | alkyl izosiyanat | Metil izosiyanat | |
| İsotiosiyanat | RNCS | izotiyosiyanato- | alkil izotiyosiyanat | Alil izotiyosiyanat | ||
| Keton | Karbonil | RCOR' |  | keto-, okso- | -on | 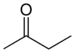 Metil etil keton (Butanon) |
| Nitrat | Nitrat | RONO2 | nitrooksi-, nitroksi- | alkil nitrat |  Amil nitrat (1-nitrooksipentan) | |
| Nitril | Nitril | RCN | siyano- | alkannitril |  Benzonitril (Fenil siyanür) | |
| Nitrit | Nitrosooksi | RONO | nitrosooksi- | alkil nitrit |  Amil nitrit (3-metil-1-nitrosooksibutan) | |
| Nitro bileşiği | Nitro | RNO2 | 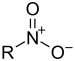 | nitro- | 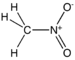 Nitrometan | |
| Nitroso bileşiği | Nitroso | RNO | nitroso- | Nitrosobenzen | ||
| Peroksit | Peroksi | ROOR | peroksi- | alkil peroksit | Di-tert-butil peroksit | |
| Benzen türevi | Fenil | RC6H5 | fenil- | -benzen | 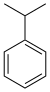 Kümen (2-fenilpropan) | |
| Fosfin | Fosfino | R3P | fosfino- | -fosfan | Metilpropilfosfan | |
| Fosfodiester | Fosfat | HOPO(OR)2 | fosforik asit di(substituent) ester | di(substituent) hydrojenfosfat | DNA | |
| Fosfonik asit | Fosfono | RP(=O)(OH)2 |  | fosfono- | substituent fosfonic asit | Benzilfosfonik asit |
| Fosfat | Fosfat | ROP(=O)(OH)2 |  | fosfo- | Gliseraldehit 3-fosfat | |
| Piridin türevi | Piridil | RC5H4N |
| 4-pyridil 3-pyridil 2-pyridil | -pyridine |  Nikotin |
| Sulfür | RSR' | di(substituent) sülfür | Dimetil sülfür | |||
| Sülfon | Sülfonil | RSO2R' |  | sülfonil- | di(ornatık) sülfon | Dimetil sülfon (Metilsülfonilmetan) |
| Sülfonik asit | Sülfo | RSO3H | 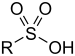 | sülfo- | substituent sülfonik asit | 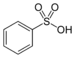 Benzensülfonik asit |
| Sülfoksit | Sülfinil | RSOR' | 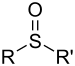 | sülfinil- | di(ornatık) sülfoksit |  Difenil sülfoksit |
| Tiyol | Sülfhidril | RSH | merkapto-, sülfanil- | -tiol | Etantiyol (Etil merkaptan) |
Fonksiyonel grupların isimlerini alkanlarınkiyle birleştirmek organik bileşikleri isimlendirmek için güçlü bir adlandırma sistemi yaratır.
Fonksiyonel grupların hidrojen olmayan atomları birbirleriyle ve molekülün geri kalanı ile kovalent bağlarla bağlıdır. Atomlar grubu molekülün kalan kısmıyla iyonik kuvvetle bağlanmışsa bu atom grubu çokatomlu iyon veya kompleks iyon olarak adlandırmak daha doğrudur. Bu atom gruplarına toplu olarak radikal denir, serbest radikal terimi bundan türetilmiştir.
Fonksiyonel grubun bağlı olduğu karbona alfa karbon denir.
Fonksiyonel gruplar organik moleküllerin omurgalarına bağlı olurlar. Molekülün özelliklerini ve kimyasal tepkimelerini belirlerler. Fonksiyonel gruplar karbon omurgadan daha az kararlıdır ve kimyasal tepkimeye girmeye daha eğilimlidirler.
Dış bağlantılar
- IUPAC ligand kısaltmaları (pdf) (İngilizce)
- IUPAC Gold Book (Kimya terminolojisi hülasası)27 Nisan 2006 tarihinde Wayback Machine sitesinde arşivlendi. (İngilizce)
- IUPAC Blue Book (Organik isimlendirme)8 Haziran 2011 tarihinde Wayback Machine sitesinde arşivlendi. (İngilizce)