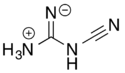
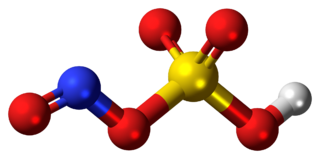
Disiyandiamid
| |||
| Adlandırmalar | |||
|---|---|---|---|
2-Siyanoguanidin | |||
Diğer adlar Siyanoguanidin, N-siyanoguanidin, 1-siyanoguanidin, 2-siyanoguanidin, Guanidin-1-karbonitril, disiyandiamin, Didin, DCD, Disi | |||
| Tanımlayıcılar | |||
CAS numarası | |||
3D model (JSmol) |
| ||
| ChEBI | |||
| ChemSpider | |||
| ECHA InfoCard | 100.006.649 | ||
| EC Numarası |
| ||
PubChem CID | |||
| RTECS numarası |
| ||
| UNII | |||
CompTox Bilgi Panosu (EPA) | |||
| |||
| |||
| Özellikler | |||
| Molekül formülü | C2H4N4 | ||
| Molekül kütlesi | 84.08 g/mol | ||
| Görünüm | Beyaz kristaller | ||
| Yoğunluk | 1.400 g/cm3 | ||
| Erime noktası | 209.5 | ||
| Kaynama noktası | 252 | ||
| Çözünürlük (su içinde) | 41.3 g/l | ||
| log P | -0.52 | ||
Henry yasası sabiti (kH) | 2.25•10−10 atm.m3/mol | ||
| -44.55•10−6 cm3/mol | |||
| Tehlikeler | |||
| GHS etiketleme sistemi: | |||
| Piktogramlar |  | ||
| İşaret sözcüğü | Dikkat | ||
| Tehlike ifadeleri | H302, H312, H332 | ||
| Önlem ifadeleri | P261, P264, P270, P271, P280, P301+P312, P302+P352, P304+P312, P304+P340, P312, P322, P330, P363, P501 | ||
| Aksi belirtilmediği sürece madde verileri, Standart sıcaklık ve basınç koşullarında belirtilir (25 °C [77 °F], 100 kPa). | |||
Disiyandiamid guanidinden türetilmiş bir nitrildir. Bir siyanamid dimeridir ve siyanamidden hazırlanabilir. Disiyandiamid, su, aseton ve alkolde çözünebilen renksiz bir katıdır. Polar olmayan organik çözücülerde çözünemez.[1]
Üretimi ve kullanımı
Disiyandiamid, siyanamidin baz ile olan reaksiyonu ile üretilir. Toprakta siyanamidin ayrışmasıyla üretilir. Disiyandiamid, guanidinler ve melaminden çeşitli faydalı bileşikler üretilir. Örneğin, asetoguanamin ve benzoguanamin, disiyandiamidin nitrille olan kondenzasyonundan hazırlanır:[2][3]
- (H2N)2C=NCN + RCN → (CNH2)2(CR)N3
Disiyandiamid ayrıca yavaş salınımlı bir gübre olarak kullanılır. Eskiden bazı patlayıcılarda yakıt olarak kullanılıyordu. Yapıştırıcı endüstrisinde epoksi reçineleri için sertleştirici madde olarak kullanılır.[1]
Kimyası
Nitril grubunun bağlı olduğu azotun protonlanması ve bağlanmasında farklılık gösteren iki tautomerik form mevcuttur.
Disiyandiamid, azotlar arasında biçimsel bir asit-baz tepkimesi yoluyla zwitteriyonik bir formda da bulunabilir.
Zwitteriyonik formdan amonyak (NH3) kaybının ardından, geriye kalan azot atomunun protondan arındırılmasıyla, disiyanamid anyonunu, [N(CN)2]− verir.
Kaynakça
- ^ a b Thomas Güuthner; Bernd Mertschenk (2006). "Cyanamides". Ullmann's Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. doi:10.1002/14356007.a08_139.pub2.
- ^ H. Deim; G. Matthias; R. A. Wagner (2012). "Amino Resins". Ullmann's Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. doi:10.1002/14356007.a02_115.pub2.
- ^ J. K. Simons; M. R. Saxton (1953). "Benzoguanamine". Organic Syntheses. 33: 13. doi:10.15227/orgsyn.033.0013.
Dış bağlantılar
- Uluslararası Kimyasal Güvenlik Kartı 0650
- OECD document17 Mayıs 2017 tarihinde Wayback Machine sitesinde arşivlendi.
- Entry at chemicalland21.com14 Eylül 2020 tarihinde Wayback Machine sitesinde arşivlendi.