
Rubidyum, Rb sembolü ile gösterilen, 37 atom numarasına sahip alkali metaller grubundan bir kimyasal element. 1861 yılında Gustav Kirchhoff ve Robert Bunsen tarafından Almanya'da keşfedilmiştir. Kimyasal açıdan potasyum ve sezyumun özelliklerine benzer özellikler gösterir ama potasyuma oranla çok ender bulunur. Oda sıcaklığında gümüşi beyaz renkli, yumuşak ve parlak bir katıdır. Kuru havada bile çok çabuk yükseltgenir, bu yüzden açık havada saklanamaz. Suyu şiddetle ayrıştırır ve ortaya çıkan hidrojeni tutuşturur.

Sodyum, periyodik cetvelde Na simgesi ile gösterilen ve atom numarası 11 olan element. Sodyum yumuşak ve kaygan bir metal olup alkali metaller grubuna aittir. Doğal bileşiklerin içinde bol miktarda bulunur. Yüksek oranda reaktiftir, sarı bir alevle yanar, su ile şiddetli reaksiyon verir ve havada hızla oksitlenir. Dolayısıyla, vazelin, gazyağı gibi hava ve su ile temasını kesecek bir ortamda saklanması gerekir.
Hidroliz işlemi suyu oluşturan hidrojen ve oksijen elementlerinin birbirinden ayrılması ile sonuçlanan bir işlemdir. Bazı kaynaklarda hidroliz, moleküllerin su ilavesiyle daha fazla sayıda parçacık oluşturması olarak da geçer. Hidroliz, su ile bir kimyasal bağın parçalanmasıdır yani bir kimyasal reaksiyondur. Hidroliz genel olarak suyun nükleofil olduğu ikame(yer değiştirme reaksiyonu), eliminasyon(organik reaksiyon türü) ve solvasyon (çözme) reaksiyonları için kullanılır.
Kloroform veya triklorometan, CHCl
3 formülüne sahip bir organik bileşiktir. Oda sıcaklığında kolay buharlaşan, hoş kokulu, renksiz, yanıcı olmayan ağır bir sıvıdır. Çözücü olarak sıkça kullanılır. PTFE (Teflon) ve bazı soğutucuların üretiminde kullanılmak için bol miktarlarda üretilir.

Sodyum perklorat formülü NaClO4 olan bir kimyasal bileşiktir. Perklorik asitin sodyum tuzu olan bu bileşik diğer perkloratlar gibi kuvvetli bir oksitleyicidir. Sodyum perkloratın çözünürlüğü diğer perklorat tuzları içinde en yüksek olanıdır. Beyaz kristallerden oluşan ve higroskopik özellikte olan sodyum perklorat suda ve alkolde oldukça çok çözünür. Genellikle monohidrat form halinde bulunur ve rombik bir kristal yapısına sahiptir. Standart oluşum entalpisi −382.75 kJ mol−1 dir.

Potasyum perklorat formülü KClO4 olan bir kimyasal bileşiktir. Diğer perkloratlar gibi, bu tuz da güçlü bir oksitleyici olup potansiyel olarak birçok organik maddeyle reaksiyona girer. Havai fişek, mühimmat kapsülleri ve primer patlayıcılarda yaygın bir oksitleyici olarak kullanılan katı ve renksiz kristallerden oluşan bu madde çeşitli şekilde itici yakıtlar, flaş bileşimleri, yıldızlar ve maytaplarda da kullanılmaktadır. Daha yüksek performanslı amonyum perklorat yerine çoğu kez ikame edilerek katı yakıtlı roket itici yakıtı olarak da kullanılmıştır. KClO4 alkali metal perkloratlar içerisinde en düşük çözünürlüğe sahiptir (25 °C'deki 100 ml. suda 1.5 gr.).
Yer değiştirme reaksiyonu, reaksiyona giren iki kimyasal tür arasındaki bağların değişimi ile benzer ya da aynı bağlanma özelliğindeki ürünlerin oluşumuna yol açan kimyasal bir işlemdir. Bu reaksiyonun temsil edildiği genel şema şu şekildedir:

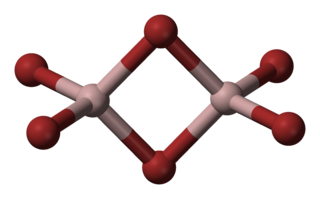
Alüminyum bromür veya diğer adıyla alüminyum tribromür, içinde alüminyum ve brom bulunan, kimyasal formülü AlBr3 veya Al2Br6 olan kimyasal birleşik Mol kütlesi 374,8 gram, erime noktası 97 °C, kaynama noktası 255 °C, yoğunluğu 3,01 g/mL olan suda çözünebilen bir maddedir. Sentezlerde açilleme katalizörü olarak kullanılan, beyazdan sarıya değişen renkte, nem çekici, kristal yapıda bir maddedir. Havada kuvvetle dumanlanır, suyla şiddetle birleşir. Organik çözücülerde çözünür. Dimer biçiminde de bulunur (Al2Br6).

Karbon tetraklorür ya da tetraklorometan, CCl4 formülüne sahip bir klorokarbon. Kokusu Kloroforma benzeyen, renksiz, yanıcı olmayan, sudan ağır bir sıvıdır. Suda çözünmezken birçok organik çözücü içinde çözünür. Geçmişte soğutucu gazların üretiminde, yangın söndürücülerde lav lambalarında, temizlik malzemesi ve kurt düşürücü olarak yaygın bir şekilde kullanılmıştır.

Sodyum bromür, NaBr formülüne sahip inorganik bir bileşiktir. Yüksek erime noktasına sahip beyaz kristal yapısıyla sofra tuzuna benzemektedir. Genellikle bromür iyonu kaynağı olarak çeşitli alanlarda kullanılmaktadır.
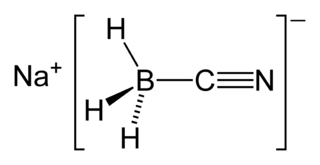
Sodyum siyano borhidrür kimyasal formülü NaBH3(CN) olan bir bileşiktir. Normalde beyaz renkli bir tozdur ancak ticari olarak taba renginde de bulunabilir. Genellikle organik sentezlerde iminlerin indirgenmesi amacıyla kullanılır. Tuz, sulu hâlini tolere edebilir.
Polisülfürler kükürt atom zincirleri içeren bir sınıf kimyasal bileşiklerdir. Polisülfürler iki ana sınıfa ayrılır: anyonlar ve organik polisülfürler. Anyonlar S2−ngenel formülüne sahiptir. Bu anyonlar hidrojen polisülfürlerin H2Sn konjüge bazlarıdır. Organik polisülfürler genellikle RSnR formülüne sahiptir, burada R = alkil veya arildir.

Trihidridoboron, boran veya borin, BH3 kimyasal formülü ile gösterilen dengesiz ve oldukça reaktif bir moleküldür. Boran karbonilin BH3(CO) hazırlanması, boran kimyasının araştırılmasında büyük rol oynamıştır. Ancak, BH3 molekül türleri çok güçlü Lewis asidilerdir. Sonuç olarak, oldukça reaktifdir ve doğrudan bir akış sisteminde, sürekli olarak üretilen, geçici bir ürün olarak veya lazerle çıkarılmış atomik borun hidrojen ile reaksiyonundan doğrudan gözlenebilir.

Tetrakloroetilen, perkloroetilen ya da sistematik adıyla tetrakloroeten, formülü C
2Cl
4 olan bir klorokarbon ve çözücü olarak kullanılan uçucu, ağır bir sıvıdır. Çeşitli yağları çözebilmesinden ötürü yaygın olarak kuru temizleme ve sanayide yağ giderme için kullanılır. Kuru temizleme ile özdeşleștirildiğinden çoğu zaman "kuru temizleme sıvısı" olarak anılır. Otomotiv sanayiinde etkili bir fren temizleyicisidir. Geçmişte hayvanlar ve insanlar üzerinde kurt düşürücü olarak sıkça kullanılmıştır.

Sodyum fenolat (sodyum fenoksit) NaOC6H5 formülüne sahip bir organik bileşiktir. Beyaz kristalimsi bir katıdır. Aynı zamanda fenoksit olarak da bilinen fenolat anyonu, fenolün konjuge bazıdır. Aril eterler gibi diğer birçok organik bileşiğin öncül maddesi olarak kullanılır.

Bir Grignard reaktifi veya Grignard bileşiği, X'in bir halojen ve R'nin normalde bir alkil veya aril olduğu organik bir grup olduğu genel formül R−Mg−X'e sahip kimyasal bir bileşiktir. İki tipik örnek, metilmagnezyum klorür Cl−Mg−CH
3 ve fenilmagnezyum bromür (C
6H
5)−Mg−Br'dir. Organomagnezyum bileşiklerinin bir alt sınıfıdır.
Demir (III) klorür FeCl
3 formüllü inorganik bir bileşiktir. Kristal bir katı olmasının yanı sıra görüş açısına bağlı olarak farklı renklerle gözlemlenebilir; koyu yeşil, mor-kırmızı. Sulu formu da katı formu da fiziksel görünüm olarak koyu kahverengi rengindedir.

Fenton reaktifi kirleticileri veya atık suları oksitlemede kullanılan, katalizör olarak demir içeren bir demir bileşiği (genellikle demir (II) sülfat, FeSO4) ile hidrojen peroksitin (H2O2) bir çözeltisidir. Fenton reaktifi, trikloroetilen (TCE) ve tetrakloroetilen (perkloroetilen, PCE) gibi organik bileşikleri yok etmek için kullanılabilir. 1890'larda Henry John Horstman Fenton tarafından analitik bir reaktif olarak geliştirilmiştir.
Sübstitüsyon reaksiyonu, kimyasal bileşikteki bir fonksiyonel grubun başka bir fonksiyonel grup ile değiştirildiği kimyasal bir reaksiyondur. Yer değiştirme reaksiyonları organik kimyada çok önemlidir. Organik kimyadaki ikame reaksiyonları, reaksiyonda yer alan bir reaktif ara maddenin bir karbokatyon, bir karbanyon veya bir serbest radikal olup olmadığına ve substratın alifatik veya aromatik olup olmadığına bağlı olarak ilgili reaktife bağlı olarak elektrofilik veya nükleofilik olarak sınıflandırılırlar. Bir reaksiyon türünün ayrıntılı olarak anlaşılması, bir reaksiyondaki ürün sonucunun tahmin edilmesine yardımcı olur. Ayrıca, sıcaklık ve çözücü seçimi gibi değişkenlere göre bir reaksiyonu optimize etmek için de yararlıdır.

Reimer–Tiemann reaksiyonu, fenollerin orto-formilasyonu için kullanılan kimyasal bir reaksiyondur. Bu reaksiyon ilk olarak Karl Reimer ve Ferdinand Tiemann tarafından rapor edildi.


















