Hidrojen, sembolü H, atom numarası 1 olan kimyasal bir element. Standart sıcaklık ve basınç altında renksiz, kokusuz, metalik olmayan, tatsız, oldukça yanıcı ve H2 olarak bulunan bir diatomik gazdır. 1,00794 g/mol'lük atomik kütlesi ile tüm elementler arasında en hafif olanıdır. Periyodik cetvelin sol üst köşesinde yer alır. Hidrojenin adı, Yunancada "su oluşturan" anlamına gelen ὑδρογόνο'dan (idrogono) kelimesinden gelir.

Oksijen atom numarası 8 olan ve O harfi ile simgelenen kimyasal elementtir. Oksijen ismi Yunanca ὀξύς (oxis - "asit", tam anlamıyla "keskin", asitlerin acı tadı kastedilir) ve -γενής (-genēs) ("üretici", tam anlamıyla "sebep olan şey") köklerinden gelmektedir, çünkü isimlendirildiği zamanlarda tüm asitlerin oksijen içerikli olduğu sanılırdı. Standart şartlar altında, elementin iki atomu bağlanarak çok soluk mavi renkte, kokusuz, tatsız, diatomik yapıdaki, O2 formülüne sahip dioksijen gazını oluşturur.

Benzin, petrolden imal edilen bir tür yakıttır.
- 150 °C'a kadar ham benzin,
- 150-250 °C'a kadar gaz yağı, kerosen, jet yakıtı,
- 250-350 °C'a kadar dizel yakıtı,
- 350 °C'dan sonra da ağır yağlar elde edilir.

Cıva sembolü "Hg" ve atom numarası 80 olan kimyasal element. "Hg" sembolü, Latincedeki hydrargyrum sözcüğünden gelir. Oda sıcaklığında sıvı hâlde bulunan Cıva için İngilizcede iki sözcük kullanılır: "mercury" ve "quicksilver".

Organik kimya, organik bileşiklerin ve organik maddelerin yani karbon atomlarını içeren çeşitli formlardaki maddelerin yapısını, özelliklerini ve reaksiyonların bilimsel çalışmasını içeren, kimyanın bir alt dalıdır. Yapının incelenmesi yapısal formüllerini belirler. Özelliklerin incelenmesi, fiziksel ve kimyasal özellikleri ve davranışlarını anlamak için kimyasal reaktivitenin değerlendirilmesidir. Organik reaksiyonların incelenmesi doğal ürünlerin, ilaçların ve polimerlerin kimyasal sentezini ve bireysel organik moleküllerin laboratuvarda ve teorik çalışma yoluyla incelenmesidir.
Sinir gazı, solunum, enjeksiyon ya da deriden nüfuz yoluyla vücuda girip nöronlara zarar vererek vücutta, istemsiz kasılma ve ölüme sebep olan kimyasal maddedir.
Alaşım, bir metal elementin en az bir başka element ile birleşmesiyle oluşan homojen karışımıdır. Elde edilen malzeme yine metal karakterli malzeme olur. Alaşımlar karışıma giren metallerin özelliklerinden farklı özellikler gösterirler. En bilinen alaşımlara; tunç (bakır-kalay), pirinç (bakır-çinko), lehim (kalay-kurşun) ve cıva alaşımları olan amalgamlar örnek verilebilir. Alaşımlar, uygulamaların gerektirdiği fiziksel özelliklere sahip malzemeler üretilmesinde yaygın olarak kullanılır.

Kimyasal savaş, kimyasal silahların kullanıldığı saldırılara verilen isimdir.
Toluen tinerin karakteristik kokusuna sahip renksiz, suda çözünmeyen bir sıvıdır. Toluen, bir fenil grubuna bağlı CH3'ten oluşan mono-substituent benzen türevidir. Bundan dolayı toluenin IUPAC sistematik adı metil benzendir. Toluen bir aromatik hidrokarbondur. Ayrıca TNT (trinitrotoluen) patlayıcı madde yapımında kullanılır.

Ekstraksiyon, bir çözelti ya da süspansiyon içindeki inorganik veya organik bir maddeyi bir başka çözücü yardımıyla ayırma işlemidir. Kimyada bilinenin aksine bir saflaştırma değil ayırma yöntemi olarak kullanılır.

Victor Grignard, Fransız kimyager.

Kimyasal silahlar, insan üzerinde fiziksel veya psikolojik tahrip etkisi yapmak üzere kimyevî maddelerin zehirleyici özelliklerinden yararlanılarak üretilmiş olan maddelerdir. Bu maddeler, cansız olmaları nedeniyle çoğalmaları veya insandan insana veya diğer canlılara bulaşmaları söz konusu değildir.

Uçucu yağ ya da organik hidrosol, çiçek veya bitki özsuları, distile özsuları veya bitki suları olup damıtma işleminin su içeren bir yan ürünüdür.

Çevre kirliliği, çevrenin doğal olmayan bir şekilde insan eliyle doğallığının bozulmasıdır. Bu ekosistemi bozma eylemleri; kirlenme şeklinde tabir edilmektedir.

Kimyasal madde, kimyevî madde veya kısaca kimyasal, sabit bir kimyasal bileşimi ve karakteristik özelliklere sahip bir madde türüdür. Bu kimyasal bağlar bozulmadan, fiziksel ayırma yöntemleri ile bileşenlerine ayrılmaz. Bu kimyasallar katı, sıvı veya gaz hâlinde olurlar.

İyot heptaflorür, diğer adıyla iyot(VII) florür ya da iyot florür, IF7 kimyasal formülüne sahip interhalojen bileşiktir. VSEPR teorisinde öngörüldüğü gibi alışılmadık bir beşgen bipiramidal yapıya sahiptir. Molekül, Berry mekanizmasına benzeyen ancak heptakoordineli bir sistem için kullanılan sahte bir Bartell mekanizması isimli bir yeniden düzenlemeye tabi tutulabilir. 4.5 °C'de eriyen renksiz kristallerden oluşur: sıvı aralığı son derece dardır, kaynama noktası 4.77 °C'dedir. Yoğun buhar, küflü ve buruk bir kokuya sahiptir. Molekül D5h simetriye sahiptir.

Fosgen ya da IUPAC tarafından verilen adıyla karbonil diklorür COCl2 formülüne sahip organik bir bileşiktir. Renksiz bir gazdır, kokusu düşük konsantrasyonlarda yeni kesilmiş ot kokusunu andırır. Fosgen, sıvılaştırılmış hâlde saklanır. Sıkıştırıldığında açık sarı bir sıvıya dönüşür. Suda çözünmez ve suyla tepkimeye girer. Benzen, toluen, karbon tetraklorür, asetik asit ve kloroformda çözünür. Alkoller ve çeşitler asitlerin içinde bozunur. Çok zehirli bir gaz olduğu için I. Dünya Savaşı'nda kimyasal silah olarak kullanılmıştır ve 85.000 kadar kişinin ölümüne sebebiyet vermiştir. Fosgenin biraz solunması 36 saat içerisinde ölüme sebep olur. Maruz kalma sınırı 0,5 ppm'dir.

Ayırma işlemi, bir kimyasal madde karışımını en az iki veya daha fazla ürüne dönüştürmek için kullanılan yönteme verilen addır. Ayırma işlemi sonucunda oluşan ürünlerden en az biri, kaynaktaki bileşenlerden en az biri ya da birden fazlası bakımından zenginleşir. Bazı durumlarda karışımlar bir ayırma işlemiyle neredeyse tamamen saf iki bileşene ayırabilir. Karışımın bileşenleri arasındaki fiziksel veya kimyasal farklarından yararlanılarak ayırma gerçekleştirilir.

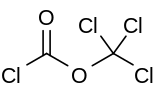
Organoklorürler, klorlu hidrokarbonlar ya da klorokarbonlar, en az bir adet kovalent bağlanmış klor atomuna sahip organik bileşiklerdir. En basit örnekleri kloroalkanlardır. Organoklorürlerin geniş bir yapısal çeşitliliğe sahip olması onların farklı kimyasal özelliklere, isimlere ve kullanım alanlarına sahip olmasına sebep olmuştur. Bazı organoklorürlerin yararlı olmasına karşın bazıları zehirli ve çevreye zararlıdır.
Gaz çıkışı, bir maddede çözünmüş, hapsolmuş, donmuş veya emilmiş bir gazın salınmasıdır. Gaz çıkışına örnek olarak süblimleşme ve buharlaşmanın yanı sıra desorpsiyon, çatlaklardan sızıntı ve yavaş kimyasal reaksiyonlardan açığa çıkan gazlar verilebilir. Kaynama, bir sıvının aynı maddenin buhar fazına geçişi olduğu için genellikle gaz çıkışından ayrı bir olay olarak düşünülür.