Demir sülfat
Demir sülfat deyimi genel bir ifade tarzı olup aşağıdaki anlamlardan biri herhangi birini ifade edebilir:
- Ferro sülfat, Demir(II) sülfat, FeSO4
- Ferri sülfat, Demir(III) sülfat, Fe2(SO4)3
Demir sülfat deyimi genel bir ifade tarzı olup aşağıdaki anlamlardan biri herhangi birini ifade edebilir:
Vitriol bir simya terimidir. Latincede "küçük cam" anlamına gelen "vitriolus" kelimesinden türemiştir. Vitriol adı verilen bileşikler bazı metal sülfatlar ve sülfürik asittir. Kükürt içermemesine rağmen, sülfürik asit kullanılarak yapılan hoş kokulu sıvı dietil etere "tatlı vitriol yağı" denmiştir.

Alçı taşı, kalsiyum sülfat dihidrattan oluşan yumuşak bir sülfat mineralidir ve kimyasal formül CaSO4 · 2H2O'dur. Alçıtaşı ayrıca selenitin yarı saydam kristalleri olarak kristalleşir. Aynı zamanda bir evaporit minerali ve anhidritin hidrasyon ürünü olarak oluşur. İçinde su bulunan kalsiyum sülfat minerali, tek veya ikiz sütunlar hâlinde billûrlanır. Alçı billurlarına kil ve marn içinde veya tuzlu ve alçılı dağların boşluklarında rastlanır.
Anaerobik solunum veya oksijensiz solunum, oksijen (O2) yerine ETS elemanlarının kullanılıp oksidasyon (yükseltgenme) sonucu ATP elde edilmesidir. Aerobik solunum (Oksijenli solunum) ile temel farkı, oksijen kullanılmamasıdır. Fermantasyon ile karıştırılmamalıdır. Anaerobik solunum yapan mikroorganizmalarda elektron taşıma zincirinin sonunda elektron alıcısı olarak oksijen yerine sülfat (SO4), nitrat (NO3) veya kükürt (S) kullanılır. Moleküler oksijenin elektron alma isteğine oranla bu maddelerin elektron alma isteği daha az olduğundan oksijeniz solunumda ortama verilen enerji de oksijenli solunumdan daha düşüktür.

Küprik sülfat ya da sadece bakır sülfat olarak da bilinen Bakır (II) sülfat, kimyasal formülü CuSO4 olan bir kimyasal bileşiktir. Bu tuzun hidrasyon derecelerine bağlı olarak bir dizi farklı bileşikleri mevcuttur. Susuz formu soluk yeşil ya da grimsi beyaz bir toz olmasına karşın en çok bilinen pentahidrat (CuSO4•5H2O) formu, parlak mavi renktedir. Çok az miktardaki CuSO4•5H2O çevreye çok zehirlidir, gözleri ve cildi tahriş eder ve yutulduğunda zararlı da olabilir. Oktahedral moleküler geometriye ve paramanyetik özelliğe sahip olan bakır (II) sülfat ekzotermik olarak suda çözünürek [Cu(H2O)6]2+ kompleksini oluşturur. Bakır (II) sülfat "mavi vitriyol", "göztaşı" ve "göktaşı" olarak da bilinmektedir.

Mangan (II) sülfat, MnSO4 formüllü inorganik bileşiktir. Bu renksiz nemli katı ticari açıdan önemli bir mangan (II) tuzudur. 2005 yılında dünyada yaklaşık olarak 260M kg/y kadar üretildi. Mangan metalinin ve birçok kimyasal bileşiğin ön maddesidir. Mangan eksikliği olan topraklar bu tuzla düzeltilir.
Şaplar çift tuz grubuna giren bileşiklerdir. Genel formülleri [M+1M+3(SO4)2.12H2O] şeklindedir. Buradaki M+1 = K+, NH4+, Rb+, Cs+, TI+; M+3 = Al+3, Fe+3, Ga+3, In+3, Cr+3, V+3 şeklinde ifade edilebilir.
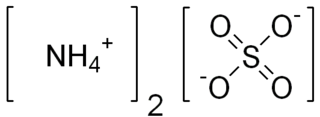
Amonyum sülfat, (NH4)2SO4 formülüne ve çok sayıda ticari kullanıma sahip bir inorganik tuzdur. Toprak gübresi olarak yaygın bir şekilde kullanılır. %21 azot ve %24 kükürt içerir.

Fransa'nın Bourgogne bölgesinde ilk defa üzüm ve asmaların tedavisinde kullanıldığı için bu bölgenin adını alan Burgonya bulamacı bakır sülfat ve sodyum karbonatın bir karışımıdır. İçerisinde %1 -20 arasında toplam bir bakır konstrasyonuna sahip olabilen bu bulamaç, ağaçlar ve küçük meyvelerdeki fungal etmenlere karşı püskürtülerek kullanılır.

Potasyum sülfat, formülü K2SO4 olan, yanmaz, suda çözünebilen beyaz kristal yapıda bir potasyum tuzudur. Genellikle potasyum ve kükürt kaynağı olarak gübrelerde kullanılır.

Evaporit, sulu bir çözeltinin buharlaşmasıyla kristalleşme ve yoğunlaşma sürecinde sonuçlanır. Evaporit suda çözünen mineral sedimentin (mineralin) ismidir. İki çeşit tuz taşı birikintisi vardır:

Magnezyum sülfat kimyasal formülü MgSO4 olan, magnezyum, kükürt ve oksijen ihtiva eden bir inorganik tuz. Genellikle heptahidrat (MgSO4·7H2O) formunda sülfat minerali olan Epsomit ya da diğer adıyla Epsom tuzu (İngiliz tuzu) hâlinde bulunur. Epsom adını İngiltere'deki bir yerleşim yerinden almıştır. Monohidrat formu olan kieseritin (MgSO4·H2O) 1970'lerin ortalarında genel küresel yıllık kullanımı 2.3 milyon ton civarındaydı ve bunun büyük çoğunluğu tarımda kullanılmıştır.

Kristal suyu içeren kalsiyum sülfat (CaSO4.2H2O), alçı taşı (jips) olarak adlandırılır. Alçı taşı yaygın olarak mücevher yapımında ve dişçilikte kullanılır. Alçı taşı 128 °C'ta ısıtıldığında içerdiği suyun %75'ini kaybederek alçıya dönüşür. Alçı suyla karıştırılırsa suyu kendisine bağlayarak sertleşir. Bu özelliğinden dolayı alçı kalıpçılıkta, dekorasyon ve işlerinde kullanılır. Heykeltıraşlar heykel yaparken alçının içine su katarlar.

Gümüş sülfat (Ag2SO4) gümüş kaplamada ve gümüş nitrat yerine boyanmayan madde olarak kullanılan gümüş iyonik bileşiği. Bu sülfat normal kullanım ve depolama durumunda kararlıdır fakat havaya ve ışığa maruz kaldığında kararır. Suda çok az çözünür.

Demir mazı mürekkebi, demir tuzlarından ve bitkisel kaynaklardan gelen tannik asitlerden yapılmış mor-siyah veya kahverengi-siyah mürekkeptir. Avrupa'da 5. ve 19. yüzyıllar arasındaki ondört yüz yıl boyunca kullanılan standart mürekkep formülasyonuydu, 20. yüzyılda yaygın olarak kullanılmaya devam etti ve bugün hala satılıyor.

Alüminyum sülfat Al2(SO4)3 formülüne sahip kimyasal bir bileşiktir. Suda çözünür ve esas olarak içme suyu ve atık su arıtma tesislerinin saflaştırılmasında ve ayrıca kağıt imalatında pıhtılaştırıcı bir ajan olarak kullanılır.

Nikel sülfat NiSO
4 formülüne sahip bir metal bileşiğidir. Nikel sülfat hidratsız formu oda sıcaklığında sarımsı bir renge sahipken hekzahidrat ve heptahidrat hâli mavi bir renge sahiptir, bakır sülfat rengini andırır. Suda çok iyi çözünür.

Fenton reaktifi kirleticileri veya atık suları oksitlemede kullanılan, katalizör olarak demir içeren bir demir bileşiği (genellikle demir (II) sülfat, FeSO4) ile hidrojen peroksitin (H2O2) bir çözeltisidir. Fenton reaktifi, trikloroetilen (TCE) ve tetrakloroetilen (perkloroetilen, PCE) gibi organik bileşikleri yok etmek için kullanılabilir. 1890'larda Henry John Horstman Fenton tarafından analitik bir reaktif olarak geliştirilmiştir.
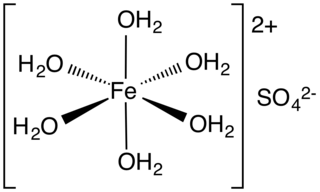
Demir (II) sülfat veya demir sülfat FeSO4•xH2O formülüne sahip bir dizi tuz anlamına gelir. Bu bileşikler en yaygın olarak heptahidrat (x = 7) olarak bulunursa da x için birkaç değer bilinmektedir. Hidratlı form tıp alanında demir eksikliğini tedavi etmek ve ayrıca endüstriyel uygulamalar için kullanılır. Antik çağlardan beri, Zaç-ı Kıbrıs ve yeşil vitriyol (vitriyol, sülfat için eski bir isimdir) olarak bilinen, mavi-yeşil heptahidrat (7 molekül su içeren hidrat) bu maddenin en yaygın şeklidir. Tüm demir (II) sülfatlar suda çözünerek oktahedral moleküler geometriye sahip ve paramanyetik olan aynı akua kompleksi [Fe(H2O)6]2+ verir.
Simya çalışmaları sayesinde daha sonra belirli kimyasal bileşikler veya bileşik karışımları olarak sınıflandırılan birçok kimyasal madde üretilmiştir.

Kobalt(II) sülfat; CoSO4(H2O)x formülüne sahip inorganik bileşiklerden herhangi birine verilen isimdir. Genellikle sırasıyla kobalt sülfat, heksa- veya heptahidratları (CoSO4.6H2O or CoSO4.7H2O) tanımlar. Heptahidrat, suda ve metanolde çözünen kırmızı bir katıdır. Kobalt(II) tek sayıda elektrona sahip olduğu için tuzları paramanyetiktir.