Demir-karbon denge diyagramı
Metalurji biliminde faz terimi, fazın belirli bir kimyasal bileşime, farklı bir atomik bağ ve element düzenine sahip olduğu fiziksel olarak homojen bir madde durumunu belirtmek için kullanılmaktadır. Bir alaşım içinde aynı anda iki veya daha fazla farklı faz mevcut olabilmektedir. Bir alaşım içindeki her fazın kendine özgü fiziksel, mekanik, elektriksel ve elektrokimyasal özellikleri vardır. Bir alaşımda bulunan fazlar, alaşım bileşimine ve alaşımın maruz kaldığı ısıl işleme bağlıdır. Faz diyagramları, belirli bir sıcaklıkta tutulan belirli bir alaşımda bulunan fazların grafiksel temsilleridir. Faz diyagramları, belirli bir ısıl işleme tabi tutulmuş bir alaşımda meydana gelen faz değişikliklerini tahmin etmek için kullanılabilmektedir. Bu önemlidir çünkü bir metal bileşenin özellikleri metalde bulunan fazlara bağlıdır. Faz diyagramları, belirli bir bileşime sahip alaşımların seçimi ve belirli özellikler üretecek ısıl işlem prosedürlerinin tasarımı ve kontrolü için metalurji uzmanları tarafından kullanılmaktadır. Ayrıca kalite sorunlarını gidermek için kullanılırlar.[1]
Demir-Karbon denge diyagramı dönüşümler
Peritektik dönüşüm bir katı ve beraberinde bir sıvı fazın bileşip katı form oluşturmasıdır.
Ötektik dönüşüm bir sıvının iki ayrı katıya dönüşmesi durumudur.
Ötektoid nokta bir katının iki ayrı katı faza dönüşmesidir.
| Peritektik Nokta | δ + Sıvı Östenit |
|---|---|
| Ötektik Nokta | Sıvı Östenit + Sementit |
| Ötektoid Nokta | Östenit Perlit + sementit |
Fazlar
Perlit, %0.80 C içeren ötektoid karışımdır ve 723 °C' de çok yavaş soğuma ile oluşmaktadır. Ferrit ve sementitin çok ince bir levhası veya lamel karışımıdır. Beyaz ferritik arka plan veya matris, ince sementit plakaları (koyu) içermektedir.[2]
Östenit, demirde çözünmüş bir arayer katı karbon çözeltisidir. Yüksek şekillendirilebilirlik, ısıl işlemlerin çoğu bu tek faz ile başlamaktadır. Normalde oda sıcaklığında stabil değildir. Ancak belirli koşullar altında oda sıcaklığında östenit elde etmek mümkündür.[2]
Ferrit, α katı çözelti olarak bilinmektedir. α demirde çözülmüş az miktarda karbonun arayer katı çözeltisidir. 910 derecenin altında kararlı demir formu 723oC' de maksimum çözünürlük %0.025 C' dir ve oda sıcaklığında sadece %0.008 C çözünmektedir. Diyagramda görünen en yumuşak yapıdır.[2]
Sementit veya demir karbür, Fe3C olarak % 6,67 C içerdiğinden, çok sert, kırılgan demir ve karbon intermetalik bileşiğidir.[2]
Diyagramda görünen en sert yapıdır, erime noktası tam olarak bilinmemektedir. Kristal yapısı ortorombiktir. Düşük çekme mukavemetine (yaklaşık 5.000 psi) sahiptir, ancak yüksek basınç mukavemetine sahiptir.[2]
Ledeburit, östenit ve sementitin ötektik karışımıdır. Yüzde 4,3 C içerir ve 1147 °C' de oluşmaktadır.[2]

Demirde bulunan kristal kafes yapıları
Demir, farklı allotroplarını kullanarak pek çok farklı uygulamada kullanılmaktadır. 4 allotrop demir vardır:

- Alfa
- Gama
- Delta
- Epsilon
Bunlardan alfa, gama ve delta demirin tümü atmosfer basıncında bulunurken epsilon yalnızca yüksek basınçlarda bulunmaktadır.[3]
Alfa demir
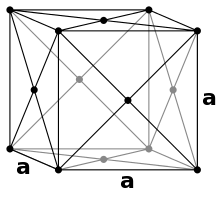
Alfa demir, erimiş demir 910 °C' ye soğutulduğunda oluşan hacim merkezli kübik bir allotroptur. Sadece küçük karbon konsantrasyonlarını çözebilmektedir. Çelik bir demir-karbon alaşımı olduğundan, alfa-demirden yapılan çelik düşük karbonlu bir çeliktir. Bu çelik türü sünektir ve tellerde kullanılmaktadır. Alfa demir en yüksek hacmi içerir ve üç atmosferik allotroptan en az yoğun olanıdır. Alfa demir aynı zamanda oda sıcaklığında bulunan en kararlı demir şeklidir.[3]
Gama demir
Gama demiri, erimiş demir 1392 °C'ye soğutulduğunda oluşan yüzey merkezli kübik bir allotroptur. Bu form en düşük hacme sahiptir ve en yoğun olanıdır. Yüzey merkezli kübik kristal yapı, birbirine bağlı bir demir atomu küpüne sahiptir ve küpün her yüzünde birbirine bağlı demir atomları vardır.[3]
Dış bağlantılar
Kaynakça
- ^ "Phase Diagram". Industrial Metallurgists (İngilizce). 8 Temmuz 2020 tarihinde kaynağından arşivlendi. Erişim tarihi: 4 Temmuz 2021.
- ^ a b c d e f "Arşivlenmiş kopya" (PDF). 9 Temmuz 2021 tarihinde kaynağından arşivlendi (PDF). Erişim tarihi: 4 Temmuz 2021.
- ^ a b c "Allotropes of Iron: Types, Density, Uses & Facts". study.com. 4 Temmuz 2021. 9 Temmuz 2021 tarihinde kaynağından arşivlendi. Erişim tarihi: 4 Temmuz 2021.










