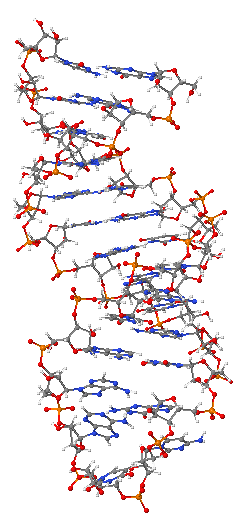
DNA ergimesi
DNA denatürasyonu (DNA ergimesi olarak da bilinir), iki iplikçikli DNA'nın bazları arasındaki hidrojen bağlarının kırılması sonucu, çözülüp, iplikçiklerinin birbirinden ayrılması sürecidir. Her iki terim de, çözeltideki DNA'nın ısıtılması sonucu iplikçiklerin ayrılması için kullanılır ancak denatürsayon, üre gibi kimyasallar tarafından da meydana gelebilir. Çok sayıda DNA molekülünden söz edilirken, ergime sıcaklığı (Tm), DNA iplikçiklerinin yarısının ikili sarmal, yarısının ise rastgele sarım (İng. random coil) hâlinde olduğu sıcaklıktır.[1] Ergime sıcaklığı, molekülün uzunluğuna ve onun nükleotit bileşimine bağlıdır.
DNA denatürasyonunun uygulamaları
DNA denatürasyonu DNA'nın belli özelliklerinin anlaşılmasında kullanılabilir. Sitozin/guanin baz eşleşmesi adenin/timin baz eşleşmesinden daha kuvvetli olduğu için, bir genomdaki sitozin ve guanin oranı (GC içeriği olarak adlandırılır), genomik DNA'nın ergime sıcaklığının ölçülmesiyle kestirilebilir.[2] Yüksek sıcaklıklar yüksek GC oranına karşılık gelir.
DNA denatürasyonu iki farklı DNA dizisi arasındaki farklılığı belirlemek için kullanılır. DNA ısıtılarak tek iplikçikli bir duruma getirilir ve sonra karışım yavaşça soğutularak iplikçiklerin yeniden hibritleşmesine izin verilir. Hibrit moleküller benzer diziler arasında meydana gelir, diziler arasındaki farklılıklar baz eşleşmesini bozar. Genom düzeyinde, bu yöntem (DNA-DNA hibridizasyonu) kullanılarak iki farklı biyolojik tür arasındaki genetik uzaklık kestirilmiştir.[3] Belli bir DNA bölgesi söz konusu olduğunda, iki dizi arasındaki ufak farklılıkların belirlenebilmesi için denatüran gradyan jel elektroforezi ve sıcaklık gradyan jel elektroforezi kullanılır.[4][5]
Ergime sıcaklığına dayalı DNA analiz yöntemleri ile DNA dizileri hakkında çıkarımı yapmak dolaylı olduğu için genelde doğrudan DNA dizilemesi yapmak yeğlenir.
DNA ergime süreci moleküler biyoloji tekniklerinde kullanılır. Bunların başında polimeraz zincir tepkimesi (PCR) gelir. Bu yöntemde DNA sıcaklığı bilgi verici değildir ancak yöntemde kullanılacak doğru sıcaklığın belirlenebilmesi için Tm'nin kestirilmesi önemlidir. DNA ergime sıcaklıkları eşitlenerek bir grup DNA molekülünün hibridiazsyon kuvvetinin eşitlenmesi sağlanabilir. Bu yöntem, örneğin, DNA mikrodizilimlerindeki oligonükleotit probların tasarlanmasında kullanılır.
Tm belirleme yöntemleri
Tm değerini hesaplamak için çeşitli formüller mevcuttur.[6][7] Bazı formüller DNA ikililerinin (duplekslerinin) ergime sıcaklılarının öndeyiminde daha yanlışsızdır.[8]
En yakın komşu yöntemi
En yakın komçu yöntemi, nükleik asit ikililerinin ergime sıcaklıklarının öndeyisinde kullanılan bir yöntemdir. İki iplikçikli DNA'nın hibridizasyon enerjisinde GC içeriği önemli bir etken olsa da, komşu bazlar arasındaki etkileşim, istiflenme enerjisini de önemli kılar. En yakın komşu yöntemi, nükleik asidin omurgası boyunca bazları ikişer ikişer değerlendirerek bunu hesaba katar.[1] Her birinin entalpik ve entropik parametreleri vardır, bunların toplamı ergime sıckalığını aşağıdaki denkleme göre belirler:
- Burada iki tek iplikçikten bir dupleks oluşma sürecinde
- standart entalpi ve standart entropidir,
- tek sarmallı moleküllerden daha fazla miktarda bulunanın derişimi (genelde bu bir prob ya da primerdir),
- daha düşük miktarda bulunan, komplemanter iplikçiğin derişimidir (genelde bu hedef iplikçiktir),
- evrensel gaz sabitidir. .
Tavlama tepkimesinde standart entalpi ve entropiler negatiftir ve sıcaklıktan bağımsız oldukları varsayılır. Eğer ise, ihmal edilebilir.
Tablo 1. DNA/DNA dupleksleri için en yakın komşu parametreleri[1] değerleri kilokalori/mol olarak verilmiştir ve değerleri kalori bölü mol bölü derece Kelvin olarak verilmiştir.
| En yakın komşu dizisi (5'-3'/5'-3') | kcal/mol | cal/(mol·K) |
|---|---|---|
| AA/TT | -7.9 | -22.2 |
| AG/CT | -7.8 | -21.0 |
| AT/AT | -7.2 | -20.4 |
| AC/GT | -8.4 | -22.4 |
| GA/TC | -8.2 | -22.2 |
| GG/CC | -8.0 | -19.9 |
| GC/GC | -9.8 | -24.4 |
| TA/TA | -7.2 | -21.3 |
| TG/CA | -8.5 | -22.7 |
| CG/CG | -10.6 | -27.2 |
| Uç A-T baz çifti | 2.3 | 4.1 |
| Uç G-C baz çifti | 0.1 | -2.8 |
Notlar
- ^ a b c John SantaLucia Jr. (1998). "A unified view of polymer, dumbbell, and oligonucleotide DNA nearest-neighbor thermodynamics". Proc. Natl. Acad. Sci. USA. 95 (4). ss. 1460-5. doi:10.1073/pnas.95.4.1460.[1] 1 Ekim 2007 tarihinde Wayback Machine sitesinde arşivlendi.
- ^ M. Mandel and J. Marmur (1968). "Use of Ultravialet Absorbance-Temperature Profile for Determining the Guanine plus Cytosine Content of DNA". Methods in Enzymology. 12 (2). ss. 198-206. doi:10.1016/0076-6879(67)12133-2. ISBN 978-0-12-181856-2.
- ^ C.G. Sibley and J.E. Ahlquist (1984). "The Phylogeny of the Hominoid Primates, as Indicated by DNA-DNA Hybridization". Journal of Molecular Evolution. Cilt 20. ss. 2-15. doi:10.1007/BF02101980.
- ^ R.M. Myers, T. Maniatis, and L.S. Lerman (1987). "Detection and Localization of Single Base Changes by Denaturing Gradient Gel Electrophoresis". Methods in Enzymology. Cilt 155. ss. 501-527. doi:10.1016/0076-6879(87)55033-9. ISBN 978-0-12-182056-5.
- ^ T. Po, G. Steger, V. Rosenbaum, J. Kaper, and D. Riesner (1987). "Double-stranded cucumovirus associated RNA 5: experimental analysis of necrogenic and non-necrogenic variants by temperature-gradient gel electrophoresis". Nucleic Acids Research. 15 (13). ss. 5069-5083. doi:10.1093/nar/15.13.5069.
- ^ Breslauer, K.J.; ve diğerleri. (1986). "Predicting DNA Duplex Stability from the Base Sequence". Proc. Natl. Acad. Sci. USA. Cilt 83. ss. 3746-3750. doi:10.1073/pnas.83.11.3746. (pdf) 24 Temmuz 2021 tarihinde Wayback Machine sitesinde arşivlendi.
- ^ Rychlik, W. et al. (1990) Nucleic Acids Res. 18, 6409-6412.
- ^ Owczarzy R., Vallone P.M., Gallo F.J., Paner T.M., Lane M.J. and Benight A.S (1997). "Predicting sequence-dependent melting stability of short duplex DNA oligomers". Biopolymers. Cilt 44. ss. 217-239. doi:10.1002/(SICI)1097-0282(1997)44:3<217::AID-BIP3>3.0.CO;2-Y. (pdf) 11 Aralık 2012 tarihinde Archive.is sitesinde arşivlendi
Kaynakça
Ayrıca bakınız
- DNA
- Denatürasyon
- Hibritleşme
- PCR
- Ergime noktası
- Primer (Tm hesaplaması için)
Dış bağlantılar
- OligoAnalyzer'da Tm hesaplamaları24 Mart 2009 tarihinde Wayback Machine sitesinde arşivlendi.
- Tm hesaplaması21 Haziran 2009 tarihinde Wayback Machine sitesinde arşivlendi. - (bioPHP.org).
- https://web.archive.org/web/20080516194508/http://www.promega.com/biomath/calc11.htm#disc
- Invitrogen Tm hesaplaması28 Eylül 2007 tarihinde Wayback Machine sitesinde arşivlendi.
- En yakın komşu yöntemi ile Tm hesaplaması için AnnHyb açık kaynak yazılımı26 Nisan 2009 tarihinde Wayback Machine sitesinde arşivlendi.
- Sigma-aldrich teknik notları29 Nisan 2008 tarihinde Wayback Machine sitesinde arşivlendi. (İngilizce)
- Primer3 hesaplaması18 Haziran 2010 tarihinde Wayback Machine sitesinde arşivlendi.