Hidrokarbon, sadece karbon ve hidrojen atomlarından oluşan kimyasal bileşiklerin genel adı.

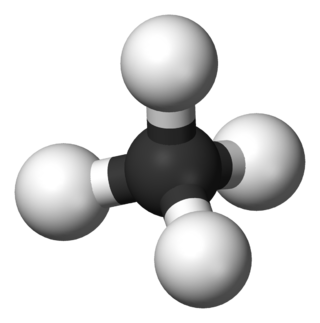
Alkanlar, (diğer bir deyişle Parafinler) sadece karbon (C) ve hidrojen (H) elementlerinin bulunduğu ve bu elementlerin birbirleriyle tekli bağ yaptığı doymuş alifatik organik bileşiklerin genel ismidir. Alkanlar birbirlerini 1 karbon ve 2 hidrojen ile takip eden bir homolog seri oluştururlar. Örneğin tek karbonlu metan, CH4 formülüne sahipken, çift karbonlu etan C2H6 kapalı formülüne sahiptir. Alkanlarda tüm atomlar tekli bağlarla birbirlerine bağlandığı ve Karbon atomunu bağlayabileceği en fazla Hidrojen atomunu bağladığından dolayı doymuş bileşikler kategorisine girerler. Doymuş hidrokarbonlardan olan alkanlar, CnH2n+2 n=1,2,3,.... genel formülüne sahiptir. Burada n'in 3 veya 3'ten büyük olması hâlinde sikloalkan denilen halkalı yapılar oluşabilmektedirler.

Porfirin, dört metiliden (-CH=) köprüsüyle birbirine bağlı dört pirol halkasından ibaret olan porfin halka sistemi ihtiva eden molekül sistemidir. Bu molekül inorganik yapının organik yani canlı yaşamına nasıl evrildiğinin anlaşılmasını da sağlamıştır. Yani dünyadaki yaşam cansızdan canlıya bu madde ile geçmiştir. Doğada genellikle I ve III numaralı porfirin şekli bulunur. Porfirinlerdeki yan grupların dizilimi simetrik olduğu takdirde Tip I; asimetrik olduğu takdirde Tip III izomerleri oluşur. Tip III izomerleri en fazla bulunan ve önemli olan tiptir.

Alkenler yapılarında en az bir tane karbon-karbon (C=C) çift bağı içeren organik bileşiklerdir. Alkenlerin yapısında karbon-karbon çift bağı bulunduğundan ve bu karbonların yapabileceği en fazla hidrojenle bağ yapmamış olduğundan alkenler doymamış bileşikler kategorisine girerler. Alkenlerin yapısında sadece bir karbon-karbon çift bağının bulunması durumunda homolog seriler oluşturur. Bu homolog serilerin genel formülü CnH2n şeklindedir. Burada n-in en az 2 olma şartı vardır. Aşağıda en basit alken olan eten, yaygın ismiyle etilenin, çeşitli modellemelerle çizilmiş şekillerinin yanı sıra alkenlerin çeşitli şekillerdeki yazılış şekilleri de bulunmaktadır.
Kimya ve biyokimyada, yağ asidi, genelde uzun, alifatik kuyruklu bir karboksilik asittir. Uzun karboksilik yağ asitlerinden 4 karbonlu ve daha uzun zincirlileri yağ asidi olarak sayılır; doğal yağları (trigliseritleri) oluşturan yağ asitlerinden söz ederken ise bunların en az 8 karbonlu olduğu varsayılabilir. Çoğu doğal yağ asitlerinin çift sayılı karbon atomu vardır, çünkü bunların biyolojik sentezlerinde iki karbon atomlu asetat kullanılır.

Organik kimya, organik bileşiklerin ve organik maddelerin yani karbon atomlarını içeren çeşitli formlardaki maddelerin yapısını, özelliklerini ve reaksiyonların bilimsel çalışmasını içeren, kimyanın bir alt dalıdır. Yapının incelenmesi yapısal formüllerini belirler. Özelliklerin incelenmesi, fiziksel ve kimyasal özellikleri ve davranışlarını anlamak için kimyasal reaktivitenin değerlendirilmesidir. Organik reaksiyonların incelenmesi doğal ürünlerin, ilaçların ve polimerlerin kimyasal sentezini ve bireysel organik moleküllerin laboratuvarda ve teorik çalışma yoluyla incelenmesidir.
Hidrojenasyon, bir kimyasal reaksiyon sınıfıdır ve organik bileşiklere hidrojen (H2) eklenmesi işlemidir. Hidrojenasyon, özellikle doymamış organik bileşikler (alkenler, alkinler, ketonlar ve nitriller ) için önemli bir reaksiyondur. Genellikle basınç altında katalizörler yardımı ile direkt hidrojen eklemesi ile gerçekleştirilir. Hidrojenasyon için en klasik örnek, alkenlerdeki doymamış karbon kimyasal bağına bir hidrojenin ekleyerek, alkeni alkana dönüştürmektir. İlaç ve petrokimya endüstrisinde çok değişik uygulamaları vardır. Bu kimyasal işlemin tersi dehidrojenasyondur. Alkenlere hidrojenin katılması sonucunda Alkanlar oluşur. Alkankar sadece karbon-karbon tekli bağlara sahiptirler. Bu tepkimede katalizör kullanıldığından katalitik hidrojenleme olarak da adlandırılır. Alkenlere hidrojen katılma tepkimeleri ekzotermik tepkimeler olup oda sıcaklığında katalizörsüz tepkime gerçekleşmez. Burada katalizör kullanılarak tepkimenin oda sıcaklığında gerçekleşmesi sağlanır. Yalnız katalizörün etkisi bununla sınırlı kalmıyor. Kullanılan katalizör elde edilecek olan ürünün cis-Alkan ya da trans-Alkan olmasını etkilemektedir. Eğer kullanılan katalizör heterojen bir katalizör ise, (bir parça nikel, platin, paladyum) yani çözelti içerisinde heterojen olarak karışıyorsa katılan her iki hidrojen atomu alkenin aynı tarafına eklenir ve böylece cis-Alkan oluşur. Şayet bu katalizör çözelti içerisinde homojen olarak yayılan bir katalkizörse bu seferde trans-Alkan oluşmuş olacak.

Organik bileşikler, molekülleri karbon içeren kalabalık kimyasal bileşikler sınıfındandır. Aşağıda sunulan tarihsel nedenlerden dolayı, bu bileşiklerin küçük bir kısmı, örneğin karbonatlar, basit karbon oksitleri ve siyanürlerin yanı sıra, karbon allotropları inorganik kabul edilir. "Organik" ve "inorganik" karbon bileşikleri arasındaki ayrım "kimyanın geniş alanını düzenlemek için yararlı olsa da, çoğunlukla rastgeledir".

Kimyada esterler, bir hidroksil grubundaki hidrojen atomunun bir organik grup (bu metinde R' olarak gösterilecektir) ile yer değiştirmiş olduğu organik bileşiklerdir. Hidrojenin bir H+ iyonu olarak ayrışabileceği -OH grubu olan bu tür asitlere oksijen asidi denir.

Aminler, amonyaktaki bir veya daha fazla hidrojen atomunun organik radikaller ile değiştirilmesi yöntemiyle türetilmiş organik bileşikler ve fonksiyonel gruplardır. Yapısal olarak aminler amonyağa benzerler, ama bir veya daha fazla hidrojen atomu, alkil veya aril gibi organik sübstitüentlerle yer değiştirmiştir. Bu kuralın önemli bir istisnası RC(O)NR2 tipi bileşiklerdir (C(O) karbonil grubuna karşılık gelir), bunlara amin yerine amid denir. Amidler ve aminlerin yapıları ve özellikleri farklı olduğu için bu ayrım kimyasal olarak önemlidir. Adlandırma açısında biraz akıl karıştırıcı olan bir nokta, bir aminin N-H grubunun N-M (M= metal) ile değişmesi hâlinde buna da amid denmesidir. Örneğin (CH3)2NLi, lityum dimetilamid'dir.
Karışım, birden fazla maddenin kimyasal özellikleri değişmeyecek şekilde bir araya gelmesiyle oluşan madde topluluğudur. Saf maddeler element ve bileşiklerden oluşur. Fakat maddelerin çoğu ne tek bir elementtir ne de tek bir bileşiktir. Maddelerin çoğu saf madde olmayan karışımlardır. Karışımlar homojen, kolloid ve heterojen olmak üzere üçe ayrılır.
Şeker kimyasında bir anomer, özel bir epimer tipidir. Halkalı halde bir sakkaritin stereoizomeridir, yalnızca hemiasetal karbonunun biçimi farklıdır. Eğer anomerik karbonun hidroksil grubu  grubuna göre trans konumundaysa, şeker bir alfa anomeridir. Eğer anomerik karbonun hidroksil grubu
grubuna göre trans konumundaysa, şeker bir alfa anomeridir. Eğer anomerik karbonun hidroksil grubu  grubuna göre cis konumundaysa, şeker bir beta anomeridir.
grubuna göre cis konumundaysa, şeker bir beta anomeridir.

İnorganik, organik olmayan anlamına gelir. Biyolojide su, mineral, asit, baz, tuzlar gibi canlıların yapısında bulunan ancak canlı olmayan veya bir canlı tarafından üretilmemiş bileşiklerdir. Kimyada inorganik bileşikler, sıklıkla karbon taşımayan moleküllerdir. Bunlara örnek olarak da, anyonlar veya katyonlar olarak sınıflandırılan çeşitli iyonik bileşikler ile kovalent bileşikleri verilebilir. Birçoğu iyonlardan meydana gelmiş olsa da kovalent bağlı inorganik bileşikler de bulunur. Karbon disülfür, karbonmonoksit ve siyanürler gibi karbon bileşikleri inorganik olarak kabul edilir.

Eterler, iki organik kısmın bir oksijen atomu üzerinden birbirine bağ yapmış organik moleküllerdir. Eterlerin genel formülü R-O-R' şeklindedir. Buradaki R ve R' aynı olabileceği gibi farklı organik kısımlar da olabilirler.
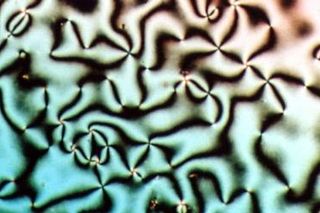
Sıvı kristaller, sıvıların ve katı kristallerin özellikleri arasında özelliklere sahip olan kimyasal maddelerdir. Örneğin, bir sıvı kristal (SK) bir sıvı gibi akar ama molekülleri bir kristalinki gibi yönlüdür. Çeşitli sıvı kristal fazları vardır, bunlar çiftkırılım gibi optik özellikleri ile tanımlanırlar. Polarize ışıkla mikroskop altında incelendiklerinde farklı sıvı kristal fazları farklı kristal dokular gösterir. Bunlar SK moleküllerinin farklı yönlü oldukları bölgelere karşılık gelir. Bu bölgelerin her birinde moleküller aynı doğrultuya sahiptirler. SK malzemeler her zaman sıvı kristallik göstermezler.
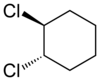
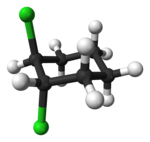
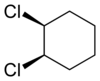
Stereoizomerler, aynı sırayla birbirine bağlanmış aynı atomlardan oluşan, fakat değişik 3-boyutlu yapıları olan bileşiklerdir. Stereoizomer çiftleri, bazen kimyasal reaksiyonlarda ayırt edilemezler, fakat molekülün fiziksel özelliği incelenerek ayırt edilebilirler.
Halojenleme veya halojenasyon, bir bileşiğe bir veya daha fazla halojenin katılmasını gerektiren kimyasal bir reaksiyondur. Alkenler, klor ve brom gibi halojenlerle, nükleofillik özelliği göstermeyen çözücüler içerisinde hızla tepkimeye girerler ve dihalojenleri oluştururlar. Bromun katılması daha kolay takip edilebilmektedir. Çünkü kırmızı-kahve rengi olan Brom çözeltisinin rengi ortadan kalkar. Bu yöntem özellikle çift bağların varlığını kanıtlamada kullanılır. Burada alken doymamış bir molekül olduğu için bromla tepkimeye girerken, alkanlar ise ortamda radikal bir çözelti olmadığı sürece tepkime vermez. Genel itibarıyla bu tepkimeler ya oda sıcaklığında ya da soğuk bir ortamda inert halojen çözücülerinin (CCl4) varlığında uygulanır.
Organik reaksiyonlar, organik maddelerin tepkimelerine verilen genel addır.

Kimyada, oktahedral moleküler geometri, bir oktahedronun köşelerini tanımlayan, merkezi bir atom etrafında simetrik olarak düzenlenmiş altı atomlu bileşiklerin veya atom gruplarının veya ligandların şeklini tanımlar. Oktahedronun sekiz yüzü vardır, dolayısıyla octa ön ekini alır. Oktahedron, Platonik katılardan biridir, ancak oktahedral moleküller tipik olarak merkezlerinde bir atom içerir ve ligand atomları arasında bağ yoktur. Mükemmel bir oktahedron Oh nokta grubuna aittir. Oktahedral bileşiklerin örnekleri arasında kükürt hekzaflorür SF6 ve molibden hekzakarbonil Mo (CO)6 gösterilebilir. "Oktahedral" terimi, kimyagerler tarafından, merkezi atoma olan bağların geometrisine odaklanarak ve ligandların kendi aralarındaki farklılıkları dikkate almadan biraz gevşek bir şekilde kullanılır. Örneğin, N-H bağlarının oryantasyonu nedeniyle matematiksel anlamda oktahedral olmayan [Co(NH3)6]3+, oktahedral olarak adlandırılır.

Maleik Asit veya cis-bütendioik Asit olarak da bilinir, HO2CCH=CHCO2H formüllü, dibazik özellikte doymamış organik asit. Başlıca poliesterlerin yapımında kullanılan bu asitten fumarik asit gibi pek çok kimyasal bileşiğin üretiminde de yararlanılır. Maleik asit ve bunun susuz türevi sanayide benzenin bir katalizör eşliğinde yükseltgenmesiyle üretilir.