
Hidrojen, sembolü H, atom numarası 1 olan kimyasal bir element. Standart sıcaklık ve basınç altında renksiz, kokusuz, metalik olmayan, tatsız, oldukça yanıcı ve H2 olarak bulunan bir diatomik gazdır. 1,00794 g/mol'lük atomik kütlesi ile tüm elementler arasında en hafif olanıdır. Periyodik cetvelin sol üst köşesinde yer alır. Hidrojenin adı, Yunancada "su oluşturan" anlamına gelen ὑδρογόνο'dan (idrogono) kelimesinden gelir.

Sodyum, periyodik cetvelde Na simgesi ile gösterilen ve atom numarası 11 olan element. Sodyum yumuşak ve kaygan bir metal olup alkali metaller grubuna aittir. Doğal bileşiklerin içinde bol miktarda bulunur. Yüksek oranda reaktiftir, sarı bir alevle yanar, su ile şiddetli reaksiyon verir ve havada hızla oksitlenir. Dolayısıyla, vazelin, gazyağı gibi hava ve su ile temasını kesecek bir ortamda saklanması gerekir.

Potasyum, bir kimyasal elementtir. Simgesi K ve atom numarası 19 dur. Potasyum adını izole edildiği Potas olarak da bilinen potasyum karbonattan almıştır. Potasyum yumuşak, gümüş-beyaz renkli alkali bir metaldir. Doğada deniz suyunda ve pek çok mineralde diğer elementlere bağlı olarak bulunur. Havada hızla oksitlenir ve suya karşı da çok aktiftir. Potasyum, pek çok açıdan sodyuma kimyasal olarak benzese de yaşayan organizmalarda, özellikle de hayvan hücrelerinde, sodyumdan farklı muamele görür. Kandaki seviyesinin düşük olmasına hipokalemi, yüksek olmasına hiperkalemi denir.

Baryum (Yunanca'da βαρυς = ağır), sembolü Ba olan kimyasal bir elementtir. Ağır manasına gelen "barys" kelimesinden türemiştir. İngilizcede Barite ağırlık yoğunluk manasında kullanılmaktadır. Baryum elementinin atom numarası 56 olup Periyodik tablonun 6. sırasında ve 2. grubunda bulunur. 2. grupta bulunması özelliğinden dolayı Baryum bir toprak alkali metalidir. Baryum ilk defa 1774 yılında İsveçli kimyacı Carl Wilhelm Sheele tarafından tanımlanmıştır. Baryum element halinde beyaz-gri metalik rengindedir fakat yüksek reaktivitelikten dolayı element halinde bulunmaz. Baryum'un hemen hemen bütün bileşikleri ise zehirlidir. Metalik Ba yakıldığında elma yeşili bir renk verir. Metalik halde saklanması çok zordur. Aktif bir element olduğu için su, hava ve asitlerle kolayca reaksiyon verir. Toprak alkali grup içerisinde doğada en yaygın bulunan element Kalsiyum(Ca)dur. Bu sınıftaki metallerin özellikleri birbirine benzemesine karşın bilhassa Kalsiyum, Stronsiyum, Baryum diğerlerinden ayrılır. Bu üç element adi derecede suyu ayrıştırarak Hidrojen açığa çıkarır ve Hidroksit(OH) oluştururlar. Bu Hidroksitler de ısıtıldığında su kaybederek Oksit haline dönmektedirler. Karbonatları ısı karşısında kolay ayrışmasına karşın Baryum Karbonat (BaCO3) en zor ayrışanıdır. Sülfatları suda hemen hemen hiç erimez.

Gümüş, elementlerin periyodik tablosunda simgesi Ag olan, beyaz, parlak, değerli bir metalik element. Atom numarası 47, atom ağırlığı 107,87 gramdır. Erime noktası 961,9 °C, kaynama noktası 1950 °C ve özgül ağırlığı da 10,5 g/cm³'tür. Çoğu bileşiklerinde +1 değerliklidir. Günümüzde Dünya'da 55 yıllık gümüş rezervi kaldığı tahmin ediliyor. Yeni gümüş rezervleri keşfedilmezse 2078 yılında Dünya'daki gümüş rezervlerinin tükenebileceği tahmin ediliyor. En çok gümüş üretimi yapan ülkeler Meksika, Çin, Peru Şili ve Avustralya'dır.

Niyobyum, sembolü Nb, atom numarası 41 olan kimyasal elementtir.

Çinko, sembolü Zn, atom numarası 30 olan kimyasal bir elementtir. Oda sıcaklığında hafif kırılgan bir metaldir ve oksidasyon giderildiğinde parlak gri bir görünüme kavuşur. Periyodik tablonun 12. (IIB) grubunun ilk elementidir. Bazı açılardan çinko kimyasal olarak magnezyuma benzer: her iki element de yalnızca bir normal oksidasyon durumu (+2) gösterir ve Zn2+ ve Mg2+ iyonları benzer boyuttadır. Çinko, Dünya kabuğundaki en bol bulunan 24. element olup beş kararlı izotopu vardır. En yaygın çinko cevheri, bir çinko sülfür minerali olan sfalerittir.

Molibden, periyodik cetvelde atom numarası 42 ve simgesi Mo olan elementtir..
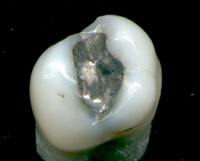
Amalgam, çok kuvvetli çözme özelliğine sahip olan cıvanın, metaller ile yaptığı karışım (alaşım).

Tungsten veya diğer adıyla volfram, atom numarası 74, atom ağırlığı 183,85 olan ve kimyasal simgesi W ile gösterilen, yoğunluğu 19,3 g/cm³ olan, 3482 °C'de eriyebilen kimyasal bir elementtir. Çok sert, ağır, çelik gri ya da beyaz renkte geçiş metallerinden biri olan tungsten, wolframite ve scheelite içeren madenlerde bulunur. Tungsten, sağlam fiziksel yapısı ve yüksek erime sıcaklığı olan önemli bir maddedir. Erime sıcaklığı en yüksek olan metaldir. Saf haliyle bazı elektronik uygulamalarda kullanılır, ancak çoğunlukla bileşik ya da alaşım olarak, diğer metallerin işlenmesi veya madencilik gibi uygulamalarda malzeme dayanımı gerektiren ekipmanlarda, ampullerin lamba tellerinde, X ışını cihazlarında ve uzay teknolojisi yüksek performans alaşımlarında kullanılır.

Plütonyum, 1940 yılında Glenn T. Seaborg, Edwin M. McMillan, J. W. Kennedy ve A. C. Wahlby tarafından 152 cm'lik siklotron içerisindeki uranyumun döteryum ile bombardımanı sonucunda elde edilmiştir.

Bizmut sembolü Bi ve atom numarası 83 olan kimyasal elementtir. 15. grupta, 6. periyotta yer alan bir metaldir. Pentavalent geçiş metalidir ve azot grubundadır; aynı gruptaki arsenik ve antimon ile benzerlik gösterir. Her ne kadar önemli ticari cevherler sülfür ve oksit formlarından oluşsa da elementer bizmut doğal olarak ortaya çıkabilir. Serbest element formundaki kurşunun %86'sı yoğunluğuna sahiptir. Yeni üretildiğinde gümüşi beyaz renkli ve kırılgan bir metaldir ancak yüzey oksidasyonu ona birçok renkte yanardöner renkler verebilir. Bizmut en doğal diyamanyetik elementtir ve metaller arasındaki en az termal iletkenlik değerlerinden birine sahiptir.

Avrupyum ve Avrupyum (Eu), atom numarası 63 olan kimyasal elementtir.
Alaşım, bir metal elementin en az bir başka element ile birleşmesiyle oluşan homojen karışımıdır. Elde edilen malzeme yine metal karakterli malzeme olur. Alaşımlar karışıma giren metallerin özelliklerinden farklı özellikler gösterirler. En bilinen alaşımlara; tunç (bakır-kalay), pirinç (bakır-çinko), lehim (kalay-kurşun) ve cıva alaşımları olan amalgamlar örnek verilebilir. Alaşımlar, uygulamaların gerektirdiği fiziksel özelliklere sahip malzemeler üretilmesinde yaygın olarak kullanılır.

Cıva(II) fülminat, Hg(CNO)2, primer patlayıcıdır. Sürtünme ve şoka çok duyarlı olduğundan dolayı özellikle diğer patlayıcıları patlatmak için kullanılan darbeli kapsüller ve patlatma kapsüllerinde bir tetikleyici olarak kullanılır.

Simyasal simgeler, aslında simyanın bir parçası olarak tasarlandı ve 18. yüzyıla kadar bazı elementleri ve bazı bileşikleri göstermek için kullanıldı.

UV kurutma işlemi ultraviyole (morötesi) ışınlar ve görünür ışınlar yardımı ile polimer yapıdaki UV Mürekkeplerinin fotokimyasal çapraz reaksiyona girerek kurutulması işlemidir. UV Kurutma işlemi; baskı, kaplama ve dekorasyon alanında anahtar bir üründür. Bu işlem düşük ısılarda, yüksek hızda ve solvent işlemine göre buharlaşma yolu ile değil polimerizasyon tekniği ile kurumaktadır. İlk olarak 1960'larda ortaya çıkan teknoloji, artırılarak birçok üretim endüstrisinde kullanılmaya başlanmıştır.

Organoklorürler, klorlu hidrokarbonlar ya da klorokarbonlar, en az bir adet kovalent bağlanmış klor atomuna sahip organik bileşiklerdir. En basit örnekleri kloroalkanlardır. Organoklorürlerin geniş bir yapısal çeşitliliğe sahip olması onların farklı kimyasal özelliklere, isimlere ve kullanım alanlarına sahip olmasına sebep olmuştur. Bazı organoklorürlerin yararlı olmasına karşın bazıları zehirli ve çevreye zararlıdır.
Dumas moleküler ağırlık belirleme yöntemi, bilinmeyen bir maddenin moleküler ağırlığını belirlemek için geçmişte kullanılan bir prosedürdü. Dumas yöntemi, oda sıcaklığında sıvı olan uçucu organik maddelerin moleküler ağırlıklarını belirlemek için uygundur.
Metal zehirlenmesi veya metal toksisitesi; belirli metallerin belirli biçim ve dozlarda yaşam üzerindeki zehirleyici etkisidir. Birtakım metaller, zehirli çözünür bileşikler oluşturduklarında zehirlidir. Birtakım metallerin biyolojik bir rolü yoktur, başka bir deyişle yaşam için zorunlu (esansiyel) minerallerden değildir veya belirli bir türevdeyken zehirlidir. Söz konusu metalin kurşun olması durumunda, kurşunun ölçülebilir herhangi bir miktarının sağlık üzerinde olumsuz etkileri olabilir. Metal zehirlenmesinin genellikle ağır metaller ile anlamdaş olduğu düşünülür, ancak berilyum ve lityum gibi daha hafif metaller de belirli durumlarda zehirli olabilir. Bütün ağır metaller özellikle zehirli değildir ve demir gibi bazı metaller canlıda çok önemli bir yer tutar. Metal zehirlenmesinin tanımı, anormal derecede yüksek dozlarda zehirli etki gösteren eser elementleri de kapsayabilir. Metal zehirlenmesinin tedavisi için şelasyon tedavisi bir seçenek olabilir; bu yöntem, metalleri vücuttan uzaklaştırmak için şelasyon ajanlarının uygulanmasını içine alan bir tekniktir.

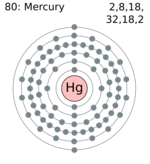



![]() Wikimedia Commons'ta Mercury ile ilgili çoklu ortam belgeleri bulunur
Wikimedia Commons'ta Mercury ile ilgili çoklu ortam belgeleri bulunur 















