Su, Dünya üzerinde bol miktarda bulunan ve tüm canlıların yaşaması için vazgeçilmez olan, kokusuz ve tatsız bir kimyasal bileşiktir. Sıklıkla renksiz olarak tanımlanmasına rağmen kızıl dalga boylarında ışığı hafifçe emmesi nedeniyle mavi bir renge sahiptir.

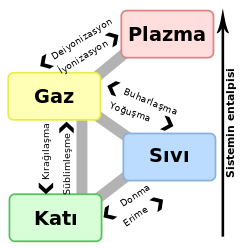
Hâl değişimi, bir maddenin moleküller arası potansiyel enerjisinin ısı alarak ya da vererek değişmesi sonucu meydana gelen olay.

Kimyasal tepkime ya da kimyasal reaksiyon, iki veya daha fazla maddenin birbiri ile etkileşmesi sonucu kendi özelliklerini kaybederek yeni özellikte maddeler oluşturmasıdır. Kimyasal olay ve kimyasal değişme kavramlarıyla eşanlamlıdır. Kimyasal reaksiyonların test edilmesi için Periyodik tablo metalleri ile aside koyarak yapılabilir.

Erime noktası, kristal ve saf olan bir maddenin katı halden sıvı hale geçtiği belirli bir sıcaklıktır. Bu sıcaklığa o maddenin erime noktası denir. Bütün kristal yapıya sahip saf maddelerin erime noktasında, yani katı halden sıvı hale geçene kadar, sıcaklığı sabit kalır. Ancak tamamen sıvı hale geçtikten sonra sıcaklığı yükselir. Saf kristal cisimlerin erime noktası ile donma noktası arasında sıcaklık farkı yoktur. Mesela saf su, 0 °C de donar. Fakat saf olmayan maddelerin, yani karışımların donma ve erime noktaları farklıdır.

Entalpi, maddenin yapısında depoladığı her türden enerjilerin toplamıdır. H ile simgelenir. Bir mol maddede depolanmış enerjiye o maddenin molar entalpisi denir.

Katı, maddenin atomları arasındaki boşluğun en az olduğu halidir. "Katı" olarak adlandırılan bu haldeki maddelerin kütlesi, hacmi ve şekli belirlidir. Bir dış etkiye maruz kalmadıkça değişmez. Sıvıların aksine katılar akışkan değildir. Fiziksel yollarla, diğer üç hal olan sıvı, gaz ve plazmaya dönüştürülebilirler. Altın demir gibi madenler katı maddelere örnektir. Ayrıca katı maddeler atomlarının en yavaş hareket edebildiği haldir. Doğa'da amorf veya kristal yapıda bulunurlar. Amorf katılar maddenin taneciklerinin düzensiz olma durumudur. Kristal katılar ise de maddenin taneciklerinin düzenli olma durumudur. Kristal katılar da aralarında 4'e ayrılır.
Kalori, atmosfer basıncında 1 gram suyun sıcaklığını 1 °C artırmak için gerekli olan enerji miktarıdır.

Çözelti ya da solüsyon, iki ya da daha fazla maddenin herhangi bir oranda bir araya gelerek oluşturdukları homojen karışımdır.
Buğu, istim veya islim ; fizik, kimya ve mühendislikte, buharlaşmış suyu ifade eder. 100 santigrat derece civarındaki sıcaklıkta ve standart atmosferik basınçtaki buhar, saftır, saydam gaz haldedir ve sıvı haldeki sudan 1600 kat daha hacimlidir. Buhar doğal olarak suyun kaynama noktasından daha sıcaktır. Daha yüksek sıcaklıklardaki buhara genelde kızdırılmış buhar denir.

Su buharı, normal şartlar altında sıvı hâlde bulunan suyun gaz hâlidir. Su, her sıcaklıkta buharlaşabildiği için havada her zaman su buharı bulunur. Buharlaşma su yüzeyinden meydana gelir. Suyun su buharı hâline gelmesine buharlaşma denir. Su buharının tekrar su hâline geçmesine de yoğunlaşma denir. Atmosferde bulunan su buharı ani yoğunlaşmalar yaşarsa yağmur yağar, yoğunlaşma ortamı aniden ve aşırı soğursa su buharı direkt yoğunlaşma olmadan katı hâle geçer. Buna da kırağılaşma denir.
- Buharlaşma, bir hâl değişimidir. Sıvıların ısı alarak gaz hâline geçmesidir.
- Kolonya kokusunun odaya yayılması (difüzyon),
- Bulutların oluşması, buharlaşmaya en iyi örnektir.
- Buharlaşma her sıcaklıkta olabilir.
- Sıcaklık arttığında maddelerde genleşme olur.
- Su buharı suyun en düzensiz hâlidir. Bu hâlde su moleküllerinin hızı en fazladır.
Süblimleşme, katı maddelerin ısıtılınca, ara bir hâl olan sıvı hâle geçmeden doğrudan gaz hâle geçmesi. Süblimleşme endotermik faz değişimidir. Faz diyagramındaki üçlü noktanın altında gerçekleşir. Süblimleşme'nin tersine ise kırağılaşma denir.
Kaynama, sıvının buhar basıncının dış basınca eşit olduğunda, sıvının her yerinden gaz kabarcıklarının çıkması. Saf maddelerin sabit atmosfer basıncı altında kaynama noktası sabittir. Kaynama süresi boyunca maddenin sıcaklığı değişmez. Sıvı bir maddenin içine uçucu olmayan bir çözünen eklenirse çözeltinin kaynama noktası yükselir. Çözünen madde miktarı arttıkça kaynama noktası yükselecektir. Aynı ortamdaki bütün sıvıların kaynama anındaki buhar basınçları eşittir, ancak maddelerin kaynama sıcaklığı maddenin cinsine, saflığına ve ortamın dış basıncına bağlıdır. Kaynama sıcaklığı maddeler için ayırt edici bir özelliktir.

Yoğunlaşma veya yoğuşma, maddenin fiziksel halinin gaz fazından sıvı faza değişimi ve buharlaşmanın tersidir. En sık su döngüsü anlamında kullanılır. Atmosfer içinde bir sıvı veya katı bir yüzey veya Yoğunlaşma bulutu ile temas ettiğinde, su buharının sıvı suya değişmesi olarak da tanımlanabilir. Doğrudan gaz fazdan katı faza geçiş gerçekleştiğinde, değişime kırağılaşma denir.

Buharlaşma, bir sıvının gaz fazına geçerken yüzeyinde oluşan buharlaşma türüdür. Çevreleyen gazdaki buharlaşan maddenin yüksek konsantrasyonu, örneğin çevredeki nemin suyun buharlaşma hızını etkilemesiyle buharlaşma yavaşlar.

Fiziksel bilimlerde faz; bir malzemenin fiziksel özelliklerinin her noktasında aynı olduğu bölgedir/alandır. Fiziksel özelliklerinin örneklerinden üç tanesi, yoğunluk içermesi, mıknatıslanma ve kimyasal bileşimi indeksi. Basit bir açıklama ile bir faz fiziksel olarak ayrı, kimyasal olarak yeknesak ve (genellikle) mekanik ayrılabilir malzemeli bir bölge olmasıdır. Bir cam kavanoz buz ve sudan oluşan bir sistemde, buz küpleri birinci faz, su ikinci faz ve suyun üstünde bulunan nem ise üçüncü fazdır. Cam kavanoz ise başka bir ayrı aşamasıdır. Faz terimi bazen maddenin hali olarak eş anlamlı bir şekilde kullanılabilir. Ancak bir maddenin aynı halde çok sayıda karışmayan fazı olabilir. Ayrıca, faz terimi bazen bir faz diyagramı için üzerinde sınır ile basınç ve sıcaklık gibi durum değişkenler açısından sınırı çizilmiş denge durumunda bir dizi oluşturmak için kullanılır. Faz sınırları gibi katı veya başka bir kristal yapısından daha ince değişikliğine sıvıdan bir değişiklik olarak maddenin organizasyon değişiklikleriyle ilgili olduğundan bu son kullanım durumuna eş anlamlısı olarak "faz" kullanımına benzer. Ancak, madde ve faz diyagramı kullanımların hali yukarıda verilen ve amaçlanan anlam terim kullanıldığı bağlamdan kısmen tespit edilmelidir resmi tanımı ile orantılı değildir. Fazın çeşitleri Farklı fazlar, gaz, sıvı, katı, plazma veya Bose-Einstein yoğuşma ürünü olarak maddenin farklı durumlar olarak tarif edilebilir. Maddenin katı ve sıvı formda diğer haller arasındaki faydalı mezofazlar.

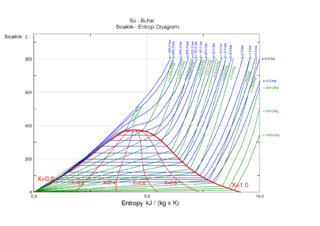
Trouton yasası çoğu sıvının kaynama noktası sırasındaki buharlaşma entropisinin yaklaşık 85-88 J K−1 mol−1, olduğunu söyler Bu buharlaşma entropisi buharlaşma entalpisinin kaynama sıcaklığına oranıdır. Yasa ismini Frederick Thomas Trouton'dan almıştır.
Buharlaşma entropisi sıvının entropisinin buharlaşma sebebiyle olan artışıdır. Her zaman pozitif olmakla beraber, bu artışın sebebi düzensizliğin sıvı halden görece daha fazla hacim kaplayan gaz hale geçerken artıyor olmasıdır. standart basınçta Po = 1 bar, buharlaşma enerjisi DSoVap şeklinde gösterilir ve birimi J mol−1 K−1.

Leidenfrost etkisi, 1756 yılında Alman bilim adamı Johann Gottlob Leidenfrost tarafından keşfedilen ve A Tract About Some Qualities of Common Water kitabında konu edindiği, sıvıların yüzeyleri ile temas ettiklerinde oluşan ve sıvının hızlı buharlaşması sonucu yüzeyde bir buhar tabakası oluşmasına neden olan fiziksel bir fenomendir. Bu buhar tabakası, sıvının yüzeyinde oluşan bir yalıtkan tabaka görevi görür ve bu sayede sıvının yüzeyine dokunulduğunda, sıvı damlacıklarının hoplayarak hareket etmesine ve hatta bazen buharlaşarak tamamen kaybolmasına neden olur. Bu etki, sıvıların yüzeylerindeki buharlaşma hızı ile sıvının sıcaklığı, yüzey gerilimi ve çevresel koşullar gibi faktörlerden etkilenir.

Buhar basıncı ya da buhar denge basıncı; kapalı bir sistemdeki katı ya da sıvı fazdaki maddelerin termodinamik denge durumundaki buharının, belirli bir sıcaklıkta uyguladığı basınçtır. Bu değer, buharlaşma hızıyla doğru orantılıdır. Normal sıcaklıklarda görece yüksek buhar basıncına sahip maddeler, uçucu olarak tanımlanır.
Hissedilir ısı, bir cisim veya termodinamik sistem tarafından değiştirilen ısı olup, burada ısı değişimi cismin veya sistemin sıcaklığını ve cismin veya sistemin bazı makroskobik değişkenlerini değiştirir, ancak hacim veya basınç gibi cisim veya sistemin diğer bazı makroskopik değişkenlerini değiştirmeden bırakır.