Sodyum, periyodik cetvelde Na simgesi ile gösterilen ve atom numarası 11 olan element. Sodyum yumuşak ve kaygan bir metal olup alkali metaller grubuna aittir. Doğal bileşiklerin içinde bol miktarda bulunur. Yüksek oranda reaktiftir, sarı bir alevle yanar, su ile şiddetli reaksiyon verir ve havada hızla oksitlenir. Dolayısıyla, vazelin, gazyağı gibi hava ve su ile temasını kesecek bir ortamda saklanması gerekir.

Asit, pH derecesi 7'den düşük olup, değişen oranlarda yakıcı ve/veya aşındırıcı özelliğe sahip olan ve oldukça geniş kullanım alanına sahip kimyasal maddelere verilen isimdir. Suda çözündüklerinde hidrojen iyonu derişimini artırarak çözeltiyi asidik yapar. Mavi turnusol kâğıdının rengini kırmızıya çeviren asitlere eski Türkçede hamız veya ekşit denir.

Brom (Br), Antoine Balard tarafından 1826 yılında keşfedilen halojen ametal. Yunanca dışkı gibi koku anlamındaki bromosdan gelmiştir.

Kimyasal bileşik, kimyasal bağlarla bir arada tutulan birden fazla kimyasal elementin atomlarını içeren birçok özdeş molekülden oluşan kimyasal maddedir. Dolayısıyla tek bir elementin atomlarından oluşan bir molekül bileşik değildir. Bir bileşik, diğer maddelerle etkileşimi içerebilen kimyasal reaksiyonla farklı bir maddeye dönüştürülebilir. Bu süreçte atomlar arasındaki bağlar kırılabilir ve/veya yeni bağlar oluşabilir.

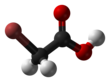
Karboksilik asitler karboksil grubu olan organik asitlerdir, -C(=O)OH formülüne sahiptirler, bu genelde -COOH veya CO2H olarak da yazılır. Karboksilik asitler Bronsted asitleridir, yani proton vericileridir. Karboksilik asitlerin tuz ve anyonlarına karboksilat denir. Karboksilik asitler, esterlerle fonsiyonel grup izomeridirler. Karboksilik asitlerin en basit dizisi alkanoik asitlerdir, R-COOH formülüyle gösterilirler, R bir hidrojen atomu veya bir alkil grubuna karşılık gelir. Bileşiklerde birden fazla karboksilik asit grubu bulunabilir.

Kimyada esterler, bir hidroksil grubundaki hidrojen atomunun bir organik grup (bu metinde R' olarak gösterilecektir) ile yer değiştirmiş olduğu organik bileşiklerdir. Hidrojenin bir H+ iyonu olarak ayrışabileceği -OH grubu olan bu tür asitlere oksijen asidi denir.

Asetik asit veya etanoik asit CH3COOH formüllü bir organik asittir, sirkeye ekşi tadını ve keskin kokusunu vermesiyle bilinir. Bu yüzden halk arasında sirke ruhu veya sirke asidi şeklinde de adlandırılır. Karboksilik asitlerin en küçüklerindendir (en küçük olan formik asittir). Doğada karbonhidratların yükseltgenmesiyle oluşur. Sanayide asetik asit hem biyolojik yolla hem de sentetik yolla imal edilir. Tuz ve esterine asetat denir. Suda tamamen çözünür.

MeOAc, asetik asit metil esteri ya da metil etanoat olarak da bilinen Metil asetat, formülü CH3COOCH3 olan karboksilli bir esterdir. Karakteristik olarak, bazı tutkallar ve oje çıkarıcıların hoş kokusunu anımsatan yanıcı bir sıvıdır. Metil asetat, zayıf polar ve lipofilik özellikte olduğundan bazen bir solvent olarak kullanılmaktadır. Ancak yakın akrabası olan etil asetat daha az toksik ve suda daha az çözündüğünden dolayı çok daha yaygın kullanılan bir çözücüdür. Metil asetat, oda sıcaklığındaki su içerisinde %25 kadar bir çözünürlüğe sahiptir. Yüksek sıcaklıktaki suda, çözünürlüğü çok daha yüksektir. Metil asetat kuvvetli sulu bazlar ya da sulu asitlerin mevcudiyetinde kararlı değildir.

İyot monoklorür ICl formülü ile gösterilen bir interhalojen bileşiktir. Oda sıcaklığına yakın eriyen kırmızı-kahverengi renge sahip bir kimyasal bileşiktir. İyot ve klorun elektronegatifliği arasındaki fark nedeniyle, ICl oldukça kutupsaldır ve I+ kaynağı olarak davranır.

Asetik anhidrit veya etanoik anhidrit  formüllü bir kimyasal bileşiktir. Organik sentezde çokça kullanılan bir bileşiktir. Güçlü bir asetik asit kokusuna sahiptir, asetik asitin havadaki nemle tepkimesi ile oluşur. Asetat iyonu verdiğinden asetik anhidrit asetilasyon tepkimelerinde kullanılabileceği gibi morfinin asetilasyonunda kullanılır, eroin (diasetilmorfin) üretiminde kullanılır.
formüllü bir kimyasal bileşiktir. Organik sentezde çokça kullanılan bir bileşiktir. Güçlü bir asetik asit kokusuna sahiptir, asetik asitin havadaki nemle tepkimesi ile oluşur. Asetat iyonu verdiğinden asetik anhidrit asetilasyon tepkimelerinde kullanılabileceği gibi morfinin asetilasyonunda kullanılır, eroin (diasetilmorfin) üretiminde kullanılır.

Hidrojen bromür, HBr formülüne sahip iki atomlu moleküldür. Renksiz bir bileşik ve bir hidrojen halojenürdür. Hidrobromik asit, su içinde bir HBr çözeltisidir. Hem HBr'nin susuz hem de sulu çözeltileri, bromür bileşiklerinin hazırlanmasında ortak reaktiflerdir.
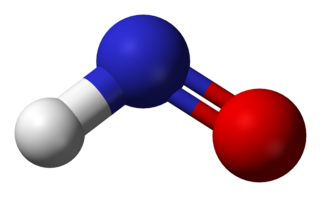
Nitroksil veya azanon, HNO kimyasal bileşiğidir. Gaz fazında iyi bilinmektedir. NO− İndirgenmiş nitrik oksit formudur (NO) ve dioksijen ile izoelektroniktir. Nitroksil, bir reaksiyon ara maddesi olarak oluşturulabilir.
Florosülfürik asit (IUPAC adı: sülfürofloridik asit), HSO3F kimyasal formüllü bir inorganik bileşiktir. Ticarî olarak temin edilebilen en güçlü asitlerden biridir. HSO3F formülü sülfürik asit (H2SO4) ile ilişkisini vurgulamaktadır. HSO3F tetrahedral bir moleküldür. Ticari numuneler genellikle sarı olmasına rağmen renksiz bir sıvıdır.
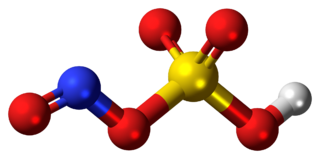
Nitrozilsülfürik asit, NOHSO4 formülüne sahip bir kimyasal bileşiktir. Endüstriyel olarak kaprolaktam üretiminde kullanılan renksiz bir katıdır. Daha önce sülfürik asit üretmek için öncü oda işleminin bir parçasıydı. Bileşik, sülfürik asit ve nitröz asidin karışık anhidritidir.
2-Nitrobenzoik asit, C6H4(NO2)CO2H formülüne sahip bir organik bileşiktir. 2-Nitrotoluenin nitrik asit oksidasyonu ile hazırlanır.
4-Nitrobenzoik asit C6H4(NO2)CO2H formül üne sahip bir organik bileşiktir. Soluk sarı renkli bir katıdır. Anestezik prokain ve folik asitin öncül maddesi olan 4-nitrobenzoil klorür kimyasal bileşiğinin öncül maddesidir. Aynı zamanda, 4-aminobenzoik asit kimyasal bileşiğinin öncül maddesidir.
Retrosentetik analiz, organik sentezlerin planlanmasındaki problemleri çözmek için kullanılan bir tekniktir. Bu, reaktiflerle herhangi bir potansiyel reaktivite/etkileşimden bağımsız olarak bir hedef molekülün daha basit öncü yapılara dönüştürülmesiyle elde edilir. Her bir öncü malzeme aynı yöntem kullanılarak incelenir. Bu prosedür, basit veya ticari olarak temin edilebilen yapılara ulaşılıncaya kadar tekrar edilir. Bu daha basit/ticari olarak temin edilebilen bileşikler, hedef molekülün bir sentezini oluşturmak için kullanılabilir. Elias James Corey bu kavramı The Logic of Chemical Synthesis kitabında resmileştirdi.

İzoamil asetat veya izopentil asetat, izoamil alkol ve asetik asit esteri olan organik bileşik. Bu renksiz, yağımsı sıvı muz veya armuda benzeyen bir kokuya sahiptir parfümlerde koku, gıdalarda muz tadı vermek için kullanılır ayrıca sanayide çözücü olarak kullanılır. Bu madde doğal muzda az miktardada olsa oluşur muzların esans yağının bir parçasıdır. Toksititesi az ve az miktarlarda bile hissedildiğinden gaz maskelerini test etmek için kullanılabilir.

Organik kimyada, bir açil klorür (veya asit klorür) -COCl fonksiyonel grubuna sahip bir organik bileşiktir. Formülleri genellikle RCOCl şeklinde yazılır. Burada R bir yan zincirdir. Karboksilik asitlerin reaktif türevleridir. Açil klorürün özgün bir örneği, CH3COCl, asetil klorür'dür. Açil klorürler açil halojenürlerin en önemli alt kümesidir.
Kimyada, bir kimyasal bileşiğin ampirik formülü, bir bileşikte bulunan atomların en basit tam sayı oranıdır. Bu kavramın basit bir örneği, kükürt monoksitin veya SO'nun ampirik formülü, S2O2 formüllü disülfür dioksitin ampirik formülü (SO) ile aynıdır. Bu nedenle, hem kükürt hem de oksijenin bileşikleri olan kükürt monoksit ve disülfür dioksit aynı ampirik formüle sahiptir.