
Deoksiriboz nükleik asit veya kısaca DNA, tüm organizmaların ve bazı virüslerin canlılık işlevleri ve biyolojik gelişmeleri için gerekli olan genetik talimatları taşıyan bir nükleik asittir. DNA'nın başlıca rolü bilgiyi uzun süre saklamasıdır. Protein ve RNA gibi hücrenin diğer bileşenlerinin inşası için gerekli olan bilgileri içermesinden dolayı DNA; bir kalıp, şablon veya reçeteye benzetilir. Bu genetik bilgileri içeren DNA parçaları gen olarak adlandırılır. Bazı DNA dizilerinin yapısal işlevleri vardır, diğerleri ise bu genetik bilginin ne şekilde kullanılacağının düzenlenmesine yararlar.

Amino asitler, proteinleri oluşturan temel yapı taşlarıdır.
Enzimler, kataliz yapan biyomoleküllerdir. Neredeyse tüm enzimler protein yapılıdır. Enzim tepkimelerinde, bu sürece giren moleküllere substrat denir ve enzim bunları farklı moleküllere, ürünlere dönüştürür. Bir canlı hücredeki tepkimelerin neredeyse tamamı yeterince hızlı olabilmek için enzimlere gerek duyar. Enzimler substratları için son derece seçici oldukları için ve pek çok olası tepkimeden sadece birkaçını hızlandırdıklarından dolayı, bir hücredeki enzimlerin kümesi o hücrede hangi metabolik yolakların bulunduğunu belirler.
Nitrik asit, HNO3 kimyasal formülüne sahip oldukça aşındırıcı bir inorganik asittir. Kezzap olarak da bilinir. Saf hâldeki bileşik renksizdir. Ancak uzun süre bekleyen eski asitler azot oksitleri ve suya ayrışması nedeniyle sarı renge dönebilme özelliğindedirler. Piyasada bulunan nitrik asitlerin çoğu % 68'lik bir konsantrasyona sahiptir. Çözelti, %86'dan fazla HNO3 içerdiğinde, dumanlı nitrik asit olarak adlandırılır. Mevcut azot dioksit miktarına bağlı olarak, dumanlı nitrik asit ayrıca %86’nın üzerindeki konsantrasyonlarda kırmızı dumanlı nitrik asit veya %95’in üzerindeki konsantrasyonlarda beyaz dumanlı nitrik asit olarak tanımlanır.

Şelasyon iki veya çok dişli bir kimyasal ligandın iyonik bir substrata bağlanması veya komplekslenmesidir. Bu ligandlar ki genelde organik bileşiklerdir, şelatör veya şelat ajanı olarak adlandırılır. Şelatörler, ASTM-A-380 standardına göre, "belli metal iyonları ile suda çözünür kompleksler oluşturan kimyasallardır, bu sayede iyonu etkinsizleştirerek onun başka elementler veya iyonlarla tepkitmeyerek, çökelek veya tortu oluşmamasını sağlar". Ligand, substrat ile birleşip bir şelat kompleksi meydana getirir. Bu terim, metal iyonunu şelatördeki iki veya daha çok atomla bağlandığı kompleksler için kullanılır. Literatürde metal iyonu tutan bağların sayısına değinmek için dişlilik terimi kullanılır, örneğin yandaki resimde görülen EDTA altı dişli bir şelatördür.
Dönüş, polipeptit zincirinin doğrultusunu ters çevirdiği bir protein ikincil yapı elemanıdır.

Enzim kinetiği enzimler tarafından katalizlenen kimyasal reaksiyonların bilimidir. Enzim kinetiğinde reaksiyon hızı ölçülür ve reaksiyon şartlarını değiştirmenin etkisi araştırılır. Bir enzimin kinetiğinin bu şekilde çalışılması enzimin katalitik mekanizmasını, metabolizmadaki rolünü, aktivitesinin nasıl kontrol edildiğini ve bir ilaç veya zehrin enzimi nasıl inhibe edebileceğini ortaya koyabilir.

Enzim ölçümleri enzim aktivitesini ölçmek için laboratuvar yöntemleridir. Enzim kinetiğini ve enzim inhibisyonunun araştırılması için önemlidirler.

Frederick Sanger, İngiliz biyokimyager. 1958 ve 1980 yıllarında 2 kez Nobel Kimya Ödülü kazanmıştır. 1958 yılında "proteinlerin, özellikle de insülinin yapısı üzerine çalışmaları için" Nobel Kimya Ödülü kazanmıştır ve bu ödülü aynı kategoride 2 kez kazanan tek kişidir. 1980 yılında da "nükleik asitlerdeki baz dizilerinin belirlenmesiyle ilgili katkıları nedeniyle" Walter Gilbert ile birlikte bu ödülü kazanmıştır. Aynı yıl ayrıca Paul Berg, "nükleik asitlerin, özellikle de rekombinant DNA'nın biyokimyası üzerine temel çalışmaları için" ödülü kazanan diğer isim olmuştur.
Stanford Moore, Amerikalı biyokimyacı. 1972 yılında, Christian B. Anfinsen ve William H. Stein ile birlikte, ribonükleaz molekülünün kimyasal yapısı ve katalitik aktivitesi arasındaki bağı anlamamıza katkıları ve ribonükleazlar üzerine çalışmaları için Nobel Kimya Ödülü'nü kazanmıştır.
Protein çözümleme veya protein assay, bir solüsyondaki çözünmüş formdaki bir proteinin konsantrasyonunu ölçmek için kullanılan analitik spektroskopik bir yöntemdir. Öznel bir yöntemdir, yani örneğin ölçülen bir proteindeki amino asidin bileşimine bağımlıdır. Bu yöntem Marion M. Bradford tarafından bulunduğundan Bradford protein çözümlemesi olarak da bilinir.

MeOAc, asetik asit metil esteri ya da metil etanoat olarak da bilinen Metil asetat, formülü CH3COOCH3 olan karboksilli bir esterdir. Karakteristik olarak, bazı tutkallar ve oje çıkarıcıların hoş kokusunu anımsatan yanıcı bir sıvıdır. Metil asetat, zayıf polar ve lipofilik özellikte olduğundan bazen bir solvent olarak kullanılmaktadır. Ancak yakın akrabası olan etil asetat daha az toksik ve suda daha az çözündüğünden dolayı çok daha yaygın kullanılan bir çözücüdür. Metil asetat, oda sıcaklığındaki su içerisinde %25 kadar bir çözünürlüğe sahiptir. Yüksek sıcaklıktaki suda, çözünürlüğü çok daha yüksektir. Metil asetat kuvvetli sulu bazlar ya da sulu asitlerin mevcudiyetinde kararlı değildir.
Lowry protein tahlil solusyondaki total protein konsantrasyonunu belirlemek için uygulanan biyokimyasal tahlil. Total protein konsantrasyonu numune solusyonundaki renk değişikliği ile gözlemlenir. Bu renk değişimi protein konsantrasyonuna oranla değişir ve kolorimetrik tekniklerle ölçülebilir. Tahlilin ismini 1940' larda tahlil reaktifini geliştiren biyokimyager Oliver H. Lowry' den alır. Lowry' nin bu tekniği açıklayan 1951'de yayınladığı makale, 300,000 kere ile bilim literatüründeki en çok atıf yapılan makaledir.
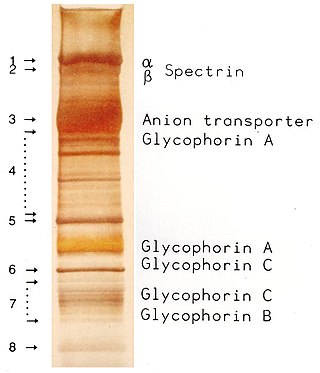
SDS-PAGE bir poliakrilamid jel elektroforez varyantı olan ve biyokimyada karışımlardaki yüklü molekülleri elektrik alan varlığında moleküler kütlelerine göre ayıran analitik bir metottur. Sodyum dodesil sülfat (SDS) molekülleri proteinlerin izolasyon ve tanımlanmasına yardım ederler.

Kapiler elektroforez kütle spektrometrisi (CE-MS), kapiler elektroforezin sıvı ayırma işleminin kütle spektrometresi ile birleşiminden oluşan bir analitik kimya tekniğidir. CE-MS, tek bir analizde yüksek ayırma verimliliği ve moleküler kütle bilgisi sağlamak için hem CE hem de MS'nin avantajlarını birleştirir. Yüksek çözünürlük ve hassasiyete sahiptir, minimum hacim gerektirir ve yüksek hızda analiz yapabilir. İyonlar tipik olarak elektrosprey iyonizasyonla oluşturulur ancak matris destekli lazer desorpsiyon/iyonizasyonu veya diğer iyonizasyon teknikleriyle de oluşturulabilirler. Proteomik ve biyomoleküllerin kantitatif analizinde ve klinik tıpta kullanılmaktadır. 1987'deki tanıtımından bu yana, yeni gelişmeler ve uygulamalar CE-MS'i güçlü bir ayırma ve tanımlama tekniği haline getirmiştir.

Organik kimyada peptit sentezi, birden fazla amino asidin peptit bağları olarak da bilinen amid bağları ile bağlandığı peptit bileşiklerinin üretimidir. Peptitler, bir amino asidin karboksil grubunun diğerinin amino grubuna yoğunlaşma reaksiyonu ile kimyasal olarak sentezlenir. Koruma grubu stratejileri genellikle çeşitli amino asit yan zincirleri ile istenmeyen yan reaksiyonları önlemek için gereklidir. Kimyasal peptit sentezi, en yaygın olarak peptitin karboksil ucunda (C-terminali) başlar ve amino terminaline (N-terminali) doğru ilerler. Canlı organizmalardaki protein biyosentezi ters yönde gerçekleşir.
Biyosentez, substratların canlı organizmalarda daha karmaşık ürünlere dönüştürüldüğü çok aşamalı, enzim katalizli bir süreçtir. Biyosentezde basit bileşikler modifiye edilir, diğer bileşiklere dönüştürülür veya makromoleküller oluşturmak üzere birleştirilir. Bu süreç genellikle metabolik yollardan oluşur. Bu biyosentetik yollardan bazıları tek bir hücresel organel içinde yer alırken diğerleri birden fazla hücresel organel içinde yer alan enzimleri içerir. Bu biyosentetik yolların örnekleri arasında çift katlı lipit katmanının bileşenlerinin ve nükleotidlerin üretimi yer alır. Biyosentez genellikle anabolizma ile eş anlamlıdır ve bazı durumlarda birbirinin yerine kullanılır.

Aminoasil-tRNA, aynı kökenli amino asidinin kimyasal olarak bağlı (yüklü) olduğu tRNA'dır. aa-tRNA, belirli uzama faktörleriyle birlikte, translasyon sırasında üretilen polipeptit zincirine dahil edilmek üzere amino asidi ribozoma iletir.
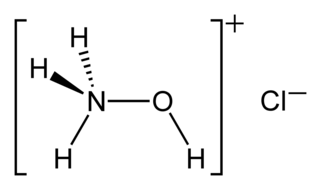
Hidroksilamonyum klorür, formülü [NH3OH]Cl olan, hidroksilaminin hidroklorür asit tuzudur. Nitratlaştırma ve anaerobik amonyum oksidasyonunda ara ürün olarak ortaya çıkar.

Lizozomal asit fosfataz, insanların 11. kromozomunda yer alan ACP2 geni tarafından kodlanan bir enzimdir.













