Benzen
| |||
 | |||
| Adlandırmalar | |||
|---|---|---|---|
Tercih edilen IUPAC adı Benzene | |||
Diğer adlar | |||
| Tanımlayıcılar | |||
CAS numarası | |||
3D model (JSmol) | |||
| ChEBI | |||
| ChEMBL | |||
| ChemSpider | |||
| ECHA InfoCard | 100.000.685 | ||
| EC Numarası |
| ||
| KEGG | |||
PubChem CID | |||
| RTECS numarası |
| ||
| UNII | |||
CompTox Bilgi Panosu (EPA) | |||
| |||
| |||
| Özellikler | |||
| Kimyasal formül | C6H6 | ||
| Molekül kütlesi | 78,11 g mol−1 | ||
| Görünüm | renksiz sıvı | ||
| Koku | benzin gibi | ||
| Yoğunluk | 0,876520 g/cm3 | ||
| Erime noktası | 5,53 °C (41,95 °F; 278,68 K) | ||
| Kaynama noktası | 80,1 °C (176,2 °F; 353,2 K) | ||
| Çözünürlük (su içinde) | 1,53 g/L (0 °C) 1,81 g/L (9 °C) 1,79 g/L (15 °C)[2][3][4] 1,84 g/L (30 °C) 2,26 g/L (61 °C) 3,94 g/L (100 °C) 21,7 g/kg (200 °C, 6.5 MPa) 17,8 g/kg (200 °C, 40 MPa)[5] | ||
| Çözünürlük | Alkol, CHCl3, CCl4, dietil eter, aseton, asetik asit içinde çözünür[5] | ||
| Çözünürlük (etandiol içinde) | 5.83 g/100 g (20 °C) 6.61 g/100 g (40 °C) 7.61 g/100 g (60 °C)[5] | ||
| Çözünürlük (etanol içinde) | 20 °C, solution in water: 1.2 mL/L (20% v/v)[7] | ||
| Çözünürlük (aseton içinde) | 20 °C, solution in water: 7.69 mL/L (38.46% v/v) 49.4 mL/L (62.5% v/v)[7] | ||
| Çözünürlük (dietilen glikol içinde) | 52 g/100 g (20 °C)[5] | ||
| log P | 2.13 | ||
| Buhar basıncı | 12.7 kPa (25 °C) 24.4 kPa (40 °C) 181 kPa (100 °C)[6] | ||
| UV-vis (λmax) | 255 nm | ||
| 54.8·10ÿ6 cm3/mol | |||
| Kırınım dizimi (nD) | 1.5011 (20 °C) 1.4948 (30 °C)[5] | ||
| Akmazlık | 0.7528 cP (10 °C) 0.6076 cP (25 °C) 0.4965 cP (40 °C) 0.3075 cP (80 °C) | ||
| Yapı | |||
| Trigonal düzlem | |||
| Dipol momenti | 0 D | ||
| Termokimya | |||
Isı sığası (C) | 134.8 J/mol·K | ||
Standart molar entropi (S⦵298) | 173.26 J/mol·K[6] | ||
Standart formasyon entalpisi (ΔfH⦵298) | 48.7 kJ/mol | ||
Standart yanma entalpisi (ΔcH⦵298) | 3267.6 kJ/mol[6] | ||
| Tehlikeler | |||
| İş sağlığı ve güvenliği (OHS/OSH): | |||
| Ana tehlikeler | potansiyel meslekî kanserojen, yanıcı | ||
| GHS etiketleme sistemi: | |||
| Piktogramlar |    [8] [8] | ||
| İşaret sözcüğü | Tehlike | ||
| Tehlike ifadeleri | H225, H304, H315, H319, H340, H350, H372[8] | ||
| Önlem ifadeleri | P201, P210, P301+P310, P305+P351+P338, P308+P313, P331[8] | ||
| NFPA 704 (yangın karosu) | |||
| Parlama noktası | 11,63 °C (52,93 °F; 284,78 K) | ||
Kendiliğinden tutuşma sıcaklığı | 49.778 °C (89.632 °F; 50.051 K) | ||
| Patlama sınırları | 1.2-7.8% | ||
| Öldürücü doz veya konsantrasyon (LD, LC): | |||
LD50 (medyan doz) | 930 mg/kg (sıçan, oral) | ||
LCLo (yayınlanan en düşük) | 44.000 ppm (tavşan, 30 dakika) 44.923 ppm (köpek) 52.308 ppm (kedi) 20.000 ppm (insan, 5 dakika)[10] | ||
| NIOSH ABD maruz kalma limitleri: | |||
| PEL (izin verilen) | TWA 1 ppm, ST 5 ppm[9] | ||
| REL (tavsiye edilen) | Ca TWA 0.1 ppm ST 1 ppm[9] | ||
| IDLH (anında tehlike) | 500 ppm[9] | ||
| Güvenlik bilgi formu (SDS) | HMDB | ||
| Benzeyen bileşikler | |||
Benzeyen bileşikler | Toluen Borazin | ||
| Aksi belirtilmediği sürece madde verileri, Standart sıcaklık ve basınç koşullarında belirtilir (25 °C [77 °F], 100 kPa). | |||

Benzen, aren veya aromatik hidrokarbonlar olarak adlandırılan organik bileşikler sınıfının en basit üyesidir. Renksiz, yanıcı, kaynama noktası 80,1 °C, erime noktası 5,5 °C olan bir sıvıdır. Moleküler formülü C6H6'dır. Benzen, endüstriyel bakımdan değerli olduğu gibi yapısı bakımından da kimya çalışmalarında önemlidir. Kan hücrelerini öldürme etkisi olduğundan kanser yapıcı bileşikler arasına girer.
Tarihçe
Eskiden balina yağının ısı etkisiyle bozunmasından elde edilen gaz, basınçla evlere gönderilir ve aydınlatmada kullanılırdı. Benzen, 1825 yılında Michael Faraday tarafından bu gazdan kalan yağımsı bölümde keşfedildi. Yaklaşık sekiz sene sonra başka araştırmacılar aynı maddeyi benzoik asidin kireçle yükseltgenmesinden elde ettiler. 1845'te August Wilhelm von Hofmann benzen diye adlandırdığı aynı maddeyi elde etmek için kömür katranı kullandı.
Yapısı

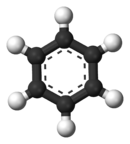
Benzen, karbon atomlarının düzlemde düzgün altıgen biçiminde dizilmesinden oluşur. Karbonlar arasındaki uzaklık 1397 angströmdür. Köşelerde bulunan her karbon atomuna bir hidrojen atomu bağlıdır. Ayrıca değişik yapılarda bulunabilir. Uzaysal olarak şekli düzlemsel şekline oranla oldukça farklıdır.
Tepkime yeteneği
Benzenin yapısının kimyasal tepkimelere ne şekilde bir tepki gösterdiği üzerine yapılan çalışmaların, organik kimya teorilerinin gelişmesinde önemi büyük olmuştur. Hidrojen atomlarının karbon atomlarına oranının böyle düşük olduğu bir bileşikten umulan katılma tepkimeleri benzende olmaz. Benzenin gösterdiği tipik tepkimelerden biri, substitüsyon tepkimeleridir. Bu tepkime bir aktif grubun benzendeki bir hidrojeni çıkarıp onun yerine geçmesi şeklinde gerçekleşir. Bu davranışı izah etmek altı elektronun (benzende varmış gibi gösterilen 3 tane çifte bağdan ileri gelen) belli karbonlarda değil bütün benzen karbonlarına dağılmış olduğunu düşünmekle mümkün olur. Elektronların böyle dağılmış olması (belli karbonlarda olmaması) molekülün kararlı olmasını sağlar ve yine bu molekülün fiziksel ve kimyasal özelliklerini belirler.
Elde edilişi

Benzenin yer değiştirme tepkimeleri oldukça önemlidir. Çünkü, aromatik bileşiklerin pek çoğu bu tepkimelerle oluşturulur. II. Dünya Savaşı'ndan önce benzenin önemli kaynağı maden kömüründen elde edilen katran idi. İkinci Dünya Savaşı sırasında benzen ve bununla ilgili aromatik hidrokarbonlara (toluen, ksilen vb.) duyulan büyük gereksinimle başka kaynaklar aranmaya başlandı. Bugün Amerika'da üretilen benzenin %75'i petrolden olup toluenin (C6H5-CH3) ya da toluen içeren petrolün dealkilizasyonu işlemi ile yapılmaktadır. Bu işlem hidrojen kullanmayı, yüksek sıcaklığı, basıncı ve bir de katalizörü gerektirmektedir. İkinci bir yöntem naftence zengin petrolün hidrojenlerinin yüksek sıcaklık ve basınçta koparılmasıdır (dehidrojenasyon). Benzen, fenolün indirgenmesiyle ve asetilenin trimerleşmesiyle elde edilir.
Kullanılışı
Benzen, sanayide plastik imalinde kullanılan stiren ve fenolün sentezinde başlangıç maddesi olarak, naylon bileşenlerinde, sentetik deterjan üretiminde kullanılır. Uçak benzinlerinde, boya yapmaya yarayan anilinin başlangıç maddesi ve böcek öldürücü olarak da benzen kullanılır. Benzen aynı zamanda iyi bir çözücüdür.
Benzenin türevleri
Anilin, DDT, DDB, Maleik anhidrit, Stiren, Diklorobenzen ve Siklohekzan gibi kimyasal maddelerin üretiminde yer almaktadır. Benzenden türeyen aromatik hidrokarbonlar sınıfı genel olarak arenler ismiyle tanınır.
Benzenin özellikleri
Benzenin özellikleri şunlardır:[12]
- Renksiz ve saydamdır.
- Işığı kıran, hoş kokulu, alevlenebilen bir sıvıdır.
- Benzende bulunan bütün karbonlar sp2 hibritleşmesi yapmıştır.
- Kaynama noktası 80,1 °C ve erime noktası 5,5 °C'dir.
- Moleküler formülü C6H6'dır.
- Kan hücrelerini öldürme etkisi olduğundan kanser yapan bileşikler arasına girer.
- Alkenlerin katılma tepkimesi verdiği koşullarda benzen, katılma tepkimesine girmez.
- Kararlı bir yapıda olduğu için tepkimeye girmeye çok istekli değildir ancak yüksek sıcaklık ve basıncın etkisiyle hidrojen ile çok yavaş bir şekilde tepkime verebilmektedir.
- Yer değiştirme tepkimesi verebilmektedirler. Böylece benzene Cl, NO2, CH3 gibi moleküller bağlanabilir.
Ayrıca bakınız
Kaynakça
- ^ Nomenclature of Organic Chemistry : IUPAC Recommendations and Preferred Adlar 2013 (Blue Book). Cambridge: The Royal Society of Chemistry. 2014. ss. 138, 577. doi:10.1039/9781849733069-FP001. ISBN 978-0-85404-182-4.
- ^ Arnold, D.; Plank, C.; Erickson, E.; Pike, F. (1958). "Solubility of Benzene in Water". Industrial & Engineering Chemistry Chemical & Engineering Data Series. 3 (2). ss. 253-256. doi:10.1021/i460004a016.
- ^ Breslow, R.; Guo, T. (1990). "Surface tension measurements show that chaotropic salting-in denaturants are not just water-structure breakers". Proceedings of the National Academy of Sciences of the United States of America. 87 (1). ss. 167-9. Bibcode:1990PNAS...87..167B. doi:10.1073/pnas.87.1.167. PMC 53221 $2. PMID 2153285.
- ^ Coker, A. Kayode; Ludwig, Ernest E. (2007). Ludwig's Applied Process Design for Chemical And Petrochemical Plants. 1. Elsevier. s. 114. ISBN 0-7506-7766-X. Erişim tarihi: 31 Mayıs 2012.
- ^ a b c d e http://chemister.ru/Database/properties-en.php?dbid 13 Eylül 2016 tarihinde Wayback Machine sitesinde arşivlendi. = 1&id = 644
- ^ a b c "Benzene". 23 Eylül 2008 tarihinde kaynağından arşivlendi. Erişim tarihi: 18 Mayıs 2023.
- ^ a b Atherton Seidell; William F. Linke (1952). = k2e5AAAAIAAJ Solubilities of Inorganic and Organic Bileşikler: A Compilation of Solubility Data from the Periodical Literature. Supplement
|url=değerini kontrol edin (yardım). Van Nostrand. - ^ a b c Sigma-Aldrich Co., Benzene 1 Aralık 2016 tarihinde Wayback Machine sitesinde arşivlendi.. Retrieved on 2014-05-29.
- ^ a b c NIOSH Pocket Guide to Chemical Hazards. "#0049". National Institute for Occupational Safety and Health (NIOSH).
- ^ 71432.html "Benzen"
|url=değerini kontrol edin (yardım). Immediately Dangerous to Life or Health Concentrations (IDLH). Ulusal İş Sağlığı ve Güvenliği Enstitüsü (NIOSH). - ^ August Kekulé: Ueber einige Condensationsproducte des Aldehyds, Liebigs Ann. Chem. 1872, 162 (1), S. 77–124; DOI:10.1002/jlac.18721620110.
- ^ "Aromatik Bileşikler - Benzen ve Benzen Türevleri". Bikifi. 29 Ağustos 2018. 19 Eylül 2020 tarihinde kaynağından arşivlendi. Erişim tarihi: 24 Şubat 2023.