
Sodyum, periyodik cetvelde Na simgesi ile gösterilen ve atom numarası 11 olan element. Sodyum yumuşak ve kaygan bir metal olup alkali metaller grubuna aittir. Doğal bileşiklerin içinde bol miktarda bulunur. Yüksek oranda reaktiftir, sarı bir alevle yanar, su ile şiddetli reaksiyon verir ve havada hızla oksitlenir. Dolayısıyla, vazelin, gazyağı gibi hava ve su ile temasını kesecek bir ortamda saklanması gerekir.

Baryum (Yunanca'da βαρυς = ağır), sembolü Ba olan kimyasal bir elementtir. Ağır manasına gelen "barys" kelimesinden türemiştir. İngilizcede Barite ağırlık yoğunluk manasında kullanılmaktadır. Baryum elementinin atom numarası 56 olup Periyodik tablonun 6. sırasında ve 2. grubunda bulunur. 2. grupta bulunması özelliğinden dolayı Baryum bir toprak alkali metalidir. Baryum ilk defa 1774 yılında İsveçli kimyacı Carl Wilhelm Sheele tarafından tanımlanmıştır. Baryum element halinde beyaz-gri metalik rengindedir fakat yüksek reaktivitelikten dolayı element halinde bulunmaz. Baryum'un hemen hemen bütün bileşikleri ise zehirlidir. Metalik Ba yakıldığında elma yeşili bir renk verir. Metalik halde saklanması çok zordur. Aktif bir element olduğu için su, hava ve asitlerle kolayca reaksiyon verir. Toprak alkali grup içerisinde doğada en yaygın bulunan element Kalsiyum(Ca)dur. Bu sınıftaki metallerin özellikleri birbirine benzemesine karşın bilhassa Kalsiyum, Stronsiyum, Baryum diğerlerinden ayrılır. Bu üç element adi derecede suyu ayrıştırarak Hidrojen açığa çıkarır ve Hidroksit(OH) oluştururlar. Bu Hidroksitler de ısıtıldığında su kaybederek Oksit haline dönmektedirler. Karbonatları ısı karşısında kolay ayrışmasına karşın Baryum Karbonat (BaCO3) en zor ayrışanıdır. Sülfatları suda hemen hemen hiç erimez.

İnorganik, organik olmayan anlamına gelir. Biyolojide su, mineral, asit, baz, tuzlar gibi canlıların yapısında bulunan ancak canlı olmayan veya bir canlı tarafından üretilmemiş bileşiklerdir. Kimyada inorganik bileşikler, sıklıkla karbon taşımayan moleküllerdir. Bunlara örnek olarak da, anyonlar veya katyonlar olarak sınıflandırılan çeşitli iyonik bileşikler ile kovalent bileşikleri verilebilir. Birçoğu iyonlardan meydana gelmiş olsa da kovalent bağlı inorganik bileşikler de bulunur. Karbon disülfür, karbonmonoksit ve siyanürler gibi karbon bileşikleri inorganik olarak kabul edilir.

Klorik asit (HClO3), klorun bir oksoasiti ve klorat tuzlarının formal öncülüdür. Güçlü bir asit (pKa ≈1) ve oksitleyici ajandır.

Klorat, ClO3− formülüyle gösterilen bir kimyasal kök. Bileşiklerinde daima bir adet elektron alır. Kloratlar, genel olarak klorik asitin tuzu olarak bilinirler. Klorat molekülleri organik bileşikleri kolayca oksitleyeceğinden dolayı kimyasal olarak zararlı bir maddedir. Geçmişte birçok patlayıcı ve havai fişekte kullanılan klorat, günümüzde yerini perklorata bırakmıştır.

Perklorat, ClO4− formülüyle göserilen bir kimyasal kök. Bileşiklerinde daima bir adet elektron alır. Perkloratlar perklorik asitin tuzlarıdır. Perkloratlar özellikle tıpta tiroid bezleri tedavisinde kullanılmaktadır. Bunlarla beraber, hava yastığı ve havai fişek gibi bazı ürünlerde perkloratlara rastlanmaktadır.

Sodyum perklorat formülü NaClO4 olan bir kimyasal bileşiktir. Perklorik asitin sodyum tuzu olan bu bileşik diğer perkloratlar gibi kuvvetli bir oksitleyicidir. Sodyum perkloratın çözünürlüğü diğer perklorat tuzları içinde en yüksek olanıdır. Beyaz kristallerden oluşan ve higroskopik özellikte olan sodyum perklorat suda ve alkolde oldukça çok çözünür. Genellikle monohidrat form halinde bulunur ve rombik bir kristal yapısına sahiptir. Standart oluşum entalpisi −382.75 kJ mol−1 dir.
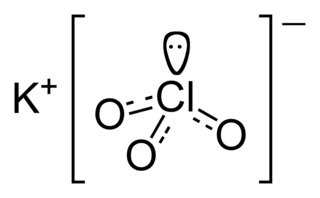
Potasyum klorat formülü KClO3 olan bir kimyasal bileşiktir. Klorik asitin potasyum tuzu olan bu bileşik diğer kloratlar gibi kuvvetli bir oksitleyicidir.

Sodyum klorat NaClO3 kimyasal formülüne sahip bir inorganik bileşiktir. Suda kolayca çözünür, beyaz kristal bir tozdur. Higroskopiktir. Sodyum klorat 300 °C’nin üzerinde ayrışarak oksijen ve sodyum klorür ortaya çıkar. Özellikle, çok parlak kâğıt imal etmek için ağartma hamurundaki uygulamalara yönelik olarak yılda birkaç yüz milyon ton üretilmektedir.

Baryum perklorat formülü Ba(ClO4)2 olan bir kimyasal bileşiktir. Perklorik asitin baryum tuzu olan bu bileşik diğer perkloratlar gibi kuvvetli bir oksitleyicidir. Piroteknik endüstrisinde kullanılır.
Magnezyum klorat formülü Mg(ClO3)2 olan bir kimyasal bileşiktir. Klorik asitin magnezyum tuzu olan bu bileşik diğer kloratlar gibi kuvvetli bir oksitleyicidir.
Bilinen inorganik ve organometalik bileşiklerin elementlere göre sıralanmış listesidir. Sıralama elementlerin kısaltmalarının alfabetik sırasına göredir.

Yükseltgen madde bir yükseltgenme-indirgenme (redoks) reaksiyonunda başka bir türden bir elektron alan element ya da bileşiktir. Yükseltgen maddelerin elektron kazandıklarından dolayı indirgendikleri söylenebilir.
Kalsiyum klorat kimyasal formülü Ca(ClO3)2 olan bir bileşiktir. Klorik asitin kalsiyum tuzudur. Potasyum klorat gibi, kuvvetli bir oksitleyici olan bu bileşik, piroteknik formülasyonlarda kullanılabilir. Kalsiyum klorat kuvvetle ısıtıldığında ya da organik madde gibi indirgeyici maddelerle karıştırıldığında patlayabilir.

Kloril florür ClO2F formüllü bileşik. Sıklıkla klor florürlerinin oksijen kaynakları ile olan reaksiyonlarında yan ürün olarak görülür. Klorik asitin asil florürüdür.

İyodik asit, HIO3, beyaz veya kirli beyaz bir katı madde olarak elde edilebilir. Suda çok iyi çözünür, ancak klorik asit veya bromik asidin aksine saf halde bulunur. İyodik asit +5 oksidasyon durumunda iyot içerir ve halojenlerin saf halde en stabil okso-asitlerinden biridir. İyot asidi dikkatle ısıtıldığında pentoksit iyice dehidre olur. Daha sonraki ısıtmada, iyot pentoksit ayrıca iyot, oksijen ve düşük iyot oksitleri karışımı vererek ayrışır.

Kloröz asit, HClO2 formülüne sahip bir inorganik bileşiktir. Zayıf bir asittir. Klor, bu asitte +3 oksidasyon durumuna sahiptir. Saf madde dengesiz, hipokloröz aside (Cl oksidasyon hali + 1) ve klorik aside (Cl oksidasyon hali + 5) orantısızdır:

Hidrojen bromat olarak da bilinen bromik asit, HBrO3 moleküler formülüne sahip bir oksoasittir. Sadece sulu çözelti içinde bulunur. Broma ayrışırken oda sıcaklığında sarıya dönen renksiz bir çözeltidir. Bromik asit ve bromatlar güçlü oksitleyici ajanlardır ve Belousov-Zhabotinsky reaksiyonlarında yaygın bileşenlerdir. Belousov-Zhabotinsky reaksiyonları denge olmayan termodinamiğin klasik bir örneğidir.

Baryum klorür, BaCl2 formüllü inorganik bir bileşik'tir. Bu bileşik baryum'un suda-çözünen en yaygın tuzlarından biridir. Diğer baryum tuzlarının çoğu gibi, baryum klorür beyaz toz halinde ve zehirlidir. Alevde sarı-yeşil renk verir. Ayrıca higroskopiktir, ilk önce dihidrat BaCl2(H2O)2' ye dönüşür.
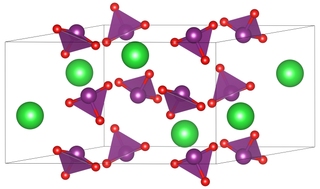
Baryum iyodat, kimyasal formülü Ba(IO3)2 olan inorganik bir kimyasal bileşiktir. Beyaz, granül bir maddedir.






















