Kimyada bir dehidrasyon veya kondenzasyon tepkimesi, tepkiyen moleküllerden su kaybının meydana geldiği bir kimyasal tepkimedir. Dehidrasyon tepkimeleri eliminasyon tepkimelerinin bir alt grubudur. Hidroksil grubu (-OH) kolay ayrılan bir grup olmadığı için bir Bronsted asit katalizörü hidroksil grubunu protonlaştırıp daha kolay ayrılan bir -OH2+ grubu oluşturur. Selülozlar Bu gruba dahil değildirler.

Hidroklorik asit, hidrojen ve klor elementlerinden oluşan, oda sıcaklığı ve normal basınçta gaz hâlinde olan hidrojen klorürün sulu çözeltisine verilen ad. Halk arasında tuz ruhu olarak da bilinir. 9. yüzyılda simyacı Câbir bin Hayyân tarafından keşfedildi ve sonrasında simya alanında kullanıldı. Sanayi Devrimi sırasında, sanayideki önemi keşfedilen asit, önce Leblanc işlemi, sonrasında Solvay işlemi ile sanayi alanında üretilmeye başladı. Hidroklorik asit, tarihte yeni kolaylıkların keşfinde önemli roller üstlendi. Günümüzde PVC'den demir-çeliğe, organik madde üretiminden gıda sektörüne kadar hemen hemen tüm alanlarda hidroklorik asit kullanılmaktadır.

Sülfürik(VI) asit ya da halk arasında bilinen ismi ile zaç yağı, H2SO4, güçlü bir mineral asididir. Olası kâşifi 8. yüzyıl simyacısı Cabir bin Hayyan tarafından yenime uğratıcı, renksiz ve yoğunluğu yüksek sıvı olarak tanımlanmıştır. Suda her konsantrasyonda çözünebilir. Büyük ölçüde korozif oluşu, güçlü asidik yapısından ve dehidrasyon özelliğinden kaynaklanmaktadır.

Tartarik asit ; bitkilerde yaygın olarak bulunan, kristal yapılı, renksiz organik asit. Başta gıda sanayi olmak üzere çeşitli sanayi dallarında kullanılan bu asit, şarabın mayalanması esnasında potasyumun yan ürünü olarak elde edilir. Tartarik asidi bu karışımdan ilk olarak Carl Wilhem Scheele ayırmıştır. Şarap üretiminede ortaya çıkan atıklar potasyum hidroksitle nötralleştirilir. Çöken kalsiyum tartarın sülfürik asitle işlenmesiyle de tartarik asit oluşur.
Nitrik asit, HNO3 kimyasal formülüne sahip oldukça aşındırıcı bir inorganik asittir. Kezzap olarak da bilinir. Saf hâldeki bileşik renksizdir. Ancak uzun süre bekleyen eski asitler azot oksitleri ve suya ayrışması nedeniyle sarı renge dönebilme özelliğindedirler. Piyasada bulunan nitrik asitlerin çoğu % 68'lik bir konsantrasyona sahiptir. Çözelti, %86'dan fazla HNO3 içerdiğinde, dumanlı nitrik asit olarak adlandırılır. Mevcut azot dioksit miktarına bağlı olarak, dumanlı nitrik asit ayrıca %86’nın üzerindeki konsantrasyonlarda kırmızı dumanlı nitrik asit veya %95’in üzerindeki konsantrasyonlarda beyaz dumanlı nitrik asit olarak tanımlanır.

Sülfat iyonu, inorganik kimyada bir sülfür atomu ile bunu tetrahedral yapıda çevreleyen dört eş oksijen atomundan oluşan, negatif yüklü bir anyondur. Ampirik formülü SO42- ve moleküler ağırlığı 96,06 daltondur. Hidrojenle birleştiğinde sülfürik asit oluşturur. Ayrıca,Dimetil sülfat gibi organik sülfatlar, kovalent bileşiklerdir ve sülfürik asidin esterleridir.
- Sülfürik asitte metalin eritilmesi
- Sülfürik asidin bir metal hidroksit veya oksit ile reaksiyonu
- Metal sülfür veya sülfitlerin oksidasyonu
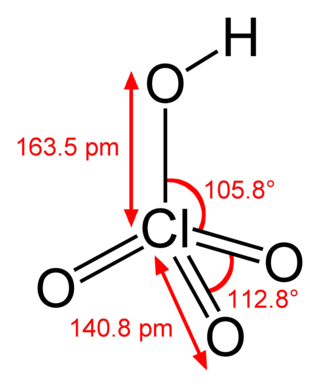
Perklorik asit, HClO4, suda çözünebilen renksiz bir sıvı olan bir klor oksoasididir. Sülfürik asit ya da nitrik asit ile kıyaslanabilecek kadar güçlü bir asittir. Perklorik asit bir süper asittir ancak en güçlü Brønsted-Lowry asidi değildir (en güçlüsü HSbF6 ya da floroantimonik asittir). Asidin pKa'sı −7'dir.

Klorik asit (HClO3), klorun bir oksoasiti ve klorat tuzlarının formal öncülüdür. Güçlü bir asit (pKa ≈1) ve oksitleyici ajandır.

Johann Rudolf Glauber, Alman-Hollandalı simyacı ve kimyacı. Almanya'nın Karlstadt am Main kentinde dünyaya gelen Glauber, resmi bir eğitim görmemiş ve 1655'te Hollanda'nın başkenti Amsterdam'a taşınmıştır

Kükürt trioksit, suyla tepkimeye girdiğinde sülfürik asit oluşturan zehirli bir gazdır. Formülü SO3 şeklindedir. Kükürtlü asidi oluşturan sülfit iyonu (SO3 2-) ile karıştırılmamalıdır.


Peroksidisülfürik asit kimyasal formülü H2S2O8 olan kükürtlü bir oksiasittir. Marshall asidi adı da verilmektedir. Yapısal adlandırmada HO3SOOSO3H olarak yazılabilir. Peroksidisülfürik asidin, niçin sülfatlardan daha yüksek bir yükseltgenme basamağı olduğunu göstermesi +6 yükseltgenme basamağındaki kükürt içermesinden başka, peroksit grubu da içermesinden dolayıdır. Asidin kendisi olmasa da, çoğunlukla persülfat olarak tanınan tuzları sanayi bakımından oldukça önemlidir. Tuzları peroksisülfat iyonu içerir. Bu tuzlar oldukça kuvvetli yükseltgen maddelerdir.
Bir asidin kuvveti, onun içinde bulunduğu çözeltiye ne kadar proton (H+) verebildiğinin ölçüsüdür. Kuvvetli asitler %100 çözünürler ve bu çözünme iyonlaşarak gerçekleşir. Yani 1 mol HA kuvvetli asidi suda çözündüğünde 1 mol H+ ve onun eşlenik bazı A- 1 mol oluşur. Hidroklorik asit, hidroiyodik asit, hidrobromik asit, perklorik asit, nitrik asit ve sülfürik asit, kuvvetli asitlere örnektir.

İyodik asit, HIO3, beyaz veya kirli beyaz bir katı madde olarak elde edilebilir. Suda çok iyi çözünür, ancak klorik asit veya bromik asidin aksine saf halde bulunur. İyodik asit +5 oksidasyon durumunda iyot içerir ve halojenlerin saf halde en stabil okso-asitlerinden biridir. İyot asidi dikkatle ısıtıldığında pentoksit iyice dehidre olur. Daha sonraki ısıtmada, iyot pentoksit ayrıca iyot, oksijen ve düşük iyot oksitleri karışımı vererek ayrışır.
Florosülfürik asit (IUPAC adı: sülfürofloridik asit), HSO3F kimyasal formüllü bir inorganik bileşiktir. Ticarî olarak temin edilebilen en güçlü asitlerden biridir. HSO3F formülü sülfürik asit (H2SO4) ile ilişkisini vurgulamaktadır. HSO3F tetrahedral bir moleküldür. Ticari numuneler genellikle sarı olmasına rağmen renksiz bir sıvıdır.

Kloröz asit, HClO2 formülüne sahip bir inorganik bileşiktir. Zayıf bir asittir. Klor, bu asitte +3 oksidasyon durumuna sahiptir. Saf madde dengesiz, hipokloröz aside (Cl oksidasyon hali + 1) ve klorik aside (Cl oksidasyon hali + 5) orantısızdır:
Permanganik asit, HMnO4 formülüne sahip bir inorganik bileşiktir. Bu güçlü oksoasit, dihidrat olarak izole edilmiştir. Permanganat tuzlarının konjugat asididir. Çok az sayıda yayın konusu olup, karakterizasyonu ve kullanımları çok sınırlıdır.
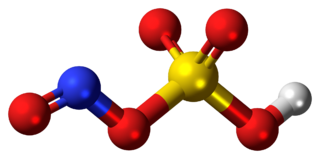
Nitrozilsülfürik asit, NOHSO4 formülüne sahip bir kimyasal bileşiktir. Endüstriyel olarak kaprolaktam üretiminde kullanılan renksiz bir katıdır. Daha önce sülfürik asit üretmek için öncü oda işleminin bir parçasıydı. Bileşik, sülfürik asit ve nitröz asidin karışık anhidritidir.

Disülfürik asit veya pirosülfürik asit, kükürtün bir oksoasitidir. Oleumun önemli bir bileşenidir ve çoğu kimyager bu şekilde karşılaşır. Aynı zamanda, dengeye bağlı olarak sıvı susuz sülfürik asidin küçük bir bileşenidir:
- H2SO4 ⇌ H2O + SO3
- SO3 + H2SO4 ⇌ H2S2O7

Tellürik asit, Te(OH)6 formülüne sahip kimyasal bir bileşiktir. Sulu çözelti içinde devam eden oktahedral Te(OH)6 moleküllerinden oluşan beyaz bir katıdır. Rombohedral ve monoklinik olmak üzere iki formu vardır ve her ikisi de oktahedral Te(OH)6 molekülleri içerir. Tellürik asit, güçlü bazlara sahip tellürat tuzları ve zayıf bazlara sahip hidrojen tellürat tuzları veya sudaki tellüratların hidrolizi üzerine dibazik olan zayıf bir asittir.
Kimyada, süper asit, orijinal tanımıyla, asitliği %100 saf sülfürik asitten daha yüksek olan bir asittir. Modern tanımıyla süper asit, protonun kimyasal potansiyelinin saf sülfürik asitten daha yüksek olduğu bir ortamdır. Ticarî olarak temin edilebilen süperasitler arasında triflik asit olarak da bilinen triflorometansülfonik asit ve florosülfürik asit bulunur; bunların her ikisi de sülfürik asitten yaklaşık bin kat daha güçlüdür, yani daha negatif H0 değerlerine sahiptir.















