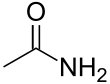
Asetamid
| |||
| Adlandırmalar | |||
|---|---|---|---|
Tercih edilen IUPAC adı Asetamid[1] | |||
Sistematik IUPAC adı Etanamid | |||
Diğer adlar asetik asit amidi Asetilamin | |||
| Tanımlayıcılar | |||
CAS numarası | |||
3D model (JSmol) | |||
| ChEBI | |||
| ChEMBL | |||
| ChemSpider | |||
| DrugBank | |||
| ECHA InfoCard | 100.000.430 | ||
| EC Numarası |
| ||
IUPHAR/BPS | |||
| KEGG | |||
PubChem CID | |||
| RTECS numarası |
| ||
| UNII | |||
CompTox Bilgi Panosu (EPA) | |||
| |||
| |||
| Özellikler | |||
| Kimyasal formül | C2H5NO | ||
| Molekül kütlesi | 59,07 g mol−1 | ||
| Görünüm | renksiz, higroskopik sıvı | ||
| Koku | kokusuz saf olmayan örnekler: fare gibi | ||
| Yoğunluk | 1.159 g cm−3 | ||
| Erime noktası | 79 ila 81 °C (174 ila 178 °F; 352 ila 354 K) | ||
| Kaynama noktası | 221,2 °C (430,2 °F; 494,3 K) (bozunur) | ||
| Çözünürlük (su içinde) | 2000 g L−1[2] | ||
| Çözünürlük | etanol 500 g L−1[2] piridin 166.67 g L−1[2] kloroform, gliserol, benzende çözünür[2] | ||
| log P | −1.26 | ||
| Buhar basıncı | 1.3 Pa | ||
| Asitlik (pKa) | 15.1 (25 °C, H2O)[3] | ||
| −0.577 × 10−6 cm3 g−1 | |||
| Kırınım dizimi (nD) | 1.4274 | ||
| Akmazlık | 2.052 cP (91 °C) | ||
| Yapı | |||
| trigonal | |||
| Termokimya[4] | |||
Isı sığası (C) | 91.3 J·mol−1·K−1 | ||
Standart molar entropi (S⦵298) | 115.0 J·mol−1·K−1 | ||
Standart formasyon entalpisi (ΔfH⦵298) | −317.0 kJ·mol−1 | ||
| Tehlikeler | |||
| GHS etiketleme sistemi: | |||
| Piktogramlar |  | ||
| İşaret sözcüğü | Warning | ||
| Tehlike ifadeleri | H351 | ||
| Önlem ifadeleri | P201, P202, P281, P308+P313, P405, P501 | ||
| NFPA 704 (yangın karosu) | |||
| Parlama noktası | 126 °C (259 °F; 399 K) | ||
| Öldürücü doz veya konsantrasyon (LD, LC): | |||
LD50 (medyan doz) | 7000 mg kg−1 (sıçan, oral) | ||
| Güvenlik bilgi formu (SDS) | External MSDS | ||
| Benzeyen bileşikler | |||
Benzeyen bileşikler | formamid | ||
| Aksi belirtilmediği sürece madde verileri, Standart sıcaklık ve basınç koşullarında belirtilir (25 °C [77 °F], 100 kPa). | |||
Asetamid, CH3CONH2 kimyasal formüllü bir organik bileşiktir. Asetik asitten türemiş en küçük amiddir. Plastikleştirici ve endüstriyel solvent olarak kullanımları bulunur.[5] İlişiği olan N,N-Dimetilasetamid bileşiği daha fazla kullanılır, lakin asetamidden üretilmez. Asetamid, aseton ve üre arasında görülebilir; asetonda karbonilin iki tarafında metil (CH3) varken ürede iki adet amid grubu bulunur.
Üretim
Asetamid laboratuvarda amonyum asetatın dehidrasyonu ile elde edilir.[6]
- [NH4][CH3CO2] → CH3C(O)NH2 + H2O
Sanayide asetamid ya laboratuvardaki ile aynı yöntemle üretilir ya da akrilonitril üretminin yan ürünü olan asetonitrilin hidrasyonu ile üretilir.[5]
- CH3CN + H2O → CH3C(O)NH2
Kaynakça
- ^ "Front Matter". Nomenclature of Organic Chemistry : IUPAC Recommendations and Preferred Names 2013 (Blue Book). Cambridge: The Royal Society of Chemistry. 2014. s. 841. doi:10.1039/9781849733069-FP001. ISBN 978-0-85404-182-4.
- ^ a b c d The Merck Index, 14th Edition, 36
- ^ Haynes, William M., (Ed.) (2016). CRC Handbook of Chemistry and Physics (97.97yayıncı= CRC Press bas.). ss. 5-88. ISBN 9781498754293.
- ^ John Rumble (18 Haziran 2018). CRC Handbook of Chemistry and Physics (99.99dil=İngilizce bas.). CRC Press. ss. 5-3. ISBN 978-1138561632.
- ^ a b "Acetic Acid". Ullmann's Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. doi:10.1002/14356007.a01_045.pub2. 16 Mart 2020 tarihinde Wayback Machine sitesinde arşivlendi.
- ^ Coleman, G. H.; Alvarado, A. M. (1923). "Acetamide 24 Temmuz 2020 tarihinde Wayback Machine sitesinde arşivlendi.". Organic Syntheses. 3: 3. doi:10.15227/orgsyn.003.0003. 24 Temmuz 2020 tarihinde Wayback Machine sitesinde arşivlendi.; Collective Volume, 1, p. 3