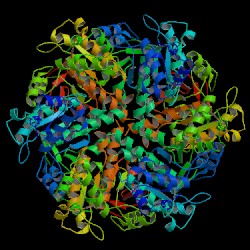
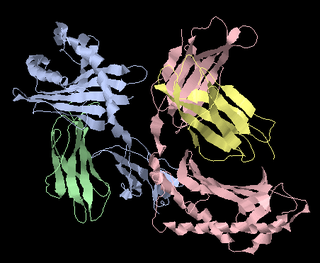
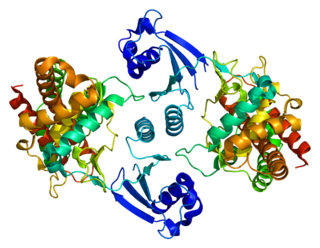
Arrestin beta 1
Arrestin beta 1 (ARRB1 olarak da bilinir), insanlarda ARRB1 geni tarafından kodlanan bir proteindir.[4][5]
İşlev
Arrestin/beta arrestin proteini ailesinin üyelerinin, G proteini kenetli reseptörlerin agonist aracılı duyarsızlaşmasına katıldıkları ve hormonlar, nörotransmitterler veya duyusal sinyaller gibi uyaranlara hücresel yanıtların özgül olarak azaltılmasına neden oldukları düşünülmektedir. Arrestin beta 1, sitozolik bir proteindir ve beta adrenerjik reseptör kinaz (BARK) aracılı beta-adrenerjik reseptörlerin duyarsızlaştırılmasında bir kofaktör görevi görür. Merkezi sinir sisteminin yanı sıra, periferik kan lökositlerinde yüksek düzeylerde dışa vurulur ve bu nedenle BARK/beta arrestin sisteminin reseptör aracılı bağışıklık işlevlerinin düzenlenmesinde önemli bir rol oynadığına inanılmaktadır. Arrestin beta 1'in farklı izoformlarını kodlayan alternatif olarak uçbirleştirilmiş transkriptler tanımlanmıştır, ancak bunların kesin işlevleri bilinmemektedir.[5] Beta arrestin ayrıca GPCR yollarında yapı iskelesi proteini olarak da rol oynayabilir.[]
Etkileşimler
Aşağıda arrestin beta 1 ile etkileşime girenler gösterilmiştir:
Kaynakça
- ^ a b c GRCh38: Ensembl release 89: ENSG00000137486 - Ensembl, May 2017
- ^ "İnsan PubMed Başvurusu:". National Center for Biotechnology Information, U.S. National Library of Medicine.
- ^ "Fare PubMed Başvurusu:". National Center for Biotechnology Information, U.S. National Library of Medicine.
- ^ "Molecular analysis of human beta-arrestin-1: cloning, tissue distribution, and regulation of expression. Identification of two isoforms generated by alternative splicing". The Journal of Biological Chemistry. 268 (13). Mayıs 1993. ss. 9753-61. 3 Ocak 2005 tarihinde kaynağından arşivlendi. Erişim tarihi: 4 Mart 2020.
- ^ a b "Entrez Gene: ARRB1 arrestin, beta 1". 5 Aralık 2010 tarihinde kaynağından arşivlendi.
- ^ "beta-Arrestin-mediated ADP-ribosylation factor 6 activation and beta 2-adrenergic receptor endocytosis". J. Biol. Chem. 276 (45). Kasım 2001. ss. 42509-13.
- ^ "The COOH-terminus of parathyroid hormone-related protein (PTHrP) interacts with beta-arrestin 1B". FEBS Lett. 527 (1-3). Eylül 2002. ss. 71-5.
- ^ "beta-Arrestin1 modulates lymphoid enhancer factor transcriptional activity through interaction with phosphorylated dishevelled proteins". Proc. Natl. Acad. Sci. U.S.A. 98 (26). Aralık 2001. ss. 14889-94.
- ^ "Subcellular localization of beta-arrestins is determined by their intact N domain and the nuclear export signal at the C terminus". J. Biol. Chem. 278 (13). Mart 2003. ss. 11648-53.
- ^ "Nedd4 mediates agonist-dependent ubiquitination, lysosomal targeting, and degradation of the beta2-adrenergic receptor". J. Biol. Chem. 283 (32). Ağustos 2008. ss. 22166-76.
- ^ "Direct binding of beta-arrestins to two distinct intracellular domains of the delta opioid receptor". J. Neurochem. 76 (6). Mart 2001. ss. 1887-94.
- ^ "Beta-arrestins regulate a Ral-GDS Ral effector pathway that mediates cytoskeletal reorganization". Nat. Cell Biol. 4 (8). Ağustos 2002. ss. 547-55.
Konuyla ilgili yayınlar
- Lefkowitz RJ (1998). "G protein-coupled receptors. III. New roles for receptor kinases and beta-arrestins in receptor signaling and desensitization". J. Biol. Chem. 273 (30). ss. 18677-80. doi:10.1074/jbc.273.30.18677. PMID 9668034.
- Lohse MJ, Benovic JL, Codina J (1990). "beta-Arrestin: a protein that regulates beta-adrenergic receptor function". Science. 248 (4962). ss. 1547-50. doi:10.1126/science.2163110. PMID 2163110.
- Calabrese G, Sallese M, Stornaiuolo A (1995). "Assignment of the beta-arrestin 1 gene (ARRB1) to human chromosome 11q13". Genomics. 24 (1). ss. 169-71. doi:10.1006/geno.1994.1594. PMID 7896272.
- Parruti G, Peracchia F, Sallese M (1993). "Molecular analysis of human beta-arrestin-1: cloning, tissue distribution, and regulation of expression. Identification of two isoforms generated by alternative splicing". J. Biol. Chem. 268 (13). ss. 9753-61. PMID 8486659.
- Iacovelli L, Franchetti R, Masini M, De Blasi A (1997). "GRK2 and beta-arrestin 1 as negative regulators of thyrotropin receptor-stimulated response". Mol. Endocrinol. 10 (9). ss. 1138-46. doi:10.1210/me.10.9.1138. PMID 8885248.
- Bonaldo MF, Lennon G, Soares MB (1997). "Normalization and subtraction: two approaches to facilitate gene discovery". Genome Res. 6 (9). ss. 791-806. doi:10.1101/gr.6.9.791. PMID 8889548.
- Goodman OB, Krupnick JG, Gurevich VV (1997). "Arrestin/clathrin interaction. Localization of the arrestin binding locus to the clathrin terminal domain". J. Biol. Chem. 272 (23). ss. 15017-22. doi:10.1074/jbc.272.23.15017. PMID 9169477.
- Lin FT, Krueger KM, Kendall HE (1998). "Clathrin-mediated endocytosis of the beta-adrenergic receptor is regulated by phosphorylation/dephosphorylation of beta-arrestin1". J. Biol. Chem. 272 (49). ss. 31051-7. doi:10.1074/jbc.272.49.31051. PMID 9388255.
- Aragay AM, Mellado M, Frade JM (1998). "Monocyte chemoattractant protein-1-induced CCR2B receptor desensitization mediated by the G protein-coupled receptor kinase 2". Proc. Natl. Acad. Sci. U.S.A. 95 (6). ss. 2985-90. doi:10.1073/pnas.95.6.2985. PMC 19681 $2. PMID 9501202.
- ter Haar E, Musacchio A, Harrison SC, Kirchhausen T (1998). "Atomic structure of clathrin: a beta propeller terminal domain joins an alpha zigzag linker". Cell. 95 (4). ss. 563-73. doi:10.1016/S0092-8674(00)81623-2. PMC 4428171 $2. PMID 9827808.
- Luttrell LM, Ferguson SS, Daaka Y (1999). "Beta-arrestin-dependent formation of beta2 adrenergic receptor-Src protein kinase complexes". Science. 283 (5402). ss. 655-61. doi:10.1126/science.283.5402.655. PMID 9924018.
- McDonald PH, Cote NL, Lin FT (1999). "Identification of NSF as a beta-arrestin1-binding protein. Implications for beta2-adrenergic receptor regulation". J. Biol. Chem. 274 (16). ss. 10677-80. doi:10.1074/jbc.274.16.10677. PMID 10196135.
- Lin FT, Miller WE, Luttrell LM, Lefkowitz RJ (1999). "Feedback regulation of beta-arrestin1 function by extracellular signal-regulated kinases". J. Biol. Chem. 274 (23). ss. 15971-4. doi:10.1074/jbc.274.23.15971. PMID 10347142.
- McConalogue K, Déry O, Lovett M (1999). "Substance P-induced trafficking of beta-arrestins. The role of beta-arrestins in endocytosis of the neurokinin-1 receptor". J. Biol. Chem. 274 (23). ss. 16257-68. doi:10.1074/jbc.274.23.16257. PMID 10347182.
- Miller WE, Maudsley S, Ahn S (2000). "beta-arrestin1 interacts with the catalytic domain of the tyrosine kinase c-SRC. Role of beta-arrestin1-dependent targeting of c-SRC in receptor endocytosis". J. Biol. Chem. 275 (15). ss. 11312-9. doi:10.1074/jbc.275.15.11312. PMID 10753943.
- Laporte SA, Oakley RH, Holt JA (2000). "The interaction of beta-arrestin with the AP-2 adaptor is required for the clustering of beta 2-adrenergic receptor into clathrin-coated pits". J. Biol. Chem. 275 (30). ss. 23120-6. doi:10.1074/jbc.M002581200. PMID 10770944.
- Bennett TA, Maestas DC, Prossnitz ER (2000). "Arrestin binding to the G protein-coupled N-formyl peptide receptor is regulated by the conserved "DRY" sequence". J. Biol. Chem. 275 (32). ss. 24590-4. doi:10.1074/jbc.C000314200. PMID 10823817.
- Shiina T, Kawasaki A, Nagao T, Kurose H (2000). "Interaction with beta-arrestin determines the difference in internalization behavor between beta1- and beta2-adrenergic receptors". J. Biol. Chem. 275 (37). ss. 29082-90. doi:10.1074/jbc.M909757199. PMID 10862778.
- Barlic J, Andrews JD, Kelvin AA (2001). "Regulation of tyrosine kinase activation and granule release through beta-arrestin by CXCRI". Nat. Immunol. 1 (3). ss. 227-33. doi:10.1038/79767. PMID 10973280.
- Shukla, A. K.; Westfield, G. H.; Xiao, K; Reis, R. I.; Huang, L. Y.; Tripathi-Shukla, P; Qian, J; Li, S; Blanc, A; Oleskie, A. N.; Dosey, A. M.; Su, M; Liang, C. R.; Gu, L. L.; Shan, J. M.; Chen, X; Hanna, R; Choi, M; Yao, X. J.; Klink, B. U.; Kahsai, A. W.; Sidhu, S. S.; Koide, S; Penczek, P. A.; Kossiakoff, A. A.; Woods Jr, V. L.; Kobilka, B. K.; Skiniotis, G; Lefkowitz, R. J. (2014). "Visualization of arrestin recruitment by a G-protein-coupled receptor". Nature. Cilt 512. ss. 218-22. doi:10.1038/nature13430. PMC 4134437 $2. PMID 25043026.
Dış bağlantılar
- İnsan ARRB130 Aralık 2019 tarihinde Wayback Machine sitesinde arşivlendi. genom yerleşimi ve ARRB1[] geni ayrıntıları sayfası UCSC Genom Tarayıcısında.