
Hidrojen, sembolü H, atom numarası 1 olan kimyasal bir element. Standart sıcaklık ve basınç altında renksiz, kokusuz, metalik olmayan, tatsız, oldukça yanıcı ve H2 olarak bulunan bir diatomik gazdır. 1,00794 g/mol'lük atomik kütlesi ile tüm elementler arasında en hafif olanıdır. Periyodik cetvelin sol üst köşesinde yer alır. Hidrojenin adı, Yunancada "su oluşturan" anlamına gelen ὑδρογόνο'dan (idrogono) kelimesinden gelir.

Helyum, sembolü He ve atom numarası 2 olan kimyasal element. Periyodik cetvelin birinci periyot 8A grubunda yer alan bir gazdır. Kokusuz, renksiz bir gazdır ve yanmaz.

Karbon, doğada yaygın bulunan ametal kimyasal elementtir. Evrende bolluk bakımından altıncı sırada yer alan karbon, kızgın yıldızlarda hidrojenin termonükleer yanmasında temel rol oynar. Dünyada hem doğal halde, hem de başka elementlerle bileşik halinde bulunan karbon, ağırlık olarak Dünya'nın yerkabuğunun yaklaşık %0,2'sini oluşturur. En arı (katışıksız) biçimleri elmas ve grafittir; daha düşük arılık derecelerinde maden kömürünün, kok kömürünün ve odun kömürünün bileşeni olarak bulunur. Atmosferin yaklaşık % 0,05'ini oluşturan ve bütün doğal sularda erimiş olarak bulunan karbon dioksit, kireç taşı ve mermer gibi karbonat mineralleri, kömürün, petrolün ve doğalgazın başlıca yapıtaşları olan hidrokarbonlar, en bol bulunan bileşikleridir.

Soy gaz veya asal gaz, standart şartlar altında her biri, diğer elementlere kıyasla daha düşük kimyasal reaktifliğe sahip, kokusuz, renksiz, tek atomlu gaz olan kimyasal element grubudur. Helyum (He), neon (Ne), argon (Ar), kripton (Kr), ksenon (Xe) ve radon (Rn) doğal olarak bulunan altı soy gazdır ve tamamı ametaldir. Her biri periyodik tablonun sırasıyla ilk altı periyodunda, 18. grubunda (8A) yer alır. Grupta yer alan oganesson (Og) için ise önceleri soy gaz olabileceği ihtimali üzerinde durulsa da günümüzde metalik görünümlü reaktif bir katı olduğu öngörülmektedir.

Benzen, aren veya aromatik hidrokarbonlar olarak adlandırılan organik bileşikler sınıfının en basit üyesidir. Renksiz, yanıcı, kaynama noktası 80,1 °C, erime noktası 5,5 °C olan bir sıvıdır. Moleküler formülü C6H6'dır. Benzen, endüstriyel bakımdan değerli olduğu gibi yapısı bakımından da kimya çalışmalarında önemlidir. Kan hücrelerini öldürme etkisi olduğundan kanser yapıcı bileşikler arasına girer.

Organik kimya, organik bileşiklerin ve organik maddelerin yani karbon atomlarını içeren çeşitli formlardaki maddelerin yapısını, özelliklerini ve reaksiyonların bilimsel çalışmasını içeren, kimyanın bir alt dalıdır. Yapının incelenmesi yapısal formüllerini belirler. Özelliklerin incelenmesi, fiziksel ve kimyasal özellikleri ve davranışlarını anlamak için kimyasal reaktivitenin değerlendirilmesidir. Organik reaksiyonların incelenmesi doğal ürünlerin, ilaçların ve polimerlerin kimyasal sentezini ve bireysel organik moleküllerin laboratuvarda ve teorik çalışma yoluyla incelenmesidir.
Ksenon, Xe sembolü ile gösterilen 54 atom numaralı kimyasal elementtir. Renksiz, ağır, kokusuz bir soy gaz olan ksenon Dünya atmosferinde eser miktarda bulunur. Genellikle reaktif olmayan element, sentezlenen ilk soy gaz bileşiği olan ksenon heksafloroplatinatın oluşumu gibi birkaç kimyasal reaksiyona maruz kalabilir.
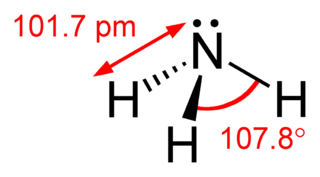
Amonyak, formülü NH3 olan; azot atomu ve hidrojen atomundan oluşan renksiz, keskin ve rahatsız edici kokulu bir bileşiktir. OH- iyonu içermediği hâlde suda zayıf baz özelliği gösterir. Bir amonyak molekülü, bir azot ve üç hidrojen atomundan oluşur. Oda sıcaklığında gaz hâlde bulunan bileşiğin ticari formu sulu çözeltiyi içermektedir.

Hidroklorik asit, hidrojen ve klor elementlerinden oluşan, oda sıcaklığı ve normal basınçta gaz hâlinde olan hidrojen klorürün sulu çözeltisine verilen ad. Halk arasında tuz ruhu olarak da bilinir. 9. yüzyılda simyacı Câbir bin Hayyân tarafından keşfedildi ve sonrasında simya alanında kullanıldı. Sanayi Devrimi sırasında, sanayideki önemi keşfedilen asit, önce Leblanc işlemi, sonrasında Solvay işlemi ile sanayi alanında üretilmeye başladı. Hidroklorik asit, tarihte yeni kolaylıkların keşfinde önemli roller üstlendi. Günümüzde PVC'den demir-çeliğe, organik madde üretiminden gıda sektörüne kadar hemen hemen tüm alanlarda hidroklorik asit kullanılmaktadır.

Astrokimya, dünya dışında bulunan kimyasal elementleri, kimyasal maddeleri ve bu maddelerin birbirine etkisini tahribatını genellikle Güneş Sistemi'nden daha geniş alanlarda özellikle moleküler gaz bulutlarında inceleyen bir bilim. Bu nedenle astrokimya, astronomi ve kimya bilimlerinin birleşmesidir. Güneş sistemi genişliğindeki incelemelere "kozmokimya" denmektedir.

Kimyasal madde, kimyevî madde veya kısaca kimyasal, sabit bir kimyasal bileşimi ve karakteristik özelliklere sahip bir madde türüdür. Bu kimyasal bağlar bozulmadan, fiziksel ayırma yöntemleri ile bileşenlerine ayrılmaz. Bu kimyasallar katı, sıvı veya gaz hâlinde olurlar.

Soy gaz bileşiği, içeriğinde en az bir soy gaz olan bileşiklerdir. 20. yüzyılın ortalarına kadar genel kanı soy gazların kimyasal tepkimelere giremeyecekleri, dolayısıyla bileşik oluşturamayacakları yönündeydi.
İnert gaz veya atıl gaz, belirli şartlar altında kimyasal reaksiyona girmeyen bir gazdır. Soy gazlar ve azot, genellikle birçok madde ile tepkimeye girmezler. İnert gazlar, genel olarak istenmeyen kimyasal reaksiyonların numuneyi etkilemelerini önlemek için kullanılır. Bu arzu edilmeyen kimyasal tepkimeler, genellikle havadaki oksijen ve nemden oluşan oksidasyon ve hidroliz reaksiyonlarıdır. Azot gazı ve bazı soy gazlar belirli koşullarda tepkimeye yol açabilir ve bu nedenle inert gaz terimi kullanıldığı kapsama bağlıdır.

Hidrojen florür, formülü HF olan bir kimyasal bileşiktir. Bu renksiz gaz genellikle, hidroflorik asit gibi sulu çözelti formunda bulunur ve florun başlıca sanayi kaynağıdır. İlaç ve polimer endüstrisinde kullanılan önemli bileşiklerin öncüsüdür. HF petrokimya endüstrisinde yaygın olarak kullanılır ve birçok süperasitin bir bileşenidir. Hidrojen florür oda sıcaklığının hemen altında kaynar. Diğer hidrojen halojenürler ise çok daha düşük sıcaklıklarda kaynarlar. Diğer hidrojen halidlerden farklı olarak, HF havadan daha hafiftir ve gözenekli maddelerde oldukça çabuk şekilde yayılır.

Ksenon hekzaflorür, kimyasal formülü XeF6 olan, ksenon ile flor elementlerinin reaksiyonuyla meydana gelen soy gaz bileşiğidir. Ksenon hekzaflorür, ksenon diflorür (XeF2) ve ksenon tetraflorür (XeF4) ile birlikte ksenonun bilinen üç florür bileşiğinin en yükseğidir.

Florokarbonlar, bazen perflorokarbon veya PFC olarak da anılır, CxFy formülüne sahip organoflor bileşikleridir. Sadece karbon ve flor içerirler fakat terminoloji her zaman çok sıkı takip edilmemektedir. Perfloro- ön ekine sahip bileşikler, heteroatomlu olanlar da dâhil olmak üzere hidrokarbonlardır, burada tüm C-H bağları C-F bağlarıyla değiştirilmiştir. Florokarbonlar perfloroalkanlar, floroalkenler ve floroalkinler ve perfloroaromatik bileşikler olabilir. Florokarbonlar ve bunların türevleri floropolimerler, soğutucular, çözücüler ve anestezikler olarak kullanılır.
İyot pentafluorür, IF5 kimyasal formülüne sahip florür ve iyottan oluşan bir interhalojen bileşiktir. 3.250 g cm−3 yoğunluğa sahip, renksiz veya sarı bir sıvıdır. İlk olarak 1891'de Henri Moissan tarafından flor gazı içinde katı iyot yakılarak sentezlendi. Bu ekzotermik reaksiyon, reaksiyon koşulları iyileştirilmiş olmasına rağmen hala iyot pentaflorür üretmek için kullanılır. I2 + 5 F2 → 2 IF5

Hipofloröz asit, kimyasal formül HOF, florun bilinen tek oksoasididir. Hipofloritlerde oksijenin oksidasyon durumu 0'dır. Aynı zamanda katı olarak izole edilebilen tek hipohaloid asittir. HOF, suyun, hidrojen florür, oksijen diflorür, hidrojen peroksit, ozon ve oksijen üreten flor ile oksidasyonunda bir ara maddedir. HOF oda sıcaklığında patlayıcıdır, HF ve O2 oluşturur:
- 2 HOF → 2 HF + O2

İzosiyanik asit, 1830'da Liebig ve Wöhler tarafından keşfedilen HNCO formülüne sahip bir kimyasal bileşiktir. Kaynama noktası 23.5 °C olan uçucu ve zehirli renksiz bir maddedir. İzosiyanik asit, organik kimya ve biyolojide en yaygın olarak bulunan dört element olan karbon, hidrojen, azot ve oksijen içeren en basit kararlı kimyasal bileşiktir.

Klor triflorür, formülü ClF3 olan interhalojen bir bileşiktir. Zehirli, aşındırıcı ve aşırı reaktiftir. Gaz hâlindeyken renksizken sıvı hâlindeyken solgun yeşilimsi sarı renktedir. Yarı iletken sanayiinde, nükleer yakıtların yeniden işlenmesinde, roket itici yakıtlarında ve diğer endüstriyel alanlarda kullanılır. Benzen, toluen, eter, alkol, asetik asit, hekzan gibi çözücüler ile reaksiyona girer. Karbon tetraklorürde çözünür ancak yüksek konsantrasyonlarda patlayıcı olabilir.

















