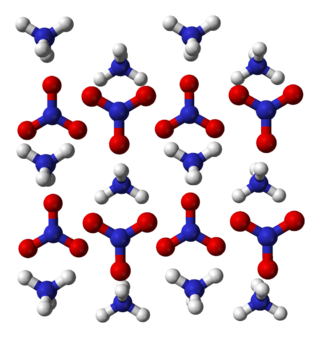
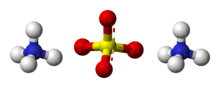
Amonyum sülfat
 | |
 | |
| Adlandırmalar | |
|---|---|
Diazanyum sülfat | |
Diğer adlar amonyum sülfat (2:1) diamonyum sülfat sülfürik asitin diamonyum tuzu şeker gübresi | |
| Tanımlayıcılar | |
CAS numarası | |
3D model (JSmol) | |
| ChemSpider | |
| ECHA InfoCard | 100.029.076 |
| E numaraları | E517 (asitliği düzenleyiciler, ...) |
| KEGG | |
| UNII | |
CompTox Bilgi Panosu (EPA) | |
| |
| |
| Özellikler | |
| Molekül formülü | (NH4)2SO4 |
| Molekül kütlesi | 132.14 gr/mol |
| Görünüm | Beyaz ince higroskopik granüller ya da kristaller. |
| Yoğunluk | 1.769 gr/cm3 (20 °C) |
| Erime noktası | 235 - 280 °C (bozunur) |
| Çözünürlük (su içinde) | 70.6 gr/100 mL (0 °C) 74.4 gr/100 mL (20 °C) 103.8 gr/100 mL (100 °C) |
| Çözünürlük | aseton, alkol ve eterde çözünmez |
| Kritik bağıl nem | %79.2 (30 °C) |
| Yapı | |
| ortorombik | |
| Tehlikeler | |
| GHS etiketleme sistemi: | |
| Piktogramlar |   |
| İşaret sözcüğü | Uyarı |
| Tehlike ifadeleri | H315, H319, H335 |
| Önlem ifadeleri | P261, P264, P270, P271, P273, P280, P301+P312, P302+P352, P304+P340, P305+P351+P338, P312, P321, P330, P332+P313, P337+P313, P362, P391, P403+P233, P405, P501 |
| NFPA 704 (yangın karosu) | |
| Parlama noktası | Yanıcı değildir |
| Öldürücü doz veya konsantrasyon (LD, LC): | |
LD50 (medyan doz) | 2840 mg/kg (sıçan, oral) |
| Benzeyen bileşikler | |
Diğer anyonlar | Amonyum tiyosülfat Amonyum sülfit Amonyum bisülfat Amonyum persülfat |
Diğer katyonlar | Sodyum sülfat Potasyum sülfat |
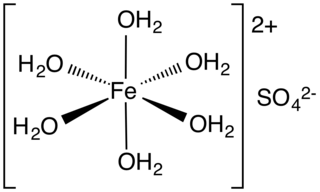
Benzeyen bileşikler | Amonyum demir(II) sülfat |
| Aksi belirtilmediği sürece madde verileri, Standart sıcaklık ve basınç koşullarında belirtilir (25 °C [77 °F], 100 kPa). | |
Amonyum sülfat, (NH4)2SO4 formülüne ve çok sayıda ticari kullanıma sahip bir inorganik tuzdur. Toprak gübresi olarak yaygın bir şekilde kullanılır. %21 azot ve %24 kükürt içerir.
Kullanımı
Amonyum sülfat esas olarak, alkali topraklarda bir gübre olarak kullanılmaktadır. Toprakta amonyum iyonu salınır ve az miktarda asit oluşturarak toprağın pH dengesini düşürürken bitki büyümesi için gerekli azotla katkıda bulunur. Amonyum sülfat kullanımının ana dezavantajı, amonyum nitrata göre düşük azot içeriği nedeniyle taşıma maliyetlerinin yüksekliğidir.[1]
Ayrıca suda çözünen insektisitler, herbisitler ve fungusitler için tarımsal bir sprey adjuvantı olarak kullanılır. Burada hem kuyu suyunda hem de bitki hücrelerinde bulunan demir ve kalsiyum katyonlarını bağlama işlevi görür. 2,4-D (amin), glifosat ve glufosinat herbisitleri için bir adjuvant olarak özellikle etkilidir.
Laboratuvar kullanımı
Amonyum sülfat çökeltmesi, çökeltme yoluyla protein saflaştırması için yaygın bir yöntemdir. Bir çözeltinin iyonik kuvveti arttıkça, o çözeltideki proteinlerin çözünürlüğü azalır. Amonyum sülfat, iyonik yapısı nedeniyle suda son derece çözünür, bu nedenle proteinleri çökeltme yoluyla "tuzlayabilir".[2] Suyun yüksek dielektrik katsayısı nedeniyle, katyonik amonyum ve anyonik sülfat olan ayrışmış tuz iyonları, su moleküllerinin hidrasyon kabukları içinde kolayca çözülür. Bu maddenin bileşiklerin saflaştırılmasındaki önemi, nispeten daha apolar moleküllere kıyasla daha fazla hidratlı hâle gelme kabiliyetinden kaynaklanır ve bu nedenle arzu edilen apolar moleküller birleşir ve çözeltiden konsantre bir formda çökelir. Bu yönteme tuzla çökelme denir ve sulu karışımda güvenilir bir şekilde çözülebilen yüksek tuz konsantrasyonlarının kullanılmasını gerektirir. Kullanılan tuzun yüzdesi, karışımın çözebileceği maksimum tuz konsantrasyonuyla karşılaştırılır. Bu nedenle, yöntemin çalışması için yüksek konsantrasyonlara ihtiyaç duyulsa da, %100'ün üzerinde bol miktarda tuz eklemek de çözeltiyi aşırı doyurabilir, bu nedenle polar olmayan çökeltiyi tuz çökeltisi ile kirletebilir.[3] Bir çözeltiye amonyum sülfat konsantrasyonu eklenerek veya arttırılarak elde edilebilen yüksek bir tuz konsantrasyonu, protein çözünürlüğündeki azalmaya bağlı olarak protein ayrılmasını sağlar; bu ayırma santrifüjleme ile elde edilebilir. Amonyum sülfat ile çökeltme, protein denatürasyonundan ziyade çözünürlüğün azalmasının bir sonucudur, bu nedenle çökelen protein, standart tamponların kullanılması yoluyla çözündürülebilir.[4] Amonyum sülfat çökeltmesi, karmaşık protein karışımlarını fraksiyonlara ayırmak için uygun ve basit bir yol sağlar.[5]
Kauçuk lateks analizinde, uçucu yağ asitleri, uçucu yağ asitlerinin sülfürik asit ile yeniden üretildiği ve daha sonra buharla damıtıldığı berrak bir sıvı bırakan %35 amonyum sülfat çözeltisi ile kauçuğun çökeltilmesiyle analiz edilir. Amonyum sülfat ile seçici çöktürme, asetik asit kullanan alışılagelmiş çökeltme tekniğinin aksine, uçucu yağ asitlerinin tayinini etkilemez.[6]
Gıda katkı maddesi
Bir gıda katkı maddesi olarak, amonyum sülfat ABD Gıda ve İlaç İdaresi tarafından genel olarak güvenli olarak kabul edilir[7] ve Avrupa Birliği'nde E numarası E517 ile belirtilir. Unlarda ve ekmeklerde asitlik düzenleyici olarak kullanılır.[8][9][10]
Diğer kullanımlar
İçme suyunun arıtımında, amonyum sülfat, dezenfeksiyon için monokloramin üretmek için klor ile kombinasyon halinde kullanılır.[11]
Amonyum sülfat, diğer amonyum tuzlarının, özellikle amonyum persülfatın hazırlanmasında küçük ölçekte kullanılır.
Amonyum sülfat, CDC'e göre birçok Amerika Birleşik Devletleri aşısının bir bileşeni olarak listelenmiştir..[12]
Ağır su (D2O) içindeki doymuş bir amonyum sülfat çözeltisi, 0 ppm kaydırma değeriyle kükürt (33S) NMR spektroskopisinde harici bir standart olarak kullanılır.
Amonyum sülfat, diamonyum fosfata çok benzeyen alev geciktirici bileşimlerde de kullanılmıştır. Alev geciktirici olarak malzemenin yanma sıcaklığını yükseltir, maksimum ağırlık kaybı oranlarını düşürür ve artık veya kömür üretiminde artışa neden olur.[13] Alev geciktirici etkinliği, amonyum sülfamat ile karıştırılarak arttırılabilir. Havadan yangın söndürmede kullanılmıştır.
Amonyum sülfat, bir ahşap koruyucu olarak kullanılmıştır. Ancak, higroskopik yapısı nedeniyle, metal bağlantı elemanı korozyonu, boyutsal dengesizlik ve yüzey kusurları ile ilgili problemler nedeniyle bu kullanım büyük ölçüde durdurulmuştur.
Üretimi
Amonyum sülfat, amonyak ve sülfürik asit arasında gerçekleşen reaksiyonla üretilir:
- 2 NH3 + H2SO4 → (NH4)2SO4
Amonyak gazı ve su buharı karışımı, 60 °C'de doymuş bir amonyum sülfat çözeltisi ve yaklaşık %2 - 4 serbest sülfürik asit içeren bir reaktöre verilir. Çözeltiyi asidik tutmak ve serbest asit seviyesini korumak için konsantre sülfürik asit eklenir. Reaksiyon ısısı, reaktör sıcaklığını 60 °C'de tutar. Kuru, toz amonyum sülfat, amonyak gazıyla dolu bir reaksiyon odasına sülfürik asit püskürtülerek oluşturulabilir. Reaksiyon ısısı, sistemde bulunan tüm suyu buharlaştırarak toz halinde bir tuz oluşturur. 1981 yılında yaklaşık 6.000 milyon ton üretildi.[1]
Amonyum sülfat ayrıca jipsten (CaSO4•2H2O) üretilir. Çok ince öğütülmüş jips, bir amonyum karbonat çözeltisine eklenir. Kalsiyum karbonat katı olarak çökelir ve çözeltide amonyum sülfat kalır.
- (NH4)2CO3 + CaSO4 → (NH4)2SO4 + CaCO3
Amonyum sülfat, volkanik fümerollerde nadir bulunan bir mineral olan mascagnit olarak ve bazı çöplüklerdeki kömür yangınları nedeniyle doğal olarak oluşur.[14]
2NH4OH+H2SO4=(NH4)2SO4+2H2O
Sülfürik ssit ve amonyum hidroksitin reaksiyonu ile de elde edilebilir
Özellikleri
Amonyum sülfat –49.5 °C'nin altındaki sıcaklıklarda ferroelektrik hale gelir. Oda sıcaklığında ortorombik sistemde, a = 7.729 Å, b = 10.560 Å, c = 5.951 Å hücre boyutlarıyla kristalleşir. Ferroelektrik duruma soğutulduğunda, kristalin simetrisi Pna21 uzay grubuna dönüşür.[15]
Reaksiyonları
Amonyum sülfat, 250 °C'nin üzerinde ısıtıldığında önce amonyum bisülfat oluşturarak ayrışır. Daha yüksek sıcaklıklarda ısıtma, amonyak, azot, kükürt dioksit ve suyla ayrışmaya neden olur.[16]
Güçlü bir asit (H2SO4) ve zayıf bir bazın (NH3) tuzu olarak, çözeltisi asidiktir; 0.1 M çözeltinin pH'ı 5.5'tir. Sulu çözeltide reaksiyonlar NH4+ ve SO4−2 iyonlarının reaksiyonlarıdır. Örneğin, baryum klorür eklenmesiyle, baryum sülfat çökelir. Süzülmüş sıvının buharlaştırılması amonyum klorürü verir.
Amonyum sülfat, çözeltisi metal sülfatların eşmolar çözeltileriyle karıştırıldığında ve çözelti yavaşça buharlaştırıldığında birçok çift tuz (amonyum metal sülfatlar) oluşturur. Üç değerlikli metal iyonları ile ferrik amonyum sülfat gibi şaplar oluşur. Çift metal sülfatlar, Tutton tuzu ve amonyum serik sülfat olarak bilinen amonyum kobaltöz sülfat, ferro diamonyum sülfat, amonyum nikel sülfat içerir.[1] Susuz çift amonyum sülfatları da Langbeinitler ailesinde bulunur. Üretilen amonyak keskin bir kokuya sahiptir ve zehirlidir.
Havadaki buharlaşan amonyum sülfat partikülleri dünya çapındaki partikül kirliliğinin yaklaşık %30'unu oluşturur.[17]
Mevzuat ve kontrol
Kasım 2009'da, Pakistan'ın Hayber Pahtunhva (NWFP) eyaleti, Upper Dir, Lower Dir, Svat, Çitral ve NWFP'nin Malakand bölgelerini içeren eski Malakand Bölgesinde amonyum sülfat, amonyum nitrat ve kalsiyum amonyum nitrat gübrelerinin militanlar tarafından patlayıcı yapmak için kullanıldığına dair raporların ardından bu gübrelere yasak getirdi. Ocak 2010'da bu maddeler aynı nedenle Afganistan'da yasaklandı.[18]
Kaynakça
- ^ a b c Karl-Heinz Zapp "Ammonium Compounds" in Ullmann's Encyclopedia of Industrial Chemistry, 2012, Wiley-VCH, Weinheim. DOI:10.1002/14356007.a02_243
- ^ Duong-Ly, Krisna C.; Gabelli, Sandra B. (1 Ocak 2014). "Salting out of Proteins Using Ammonium Sulfate Precipitation". Lorsch, Jon (Ed.). Methods in Enzymology. Laboratory Methods in Enzymology: Protein Part C. 541. Academic Press. ss. 85-94. doi:10.1016/B978-0-12-420119-4.00007-0. ISBN 9780124201194. PMID 24674064.
- ^ Duong-Ly, Krisna C.; Gabelli, Sandra B. (1 Ocak 2014). "Salting out of proteins using ammonium sulfate precipitation". Methods in Enzymology. 541: 85-94. doi:10.1016/B978-0-12-420119-4.00007-0. ISBN 9780124201194. ISSN 1557-7988. PMID 24674064.
- ^ Wingfield, Paul T. (5 Mayıs 2017). "Protein Precipitation Using Ammonium Sulfate". Current Protocols in Protein Science. 13 (1): A.3F.1-8. doi:10.1002/0471140864.psa03fs13. ISBN 978-0471140863. ISSN 1934-3655. PMC 4817497 $2. PMID 18429073.
- ^ "Ammonium Sulfate Calculator". EnCor Biotechnology Inc. 2013. 26 Ocak 2016 tarihinde kaynağından arşivlendi. Erişim tarihi: 2 Mart 2013.
- ^ ASTM Standard Specification for Rubber Concentrates D 1076-06
- ^ "Select Committee on GRAS Substances (SCOGS) Opinion: Ammonium sulfate". U.S. Food and Drug Administration. 16 Ağustos 2011. 11 Şubat 2012 tarihinde kaynağından arşivlendi. Erişim tarihi: 2 Mart 2013.
- ^ "Panera Bread › Menu & Nutrition › Nutrition Information Profile". 19 Ağustos 2009 tarihinde kaynağından arşivlendi. Erişim tarihi: 2 Mart 2013.
- ^ "Official Subway Restaurants U.S. Products Ingredients Guide". 14 Ağustos 2011 tarihinde kaynağından arşivlendi. Erişim tarihi: 2 Mart 2013.
- ^ Sarah Klein (14 Mayıs 2012). "Gross Ingredients In Processed Foods". The Huffington Post. 18 Mayıs 2012 tarihinde kaynağından arşivlendi. Erişim tarihi: 2 Mart 2013.
- ^ McCool, Pat. "Feeding Ammonium Sulfate to Form Combined Chlorine Residual" (PDF). The Kansas Lifeline. Kansas Rural Water Association. 6 Haziran 2019 tarihinde kaynağından arşivlendi (PDF). Erişim tarihi: 6 Haziran 2019.
- ^ "Vaccine Excipient & Media Summary" (PDF). Centers for Disease Control and Prevention (CDC). Şubat 2012. 5 Şubat 2011 tarihinde kaynağından arşivlendi (PDF). Erişim tarihi: 2 Mart 2013.
- ^ George, C. W.; Susott, R. A. (Nisan 1971). "Effects of Ammonium Phosphate and Sulfate on the Pyrolysis and Combustion of Cellulose". Research Paper INT-90. Intermountain Forest and Range Experiment Station: USDA Forest Service. 22 Eylül 2023 tarihinde kaynağından arşivlendi. Erişim tarihi: 11 Aralık 2022.
- ^ "Mascagnite". Mindat. 19 Ocak 2013 tarihinde kaynağından arşivlendi. Erişim tarihi: 2 Mart 2013.
- ^ Okaya, Y.; K. Vedam; R. Pepinsky (1958). "Non-isomorphism of ferroelectric phases of ammonium sulfate and ammonium fluoberyllate". Acta Crystallographica. 11 (4): 307. doi:10.1107/s0365110x58000803. ISSN 0365-110X.
- ^ Liu Ke-wei, Chen Tian-lang (2002). "Studies on the thermal decomposition of ammonium sulfate". Chemical Research and Application (Çince). 14 (6). doi:10.3969/j.issn.1004-1656.2002.06.038.
- ^ "Where Does Air Pollution Come From?". www.purakamasks.com (İngilizce). 15 Şubat 2019. 20 Şubat 2019 tarihinde kaynağından arşivlendi. Erişim tarihi: 20 Şubat 2019.
- ^ "PAKISTAN: 'Anti-terrorist' fertilizer ban hinders farmers". IRIN Humanitarian News and Analysis. 2010. 13 Mayıs 2013 tarihinde kaynağından arşivlendi. Erişim tarihi: 24 Nisan 2013.
Daha fazla bilgi için
- Properties: UNIDO and International Fertilizer Development Center (1998), Fertilizer Manual, Kluwer Academic Publishers, 0-7923-5032-4.
Dış bağlantılar
- Şablon:PPDB
- Calculators: surface tensions 22 Şubat 2020 tarihinde Wayback Machine sitesinde arşivlendi., and densities, molarities and molalities 22 Şubat 2020 tarihinde Wayback Machine sitesinde arşivlendi. of aqueous ammonium sulfate