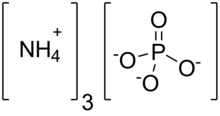
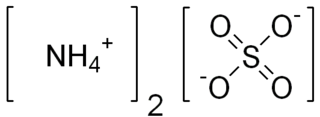Gübre, bitkinin beslenmesinde gerekli olan kimyasal elementleri sağlamak için toprağa ilave edilen herhangi bir madde.

Azot ya da nitrojen, simgesi N olan bir element olup atom numarası 7'dir. Renksiz, kokusuz, tatsız ve inert bir gazdır. Azot, dünya atmosferinin yaklaşık %78'ini oluşturur ve tüm canlı dokularında bulunur. Azot ayrıca, amino asit, amonyak, nitrik asit ve siyanür gibi önemli bileşikler de oluşturur.

Üre (Latince Urea Pura), organik bir bileşik. Formülü H2N-CO-NH2'dir. Karbonik asidin diamidi olan üre aynı zamanda karbamik asidin de amidi olduğundan karbamid adı ile de bilinir.

Thomas Graham, İskoç kimyacı.
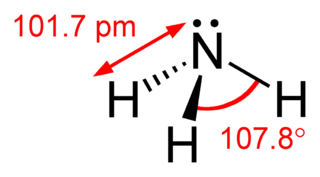
Amonyak, formülü NH3 olan; azot atomu ve hidrojen atomundan oluşan renksiz, keskin ve rahatsız edici kokulu bir bileşiktir. OH- iyonu içermediği hâlde suda zayıf baz özelliği gösterir. Bir amonyak molekülü, bir azot ve üç hidrojen atomundan oluşur. Oda sıcaklığında gaz hâlde bulunan bileşiğin ticari formu sulu çözeltiyi içermektedir.

Kimyasal bileşik, kimyasal bağlarla bir arada tutulan birden fazla kimyasal elementin atomlarını içeren birçok özdeş molekülden oluşan kimyasal maddedir. Dolayısıyla tek bir elementin atomlarından oluşan bir molekül bileşik değildir. Bir bileşik, diğer maddelerle etkileşimi içerebilen kimyasal reaksiyonla farklı bir maddeye dönüştürülebilir. Bu süreçte atomlar arasındaki bağlar kırılabilir ve/veya yeni bağlar oluşabilir.
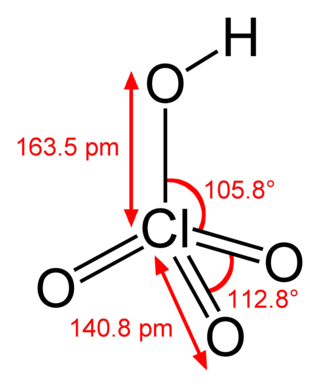
Perklorik asit, HClO4, suda çözünebilen renksiz bir sıvı olan bir klor oksoasididir. Sülfürik asit ya da nitrik asit ile kıyaslanabilecek kadar güçlü bir asittir. Perklorik asit bir süper asittir ancak en güçlü Brønsted-Lowry asidi değildir (en güçlüsü HSbF6 ya da floroantimonik asittir). Asidin pKa'sı −7'dir.
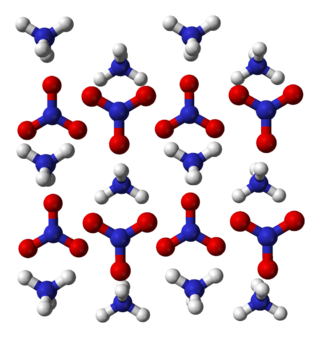
Amonyum nitrat, amonyum ve nitrat iyonlarından oluşan, NH4NO3 formülüne sahip yüksek patlayıcı bir kimyasal bileşiktir. Higroskopik özellikte ve beyaz kristal bir katı olarak hidrat oluşturmasa da suda çok çözünür. Ağırlıklı olarak, tarımda yüksek azotlu gübre olarak kullanılmaktadır. 2017 yılında küresel üretimi 21.6 milyon ton olarak tahmin edildi.
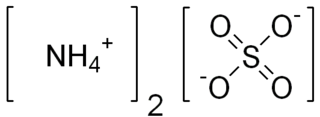
Amonyum sülfat, (NH4)2SO4 formülüne ve çok sayıda ticari kullanıma sahip bir inorganik tuzdur. Toprak gübresi olarak yaygın bir şekilde kullanılır. %21 azot ve %24 kükürt içerir.
NPK oranı (veya N-P-K) azot (N), fosfor (P) ve potasyum (K) kimyasal elementlerinin oransal içeriğini gübre etiketlerinde göstermek için, gübrelerde yaygın olarak kullanılan bir işaretleme biçimidir. N değeri, gübredeki elementel azotun ağırlıkça yüzdesidir. Gübrede bulunan P2O5 ve K2O formundaki oksit miktarı, bu formlara okside olmuş bütün elementel fosfor ve potasyum miktarını gösterir.

Amonyum klorür ya da daha çok bilinen adıyla Nişadır, formülü NH4Cl olan bir kimyasal bileşiktir. Suda yüksek oranda çözünen, beyaz kristallere sahip bir tuzdur. Amonyum klorür çözeltileri hafif asidiktir. Doğada mineral halde bazı volkan bacalarının etrafında bulunan haline sal amonyak denir. Bazı tür meyan ballarında bir aroma maddesi olarak kullanılır. Nişadır, hidroklorik asit ve amonyak arasında gerçekleşen reaksiyonla sonucu oluşur.
Protonasyon, protonlanma veya protonlaşma; bir atom, molekül veya iyona proton (H+) eklenerek konjuge asidin oluşturulmasıdır. Bazı örnekleri:
- suyun sülfürik asit tarafından protonasyonu:
- H2SO4 + H2O
 H3O+ + HSO-4
H3O+ + HSO-4
- Karbokatyon oluşumunda izobütenin protonasyonu:
- (CH3)2C=CH2 + HBF4
 (CH3)3C+ + BF-4
(CH3)3C+ + BF-4
- Amonyak ve hidrojen klorür reaksiyonundan amonyum klorür oluşumunda amonyakın protonasyonu:
- NH3(g) + HCl(g) → NH4Cl(s)

Kloroplatinik asit (hekzakloroplatinik asit olarak da bilinir), [H3O]2[PtCl6](H2O)x (0≤x≤6) formülüne sahip bir inorganik bileşiktir. Kırmızı bir katı, genellikle sulu bir çözelti olarak önemli bir platin kaynağıdır. Genellikle kısaca H2PtCl6 olarak yazılsa da, hekzakloroplatinat anyonunun (PtCl62-) hidronyum (H3O+) tuzudur. Hekzakloroplatinik asit oldukça higroskopiktir.

Tellürik asit, Te(OH)6 formülüne sahip kimyasal bir bileşiktir. Sulu çözelti içinde devam eden oktahedral Te(OH)6 moleküllerinden oluşan beyaz bir katıdır. Rombohedral ve monoklinik olmak üzere iki formu vardır ve her ikisi de oktahedral Te(OH)6 molekülleri içerir. Tellürik asit, güçlü bazlara sahip tellürat tuzları ve zayıf bazlara sahip hidrojen tellürat tuzları veya sudaki tellüratların hidrolizi üzerine dibazik olan zayıf bir asittir.

Amonyum kromat (NH4)2CrO4 formülüne sahip bir tuzdur. Sarı, monoklinik kristallerden oluşur; amonyum hidroksit ve amonyum bikromattan yapılır; jelatin kaplamalar için hassalaştırıcı olarak fotoğrafçılıkta kullanılır. Genellikle fotoğrafçılıkta, tekstil baskısında ve kromat boyalarının yün üzerine sabitlenmesinde kullanılır. Bir analitik ayıraç, katalizör ve korozyon önleyici olarak da kullanılır. Suda çözünür ve uygulandığında, mukoza, gözler, solunum sistemi, deri, vb. yerlerde tahrişe neden olabilir. Uzun süreli temastan sonra ciltte hassasiyete neden olabilir. Kanserojen (kansere neden olan) olduğu da bilinmektedir. Doku yaralanmaları ile karaciğer ve böbreklerde hasara neden olabilir.
Nitrofosfat işlemi 1927 yılında Norveç'in Odda belediyesinde Erling Johnson tarafından icat edilen azotlu gübrelerin endüstriyel üretimi için bir yöntemdi.

Diamonyum fosfat (DAP; IUPAC adı diamonyum hidrojen fosfat; kimyasal formülü (NH4)2(HPO4) olan amonyak]] ve fosforik asitin reaksiyonu ile üretilebilen bir dizi suda çözünür amonyum fosfat tuzlarından biridir.

Monoamonyum fosfat (MAP) olarak bilinen amonyum dihidrojen fosfat (ADP), (NH4)(H2PO4) kimyasal formülüne sahip bir kimyasal bileşiktir. MAP tarımsal gübrelerin ve bazı yangın söndürücülerin önemli bir bileşenidir. Optik ve elektronik alanlarında da önemli kullanımları vardır.

Sal amonyak, amonyum klorürden oluşan, formülü NH4Cl olan, nadir bulunan doğal bir mineraldir. Nişadır'ın mineral halidir ve tepkime sonucu değil, doğal olarak oluşur. İzometrik-heksoktahedral sınıfında renksiz, beyaz veya sarı-kahverengi kristaller oluşturur.

Amonyum hidrojen sülfat olarak da bilinen amonyum bisülfat, (NH4) HSO4 formülüne sahip beyaz, kristalimsi bir katıdır. Bu tuz, sülfürik asidin amonyakla yarı nötralizasyonunun ürünüdür.