
Mineral, doğal şekilde oluşan, homojen, belirli kimyasal bileşime sahip inorganik kristalleşmiş katı bir maddedir. Buna göre minerallerin özellikleri şöyledir; doğal olarak oluşur, herhangi bir parçası bütününün özelliklerini taşır, belirli bir kimyasal formülü vardır, katı hâlde olup nadiren sıvıdır ve inorganiktir.

Karbon, doğada yaygın bulunan ametal kimyasal elementtir. Evrende bolluk bakımından altıncı sırada yer alan karbon, kızgın yıldızlarda hidrojenin termonükleer yanmasında temel rol oynar. Dünyada hem doğal halde, hem de başka elementlerle bileşik halinde bulunan karbon, ağırlık olarak Dünya'nın yerkabuğunun yaklaşık %0,2'sini oluşturur. En arı (katışıksız) biçimleri elmas ve grafittir; daha düşük arılık derecelerinde maden kömürünün, kok kömürünün ve odun kömürünün bileşeni olarak bulunur. Atmosferin yaklaşık % 0,05'ini oluşturan ve bütün doğal sularda erimiş olarak bulunan karbon dioksit, kireç taşı ve mermer gibi karbonat mineralleri, kömürün, petrolün ve doğalgazın başlıca yapıtaşları olan hidrokarbonlar, en bol bulunan bileşikleridir.
Ametal, metal özelliği göstermeyen elementlerdir. Isıyı ve elektrik akımını iletmek gibi metallere özgü özellikleri göstermezler. Ayrıca kendi aralarındaki ortak özellikleri yok denecek kadar azdır. Genellikle karbon, azot, fosfor, oksijen, kükürt, selenyum, flor, klor, brom, iyot ve soy gaz elementlerine ametal denir.

Fotosentez, bitkiler ve diğer canlılar tarafından, ışık enerjisini organizmaların yaşamsal eylemlerine enerji sağlamak için daha sonra serbest bırakılabilecek kimyasal enerjiye dönüştürmek için kullanılan bir işlemdir. Bu kimyasal enerji, karbondioksit ve sudan sentezlenen şekerler gibi karbonhidrat moleküllerinde depolanır.

Fosfor, simgesi P ve atom numarası 15 olan ve insan vücudunda kalsiyumdan sonra en fazla bulunan kimyasal elementtir.

Kalay, periyodik cetvelde atom numarası 50 olan elementtir. Simgesi Sn olup Latince stannum dan gelir. Gümüşümsü gri renktedir. Havada kolaylıkla okside olmaz, korozyona karşı dirençlidir. Bu özelliğinden ötürü diğer metallerin kaplanmasında kullanılır. Tarihçesi MÖ 3000 yıllarına dayanır. Antik Mısır'da ve Mezopotamya'da bronz alaşımında kalay kullanılmıştır.

Elmas, bilinen en sert maddelerden biridir ve değerli bir taştır. Karbon elementinin bir modifikasyonu grafit, diğeri ise elmastır.

Klor, VIIA grubunda bulunan hafif, keskin kokulu, yeşilimsi sarı renkli, tahriş edici ve zehirleyici bir gaz. Havadan 2,5 kat ağır olan klor ilk zamanlar bir bileşik olarak kabul ediliyordu. Klor ilk olarak 1774 yılında Carl Wilhelm Scheele tarafından keşfedildi. 1810 yılında ise bugünkü ismi Humphry Davy tarafından verildi.
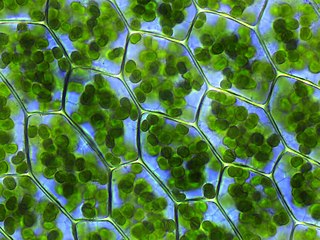
Kloroplast, fotosentezin gerçekleştiği sitoplazmik organeldir. Bitkilerin sadece yeşil kısımlarında bulunur. Bitkide besin ve oksijen üretilmesini sağlar. Genellikle yeşil renkli olduğu için bitkilerin çoğunun yeşil renkli olmasının temel sebebidir. Güneş enerjisini moleküler bağlar halinde saklayabilen tek yapı kloroplastlardır ve senede bu yolla dünyada 200 milyar ton organik madde üretilmektedir. Fotosentez yapma yeteneği kazanmış bir çekirdeksiz ve organelsiz ilkin hücre ve heterotrof (adrıbeslek) canlıların içerisine girerek simbiyoz yaşama uymuş bu şekilde kloroplastları meydana getirmiştir. Yani mavi algler kloroplastların evrimsel olarak atasıdır.

Karbondisülfür, formülü CS2 olup, yanabilen, hemen hemen renksiz olan, oldukça zehirli bir sıvı. Genel kanıya göre inorganik bileşik olarak kabul edilir. Ticari karbondisülfürün kokusu safsızlık kaynaklı olup, çürük lahana veya yumurta kokusuna benzerken saf karbondisülfürün kokusu etere benzer. Karbondisülfür -108,6 °C'de donar, 46,3 °C'de kaynar. Yoğunluğu 1,261 g/cm³'tür. Suda az çözündüğü hâlde alkol, eter ve karbon tetraklorürde çok çözünür.

Grafit ya da karataş yumuşak, yağlı, kâğıt üzerinde iz bırakan, gri-siyah renkli katı bir maddedir. Grafit, yağ haline getirilip makinelerde, çalışan parçaların birbirine sürtünürken aşınmasını azaltmak ya da engellemek amacıyla yağlayıcı olarak kullanılır. Adını, yazı yazmakta kullanılmasından almaktadır; "grafit" Yunanca grafein köküne, mineralleri belirtmekte kullanılan -it ekinin eklenmesiyle elde edilmiş bir sözcüktür. Kurşun kalemlerin içindeki uç, içine kil katılarak sertleştirilmiş grafittir.

Karabarut, kükürt, odun kömürü ve potasyum nitratın bir karışımıdır. Kükürt kullanılmadan yapılabilirse de, bu şekilde yapılan karabarut, kükürt kullanılarak yapılan kadar güçlü olmaz. Çok hızlı yanarak karbondioksit, su ve azottan ibaret sıcak bir gaz hacmi ve potasyum sülfürden oluşan katı bir artık bırakır. Yanma özelliklerinden dolayı ortaya çıkan sıcaklık ve gaz hacmi, barutun ateşli silahlarda itici yakıt ve havai fişeklerde piroteknik bileşim olarak kullanımına yol açmıştır. Modern ateşli silahlarda karabarut yerine dumansız barut kullanılır. Antika ateşli silahlarda çoğunlukla karabarut kullanılır.

Kalsiyum karbonat, halk arasında kireç taşı olarak bilinen bir tür kimyasal bileşiktir. Bileşik formülü CaCO3 şeklindedir. Bu bileşik doğada en fazla eski kayaçlarda ve deniz kabuklarında bulunur. Kalsiyum karbonat, antiasitlerin bir üyesi olsa da, fazlası biyolojik olarak zararlıdır.

Karbon Nanotüp, karbon elementinin uzunluk-çap oranı 28x106:1 olan allotropu. Bu oran başka herhangi bir malzemenin sahip olabileceğinden daha büyüktür. Tek katmanlı (tek duvarlı) ya da çok katmanlı (çoklu duvarlı) karbon nanotüpler mevcuttur. Karbon nanotüplerin yapısını açıklayabilecek en basit model tek duvarlı bir tüp için şu şekildedir: Tek sıra karbon atomundan oluşan bir grafen katmanının, silindir şeklinde bükülerek uçlarının birleştirildiği ve grafen içerisindeki bağların aynısından oluşturulduğu düşünülürse bu yapı tek duvarlı bir karbon nanotüple aynı yapı olur. Nanoteknolojide karbon elementinin allotropu olan grafitten yapay olarak üretilir.

Grafen, karbon atomunun bal peteği örgülü yapılarından bir tanesine verilen isimdir.

Fiziksel bilimlerde faz; bir malzemenin fiziksel özelliklerinin her noktasında aynı olduğu bölgedir/alandır. Fiziksel özelliklerinin örneklerinden üç tanesi, yoğunluk içermesi, mıknatıslanma ve kimyasal bileşimi indeksi. Basit bir açıklama ile bir faz fiziksel olarak ayrı, kimyasal olarak yeknesak ve (genellikle) mekanik ayrılabilir malzemeli bir bölge olmasıdır. Bir cam kavanoz buz ve sudan oluşan bir sistemde, buz küpleri birinci faz, su ikinci faz ve suyun üstünde bulunan nem ise üçüncü fazdır. Cam kavanoz ise başka bir ayrı aşamasıdır. Faz terimi bazen maddenin hali olarak eş anlamlı bir şekilde kullanılabilir. Ancak bir maddenin aynı halde çok sayıda karışmayan fazı olabilir. Ayrıca, faz terimi bazen bir faz diyagramı için üzerinde sınır ile basınç ve sıcaklık gibi durum değişkenler açısından sınırı çizilmiş denge durumunda bir dizi oluşturmak için kullanılır. Faz sınırları gibi katı veya başka bir kristal yapısından daha ince değişikliğine sıvıdan bir değişiklik olarak maddenin organizasyon değişiklikleriyle ilgili olduğundan bu son kullanım durumuna eş anlamlısı olarak "faz" kullanımına benzer. Ancak, madde ve faz diyagramı kullanımların hali yukarıda verilen ve amaçlanan anlam terim kullanıldığı bağlamdan kısmen tespit edilmelidir resmi tanımı ile orantılı değildir. Fazın çeşitleri Farklı fazlar, gaz, sıvı, katı, plazma veya Bose-Einstein yoğuşma ürünü olarak maddenin farklı durumlar olarak tarif edilebilir. Maddenin katı ve sıvı formda diğer haller arasındaki faydalı mezofazlar.

Bir Karbon gezegeni, oksijenden daha fazla karbon içeren teorik bir gezegendir. Karbon, evrende hidrojen, helyum ve oksijenden sonra kitlesel olarak dördüncü en bol elementtir.

Yöresizleşmiş elektronlar veya delokalize elektronlar bir katı metal, iyon veya molekülde bulunan elektronların tek bir atom veya kovalent bağ ile ilişkili olmamasını tanımlar.
Metalurji biliminde faz terimi, fazın belirli bir kimyasal bileşime, farklı bir atomik bağ ve element düzenine sahip olduğu fiziksel olarak homojen bir madde durumunu belirtmek için kullanılmaktadır. Bir alaşım içinde aynı anda iki veya daha fazla farklı faz mevcut olabilmektedir. Bir alaşım içindeki her fazın kendine özgü fiziksel, mekanik, elektriksel ve elektrokimyasal özellikleri vardır. Bir alaşımda bulunan fazlar, alaşım bileşimine ve alaşımın maruz kaldığı ısıl işleme bağlıdır. Faz diyagramları, belirli bir sıcaklıkta tutulan belirli bir alaşımda bulunan fazların grafiksel temsilleridir. Faz diyagramları, belirli bir ısıl işleme tabi tutulmuş bir alaşımda meydana gelen faz değişikliklerini tahmin etmek için kullanılabilmektedir. Bu önemlidir çünkü bir metal bileşenin özellikleri metalde bulunan fazlara bağlıdır. Faz diyagramları, belirli bir bileşime sahip alaşımların seçimi ve belirli özellikler üretecek ısıl işlem prosedürlerinin tasarımı ve kontrolü için metalurji uzmanları tarafından kullanılmaktadır. Ayrıca kalite sorunlarını gidermek için kullanılırlar.
Kalsinasyon, katı kimyasal bileşiklerin ısıl işlemine atıfta bulunur; bu sayede bileşik, genellikle safsızlığı veya uçucu maddeleri uzaklaştırmak ve/veya termal ayrışmaya maruz kalmak amacıyla, ortamdaki sınırlı oksijen kaynağı altında erimeden yüksek sıcaklığa yükseltilir.

















