
Hidrojen, sembolü H, atom numarası 1 olan kimyasal bir element. Standart sıcaklık ve basınç altında renksiz, kokusuz, metalik olmayan, tatsız, oldukça yanıcı ve H2 olarak bulunan bir diatomik gazdır. 1,00794 g/mol'lük atomik kütlesi ile tüm elementler arasında en hafif olanıdır. Periyodik cetvelin sol üst köşesinde yer alır. Hidrojenin adı, Yunancada "su oluşturan" anlamına gelen ὑδρογόνο'dan (idrogono) kelimesinden gelir.

Elektron dizilimi, atom fiziği ve kuantum kimyasında, bir atom ya da molekülün elektronlarının atomik ya da moleküler orbitallerdeki dağılımıdır. Örneğin Neon atomunun elektron dizilimi 1s2 2s2 2p6 olarak gösterilir.

İzotoplar, periyodik tabloda aynı atom numarasına ve konuma sahip olan ve farklı nötron sayıları nedeniyle nükleon sayıları bakımından farklılık gösteren iki veya daha fazla atom türüdür. Belirli bir elementin tüm izotopları neredeyse aynı kimyasal özelliklere sahipken, farklı atomik kütlelere ve fiziksel özelliklere sahiptirler. İzotop terimi, "aynı yer" anlamına gelen Yunan kökenli isos ve topos 'den oluşur; isimin anlamı ise, tek bir elementin farklı izotoplarının periyodik tabloda aynı pozisyonda yer alması anlamına gelir. Margaret Todd tarafından 1913 yılında Frederick Soddy'ye öneri olarak sunulmuştur.

Zehirlenme, kimyasal bir maddenin canlı organizma üzerindeki patolojik etkisidir. Görece küçük miktarlarda kimyasal ya da biyokimyasal etki gösteren zehir, süresi ve ağırlığı değişebilen bir hastalık haline ya da ölüme yol açar. Adli tıp uzmanları, zehirlenme olgularını 3 orijine ayırarak inceler:
- Kaza
- İntihar
- Cinayet

Demir, simgesi Fe ve atom numarası 26 olan kimyasal bir elementtir.

Çinko, sembolü Zn, atom numarası 30 olan kimyasal bir elementtir. Oda sıcaklığında hafif kırılgan bir metaldir ve oksidasyon giderildiğinde parlak gri bir görünüme kavuşur. Periyodik tablonun 12. (IIB) grubunun ilk elementidir. Bazı açılardan çinko kimyasal olarak magnezyuma benzer: her iki element de yalnızca bir normal oksidasyon durumu (+2) gösterir ve Zn2+ ve Mg2+ iyonları benzer boyuttadır. Çinko, Dünya kabuğundaki en bol bulunan 24. element olup beş kararlı izotopu vardır. En yaygın çinko cevheri, bir çinko sülfür minerali olan sfalerittir.

Kadmiyum, kimyasal simgesi Cd olan, gümüş beyazlığında, elektrik, seramik, pil ve akü sanayisinde kullanılan yumuşakça, kanserojen, toksik bir ağır metal element. Kadmiyum, çinko bileşikleriyle beraber doğada kadmiyum sülfür olarak bulunur. Çinko, kurşun ve bakırın yan ürünü olarak üretilir.

Fransiyum, sembolü Fr ve atom numarası 87 olan kimyasal element. Bilinen elementler içinde en az elektronegatifliğe sahip olan ve astatinden sonra doğada en az bulunan elementtir. Astatin, radyum ve radona bozunan fransiyumun radyoaktivitesi son derece yüksektir. Bir alkali metal olarak bir tane değerlik elektronuna sahiptir.

Mangan veya Manganez kimyasal bir elementtir. Simgesi Mn ve atom numarası 25'tir.

Bizmut sembolü Bi ve atom numarası 83 olan kimyasal elementtir. 15. grupta, 6. periyotta yer alan bir metaldir. Pentavalent geçiş metalidir ve azot grubundadır; aynı gruptaki arsenik ve antimon ile benzerlik gösterir. Her ne kadar önemli ticari cevherler sülfür ve oksit formlarından oluşsa da elementer bizmut doğal olarak ortaya çıkabilir. Serbest element formundaki kurşunun %86'sı yoğunluğuna sahiptir. Yeni üretildiğinde gümüşi beyaz renkli ve kırılgan bir metaldir ancak yüzey oksidasyonu ona birçok renkte yanardöner renkler verebilir. Bizmut en doğal diyamanyetik elementtir ve metaller arasındaki en az termal iletkenlik değerlerinden birine sahiptir.
Neodimyum, sembolü Nd ve atom numarası 60 olan kimyasal bir elementtir. Lantanit serisinin dördüncü üyesidir ve nadir toprak metallerinden biri olarak kabul edilir. Havada ve nemde hızla kararan sert, hafif dövülebilir, gümüşi bir metaldir. Hızla oksitlenir ve +2, +3 ve +4 pembe, mor/mavi ve sarı bileşikler üretir. Elementlerin en karmaşık spektrumlarından birine sahip olduğu kabul edilir. Neodimyum, 1885 yılında praseodimyumu da keşfeden Avusturyalı kimyager Carl Auer von Welsbach tarafından keşfedildi. Monazit ve bastnäsite minerallerinde önemli miktarlarda bulunur. Neodimyum, doğal olarak metalik formda veya diğer lantanitlerle karışmamış olarak bulunmaz ve genel kullanım için rafine edilir. Neodimyum kobalt, nikel veya bakır kadar yaygındır ve Dünya'nın kabuğunda yaygın olarak dağılmıştır. Diğer birçok nadir toprak metalinde olduğu gibi, dünyadaki ticari neodimyumun çoğu Çin'de çıkarılmaktadır.

Magnezyum (Mg), gümüş beyazlığında bir metaldir ve genellikle alaşım maddesi olarak, yani başka metallerle karıştırılarak kullanılır. Kimyasal simgesi Mg, atom numarası 12; atom ağırlığı 24,312 olan bu element en hafif metallerden biridir ve bu özelliğiyle önem kazanmıştır. Toz halindeki magnezyum kolayca tutuşur ve parlak bir alevle yanar. Bu özelliği nedeniyle, elektrikli fotoğraf makinesi flaşları çıkmadan önce, magnezyum yakılarak flaşlı fotoğraflar çekilmiştir.
Süpernova nükleosentezi kuramı, süpernova patlamalarındaki farklı pek çok kimyasal elementin nasıl üretildiğini açıklamaya çalışır. İlk kez 1954 yılında Fred Hoyle tarafından geliştirilmiştir. Nükleosentez, diğer bir deyişle hafif elementlerin ağır elementlere ergimesi, patlayıcı oksijenin yanması ya da silikonun yanması esnasında ortaya çıkar. Bu birleşme tepkimeleri, silikon, sülfür, klor, argon, sodyum, potasyum, kalsiyum, skandiyum, titanyumun yanı sıra, vanadyum, krom, manganez, demir, kobalt ve nikel gibi demir zirve elementlerinin oluşumuna yol açar. Büyük yıldızlarda saf hidrojen ve helyumdan ergiyebildikleri için bunlara “primer elementler” denir. Süpernovalardan atılımları sonucu, yıldızlararası ortamda bollukları artar. Nikelden ağır elementler, r-süreci denen bir süreçte nötronların hızlı bir biçimde tutulmasıyla ortaya çıkarlar. Ancak bunlar primer kimyasal elementlerden oldukça azdır. Yetersiz miktarda bulunan ağır elementlerin nükleosentezine yol açtığı düşünülen diğer süreçler, rp-süreci olarak bilinen proton yakalanması ve gamma süreci olarak bilinen ışıl parçalanmadır. Işıl parçalanma, ağır elementlerin en hafif ve en nötron fakiri izotoplarını sentezler.

Nükleosentez, daha önceden var olan çekirdek parçacıklarından, esasen proton ve nötronlardan, yeni atomik çekirdeklerin yaratılması sürecidir. İlk atomik çekirdekler, Büyük Patlama'dan yaklaşık üç dakika sonra, Büyük Patlama nükleosentezi olarak bilinen sürecin sonunda oluşmuştur. Hidrojen ve helyumun ilk yıldızların bileşenlerini oluşturması ve kainatın bugünkü hidrojen/helyum oranı o zamanlara dayanır.
Nükleer bağlanma enerjisi, atomun çekirdeğini bileşenlerine ayırmak için gereken enerjidir. Bu bileşenler nötron, proton ve nükleondur. Bağ enerjisi genelde pozitif işaretlidir çünkü çoğu çekirdek parçalara ayrılmak için net bir enerjiye ihtiyacı vardır. Bu yüzden, genelde bir atomun çekirdeğinin kütlesi ayrı ayrı ölçüldüğünde daha azdır. Bu fark nükleer bağlanma enerjisidir ki bu enerji birbirini tutan bileşenlerin uyguladığı kuvvet tarafından sağlanır. Çekirdeği bileşenlerine ayırırken, kütlenin bir kısmı büyük bir enerjiye dönüştürülür bu yüzden bir kısım kütle eksilir, eksik kütlede bir fark yaratır çekirdekte. Bu eksik kütle, kütle eksiği diye bilinir ve çekirdek oluşurken çıkan enerjiye takabül eder.
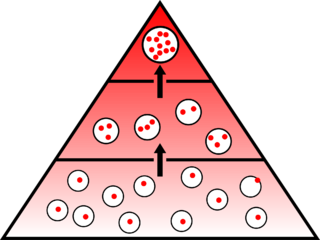
Biyobirikim ya da biyoakümülasyon, pestisit gibi toksinlerin ya da çevrede nadir bulunan yararlı ve gerekli oligoelementler gibi bazı kimyasal maddelerin bitkiler, hayvanlar, mantarlar ya da mikroorganizmalar gibi organizmaların canlı ya da cansız bölümlerinde ya da organizmalarının tamamında soğurularak birikmesini anlatan bir terimdir. Biyobirikim bir organizmanın muhtemelen toksik bir maddeyi katabolizma ya da boşaltım yolu ile yok etmesinden daha hızlı bir oranda soğurmasıyla ortaya çıkar. Dolayısıyla toksik maddenin çevrede ölçülmüş konsantrasyonu çok yüksek olmasa bile biyolojik yarı ömrü ne kadar uzunsa bu nedenle oluşabilen kronik zehirlenme riski o kadar büyüktür. Aynı organizmada görülen biyobirikim yaş ya da sağlık durumu gibi içsel faktörlerden olduğu kadar mevsim, çevrede bulunan besin miktarı, ortamın pH oranı gibi dışsal faktörlerden de oldukça önemli derecede etkilenir. Aynı tür içinde bazı bireyler genetik olarak biyobirikime daha çok ya da daha az yatkın olabilir ancak genel olarak bazı cinsler biyobirikime daha yatkındır; örneğin Agaricus türü mantarların cıva, kurşun, kadmiyum ve selenyum gibi elementleri çok iyi biriktirdikleri bilinmektedir. Biyobirikim, örneğin balıklar için modelleme yoluyla öngörülebilir. Biyodönüşüm kimyasal maddelerin organizmalarda oluian biyobirikimini önemli şekilde etkiler.

Çevre kimyası, doğal yerlerde meydana gelen kimyasal ve biyokimyasal olayların bilimsel bir araştırmasıdır. Potansiyel kirliliği kaynağında azaltmaya çalışan yeşil kimya ile karıştırılmamalıdır. Hava, toprak ve su ortamlarındaki kimyasal türlerin kaynakları, reaksiyonları, taşınması, etkileri ve kaderlerinin incelenmesi; ve insan aktivitesinin ve biyolojik aktivitenin bunlara etkisi olarak tanımlanabilir. Çevre kimyası, atmosfer, su ve toprak kimyasını içeren, aynı zamanda analitik kimyaya büyük ölçüde güvenen, çevre bilimi ve diğer bilim alanlarıyla ilgili olan disiplinlerarası bir bilimdir.

Ipomoea purpurea veya Kahkahaçiçeği Meksika ve Orta Amerika'ya özgü, Kahkahaçiçeğigiller familyası, Ipomoea cinsinden bir türdür.
Metal zehirlenmesi veya metal toksisitesi; belirli metallerin belirli biçim ve dozlarda yaşam üzerindeki zehirleyici etkisidir. Birtakım metaller, zehirli çözünür bileşikler oluşturduklarında zehirlidir. Birtakım metallerin biyolojik bir rolü yoktur, başka bir deyişle yaşam için zorunlu (esansiyel) minerallerden değildir veya belirli bir türevdeyken zehirlidir. Söz konusu metalin kurşun olması durumunda, kurşunun ölçülebilir herhangi bir miktarının sağlık üzerinde olumsuz etkileri olabilir. Metal zehirlenmesinin genellikle ağır metaller ile anlamdaş olduğu düşünülür, ancak berilyum ve lityum gibi daha hafif metaller de belirli durumlarda zehirli olabilir. Bütün ağır metaller özellikle zehirli değildir ve demir gibi bazı metaller canlıda çok önemli bir yer tutar. Metal zehirlenmesinin tanımı, anormal derecede yüksek dozlarda zehirli etki gösteren eser elementleri de kapsayabilir. Metal zehirlenmesinin tedavisi için şelasyon tedavisi bir seçenek olabilir; bu yöntem, metalleri vücuttan uzaklaştırmak için şelasyon ajanlarının uygulanmasını içine alan bir tekniktir.
Tıpta metaller organik sistemlerde teşhis ve tedavi amaçlı kullanılmaktadır. İnorganik elementler, metalloproteinler adı verilen enzimlerde kofaktörler olarak organik yaşam için de gereklidir. Metaller kıt veya çok miktarda olduğunda denge bozulmaktadır ve müdahaleli ve doğal yöntemlerle doğal haline döndürülmesi gerekmektedir.













