
Sodyum, periyodik cetvelde Na simgesi ile gösterilen ve atom numarası 11 olan element. Sodyum yumuşak ve kaygan bir metal olup alkali metaller grubuna aittir. Doğal bileşiklerin içinde bol miktarda bulunur. Yüksek oranda reaktiftir, sarı bir alevle yanar, su ile şiddetli reaksiyon verir ve havada hızla oksitlenir. Dolayısıyla, vazelin, gazyağı gibi hava ve su ile temasını kesecek bir ortamda saklanması gerekir.

Klor, VIIA grubunda bulunan hafif, keskin kokulu, yeşilimsi sarı renkli, tahriş edici ve zehirleyici bir gaz. Havadan 2,5 kat ağır olan klor ilk zamanlar bir bileşik olarak kabul ediliyordu. Klor ilk olarak 1774 yılında Carl Wilhelm Scheele tarafından keşfedildi. 1810 yılında ise bugünkü ismi Humphry Davy tarafından verildi.

Tanen, tannik asit olarak da bilinir. Tanenler polifenolik bileşikler olup, kolza, bakla, çay ve sorgumda gibi bitkilerden elde edilen, açık sarı-kahverengi toz, pul ya da süngersi bir kütle halindeki biçimsiz (amorf) maddelere verilen addır.

Lipit, tüm canlıların yapısında bulunan temel organik bileşiklerden biridir. Lipitler, doymuş ve doymamış yağlar olarak ayrılır. Doymamış yağlar, oda sıcaklığında sıvı hâlde bulunan lipitler; doymuş yağlar ise oda sıcaklığında katı hâlde bulunan lipitlerdir. Biyolojik önemi olan lipitler için yağ asitleri, nötr lipitler (trigliserit), fosfolipitler ve steroitler örnek gösterilebilir. Lipitler, insan ve hayvanların temel besinleri arasında yer alır.

Vanilin, kimyada 4-hidroksi-3-metoksibenzaldehit ismiyle bilinen, tabiî olarak vanilyanın meyvesinde glikozit halinde bulunan hoş kokulu bir madde. İğne kristaller hâlinde, renksiz, erime noktası 82 °C olan bu aromatik bileşik, alkolde, eterde ve yağlarda soğukta dahi çok iyi çözünür fakat kaynar suda çok az çözünür. Kapalı formülü C8H8O3 olan vanilinde hidroksi(-OH) ve karbon îl (-C=O) grupları bulunmaktadır. Vanilya bitkisinden elde edildiği gibi sentetik olarak da elde edilir.

Gliserin, diğer adı gliserol olan, sıvı hâlde bulunan polar organik bir trihidroksi alkoldür. Hafifçe tatlı, zehirli olmayan bir sıvıdır. Su ve etanol ile karışır; asetonda çözünür.

Asetilen (etin), bir tür hidrokarbondur. Üçlü bağ taşır ve formülü C2H2 şeklindedir. Alkin sınıfının ilk üyesidir.

Kimyada amid sözcüğü iki anlama sahiptir: - Birinci anlamıyla amid, bir azot atomuna (N) bağlı bir karbonil grubu bulunduran bir organik fonksiyonel grup veya bu gruba sahip bir bileşiktir. - İkinci anlamıyla amid, bir azot anyonudur.

Hidroklorik asit, hidrojen ve klor elementlerinden oluşan, oda sıcaklığı ve normal basınçta gaz hâlinde olan hidrojen klorürün sulu çözeltisine verilen ad. Halk arasında tuz ruhu olarak da bilinir. 9. yüzyılda simyacı Câbir bin Hayyân tarafından keşfedildi ve sonrasında simya alanında kullanıldı. Sanayi Devrimi sırasında, sanayideki önemi keşfedilen asit, önce Leblanc işlemi, sonrasında Solvay işlemi ile sanayi alanında üretilmeye başladı. Hidroklorik asit, tarihte yeni kolaylıkların keşfinde önemli roller üstlendi. Günümüzde PVC'den demir-çeliğe, organik madde üretiminden gıda sektörüne kadar hemen hemen tüm alanlarda hidroklorik asit kullanılmaktadır.

Sülfürik(VI) asit ya da halk arasında bilinen ismi ile zaç yağı, H2SO4, güçlü bir mineral asididir. Olası kâşifi 8. yüzyıl simyacısı Cabir bin Hayyan tarafından yenime uğratıcı, renksiz ve yoğunluğu yüksek sıvı olarak tanımlanmıştır. Suda her konsantrasyonda çözünebilir. Büyük ölçüde korozif oluşu, güçlü asidik yapısından ve dehidrasyon özelliğinden kaynaklanmaktadır.

Gümüş nitrat en önemli gümüş tuzudur. Renksiz ağır kristallerden oluşur. Tıpta dağlamak maksadıyla kullanılır ve antibakteriyel özelliği vardır. Bu özelliğinden dolayı siğil tedavisinde sıkça kullanılır. Ayrıca deriyi ve organik maddeleri karartmada tercih edilir. Deriyi kararttığından cehennem taşı ismini almıştır. Suda ve alkolde kolayca çözündüğünden birçok gümüş bileşiklerinin elde edilmesinde ilkel madde olarak kullanılır. En çok kullanıldığı yerler, başta fotoğrafçılık olmak üzere mürekkepler, saç boyası yapımı ve gümüş kaplamacılığıdır.bileşenleri gümüş ve nitrik asittir. Sentezi ise örnekteki formüle göre yapılır:
- Ag + 2 HNO3 → AgNO3 + NO2 + H2O

Kükürt trioksit, suyla tepkimeye girdiğinde sülfürik asit oluşturan zehirli bir gazdır. Formülü SO3 şeklindedir. Kükürtlü asidi oluşturan sülfit iyonu (SO3 2-) ile karıştırılmamalıdır.


Hipokloröz asit, HOCl formülüne sahip bir zayıf asittir.
Bir asidin kuvveti, onun içinde bulunduğu çözeltiye ne kadar proton (H+) verebildiğinin ölçüsüdür. Kuvvetli asitler %100 çözünürler ve bu çözünme iyonlaşarak gerçekleşir. Yani 1 mol HA kuvvetli asidi suda çözündüğünde 1 mol H+ ve onun eşlenik bazı A- 1 mol oluşur. Hidroklorik asit, hidroiyodik asit, hidrobromik asit, perklorik asit, nitrik asit ve sülfürik asit, kuvvetli asitlere örnektir.

Gümüş sülfat (Ag2SO4) gümüş kaplamada ve gümüş nitrat yerine boyanmayan madde olarak kullanılan gümüş iyonik bileşiği. Bu sülfat normal kullanım ve depolama durumunda kararlıdır fakat havaya ve ışığa maruz kaldığında kararır. Suda çok az çözünür.

Hidrojen bromür, HBr formülüne sahip iki atomlu moleküldür. Renksiz bir bileşik ve bir hidrojen halojenürdür. Hidrobromik asit, su içinde bir HBr çözeltisidir. Hem HBr'nin susuz hem de sulu çözeltileri, bromür bileşiklerinin hazırlanmasında ortak reaktiflerdir.
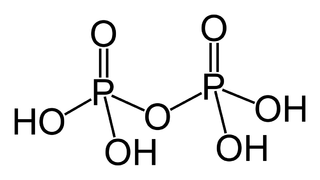
Difosforik asit olarak da bilinen pirofosforik asit, H4P2O7 formülüne sahip inorganik bir bileşik veya daha açıklayıcı olarak [(HO)2P(O)]2O'dur. Renksiz ve kokusuzdur, su, dietil eter ve etil alkolde çözünür. Susuz asit, 54.3 °C ve 71.5 °C'de eriyen iki polimorf içinde kristalleşir. Bileşik, polifosforik asit ve pirofosfat anyonunun konjugat asidinin bir bileşeni olması dışında özel olarak yararlı değildir. Pirofosforik asit anyonları, tuzları ve esterlerine pirofosfatlar denir.

Potasyum iyodat (KIO3) bir kimyasal bileşiktir. K+ ve IO3− iyonlarından oluşur. Potasyum iyodat oksitleyici bir maddedir ve bu nedenle yanıcı maddelerle temas ettiğinde yangına neden olabilir. Suda ve sülfürik asitte çözünür; alkolde çözünmez.

Magnezyum nitrat Mg(NO3)2(H2O)x formülüne sahip inorganik bileşikleri ifade eder. Formüldeki, x = 6, 2 ve 0 olabilir. Hepsi beyaz renkli katılardır. Susuz madde higroskopiktir, havada bekletildiğinde hızlı bir şekilde hekzahidrat oluşturur. Bütün tuzları hem suda hem de etanolde çok çözünür.

Klor triflorür, formülü ClF3 olan interhalojen bir bileşiktir. Zehirli, aşındırıcı ve aşırı reaktiftir. Gaz hâlindeyken renksizken sıvı hâlindeyken solgun yeşilimsi sarı renktedir. Yarı iletken sanayiinde, nükleer yakıtların yeniden işlenmesinde, roket itici yakıtlarında ve diğer endüstriyel alanlarda kullanılır. Benzen, toluen, eter, alkol, asetik asit, hekzan gibi çözücüler ile reaksiyona girer. Karbon tetraklorürde çözünür ancak yüksek konsantrasyonlarda patlayıcı olabilir.

![Top ve çubuk modeli [1][2]](https://upload.wikimedia.org/wikipedia/commons/thumb/9/99/3-Aminobenzoic-acid-3D-balls.png/110px-3-Aminobenzoic-acid-3D-balls.png)



















