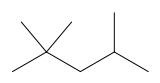
2,2,4-Trimetilpentan
 | |
 | |
 | |
| Adlandırmalar | |
|---|---|
Tercih edilen IUPAC adı 2,2,4-Trimetilpentan[1] | |
| Tanımlayıcılar | |
CAS numarası | |
3D model (JSmol) | |
| 1696876 | |
| ChEBI | |
| ChEMBL | |
| ChemSpider | |
| ECHA InfoCard | 100.007.964 |
| EC Numarası |
|
| MeSH | 2,2,4-trimethylpentane |
PubChem CID | |
| RTECS numarası |
|
| UNII | |
| UN numarası | 1262 |
CompTox Bilgi Panosu (EPA) | |
| |
| |
| Özellikler | |
| Kimyasal formül | C8H18 |
| Molekül kütlesi | 114,23 g mol−1 |
| Görünüm | renksiz sıvı |
| Koku | petrol benzeri |
| Yoğunluk | 0.692 g cm−3 |
| Erime noktası | 16.304 °C; 29.379 °F; 16.577 K |
| Kaynama noktası | 36.972 °C; 66.581 °F; 37.245 K |
| log P | 4.373 |
| Buhar basıncı | 5.5 kPa (at 21 °C) |
Henry yasası sabiti (kH) | 3.0 nmol Pa−1 kg−1 |
| UV-vis (λmax) | 210 nm |
| -98.34·10−6 cm3/mol | |
| Kırınım dizimi (nD) | 1.391 |
| Termokimya | |
Isı sığası (C) | 242.49 J K−1 mol−1 |
Standart molar entropi (S⦵298) | 328.03 J K−1 mol−1 |
Standart formasyon entalpisi (ΔfH⦵298) | −260.6 to −258.0 kJ mol−1 |
Standart yanma entalpisi (ΔcH⦵298) | −5462.6 to −5460.0 kJ mol−1 |
| Tehlikeler | |
| GHS etiketleme sistemi: | |
| Piktogramlar |     |
| İşaret sözcüğü | DANGER |
| Tehlike ifadeleri | H225, H304, H315, H336, H410 |
| Önlem ifadeleri | P210, P261, P273, P301+P310, P331 |
| NFPA 704 (yangın karosu) | |
| Parlama noktası | [dönüştürme: geçersiz sayı] |
Kendiliğinden tutuşma sıcaklığı | 396 °C (745 °F; 669 K) |
| Patlama sınırları | 1.1–6.0% |
| Benzeyen bileşikler | |
Benzeyen alkanes |
|
| Aksi belirtilmediği sürece madde verileri, Standart sıcaklık ve basınç koşullarında belirtilir (25 °C [77 °F], 100 kPa). | |
2,2,4-trimetilpentan, izooktan veya izo-oktan, (CH3)3CCH2CH(CH3)2 kimyasal formülüne sahip bir organik bileşiktir. Oktan (C8H18) izomerlerinden biridir. Bu özel izomer, oktan derecelendirme ölçeğindeki standart 100 noktadır (sıfır noktası n- heptandır ). Yakıtın vuruntu direncini artırmak için nispeten büyük oranlarda sıkça kullanılan, önemli bir benzin bileşenidir.[2]
Eğer 'izo'nun standart anlamı takip edilirse, izooktan adı izomer 2-Metilheptan için kullanılmalıdır. Fakat, 2,2,4-trimetilpentan, oktanın bugüne kadar kullanılan en önemli izomeridir ve bu nedenle, tarihsel olarak, bu isim verilmiştir.[3]
Üretimi
İzooktan, petrol endüstrisinde izobütenin izobütan ile alkilasyonu yoluyla büyük ölçekte üretilir. İşlem, asit katalizörleri varlığında alkilasyon birimlerinde gerçekleştirilir.[4]

Ayrıca amberlist katalizörü kullanılarak dimerizasyon yoluyla izobütilenden de bir izo-okten karışımı üretilebilir. Bu karışımın hidrojenlenmesi 2,2,4-trimetilpentan üretir.[5]
Tarihçe
Motor çarpması, içten yanmalı motorlarda yüksek sıkıştırma oranları sırasında meydana gelebilecek istenmeyen bir işlemdir. 1926'da Graham Edgar, benzine farklı miktarlarda n-heptan ve 2,2,4-trimetilpentan ekledi ve 2,2,4-trimetilpentan eklendiğinde vuruşun durduğunu keşfetti. Bu çalışma oktan derecelendirme ölçeğinin kökeni idi.[6] 2,2,4-trimetilpentan kullanan test motorları, 100 oktan olarak standartlaştırılmış belirli bir performans vermiştir. Heptan kullanarak aynı şekilde çalışan aynı test motorları, 0 oktan olarak standartlaştırılmış bir performans vermiştir. Diğer tüm bileşikler ve bileşik karışımları daha sonra bu iki standarda göre derecelendirildi ve oktan sayıları verildi.
Emniyet
Tüm hidrokarbonlarda olduğu gibi 2,2,4-trimetilpentan yanıcıdır.[7]
Ayrıca bakınız
- Petrol rafinerisi
- Çarpma karşıtı ajanlar
Kaynakça
- ^ "2,2,4-trimethylpentane - Compound Summary". PubChem Compound. Identification and Related Records: National Center for Biotechnology Information. 26 Mart 2005. 19 Haziran 2013 tarihinde kaynağından arşivlendi. Erişim tarihi: 11 Mart 2012.
- ^ Werner Dabelstein, Arno Reglitzky, Andrea Schütze, Klaus Reders (2007). "Automotive Fuels". Ullmann's Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. doi:10.1002/14356007.a16_719.pub2.
- ^ Clayden, Jonathan (2005). Organic chemistry (Reprinted (with corrections). ed.). Oxford [u.a.]: Oxford Univ. Press. p. 315. ISBN 978-0-19-850346-0.
- ^ Bipin V. Vora, Joseph A. Kocal, Paul T. Barger, Robert J. Schmidt, James A. Johnson (2003). "Alkylation". Kirk‐Othmer Encyclopedia of Chemical Technology. doi:10.1002/0471238961.0112112508011313.a01.pub2.
- ^ İzobütilen 6 Ağustos 2014 tarihinde Wayback Machine sitesinde arşivlendi., Amberlyst.com'un boyutlandırılması
- ^ Yakıtlar ve yağlayıcılar el kitabı, Cilt 1, George E. Totten, Steven R. Westbrook, Rajesh J. Shah, sayfa 62
- ^ 2,2,4-Trimethylpentane 24 Eylül 2015 tarihinde Wayback Machine sitesinde arşivlendi., Bütünleşik Risk Bilgi Sistemi, ABD Çevre Koruma Ajansı
Dış bağlantılar
 Wikimedia Commons'ta Isooctane ile ilgili çoklu ortam belgeleri bulunur
Wikimedia Commons'ta Isooctane ile ilgili çoklu ortam belgeleri bulunur- Uluslararası Kimyasal Güvenlik Kartı 0496 22 Nisan 2019 tarihinde Wayback Machine sitesinde arşivlendi.