
Propanol, üç karbonlu doymuş alifatik alkol. Normal propanolün (n-propanol) formülü CH3CH2CH2OH olup buna 1-propanol de denir. Renksiz, akışkan, keskin ve hoş olmayan bir kokuya sahiptir. Su ve organik çözücülerde çözünür. n-Propanol, karbon monoksit ve hidrojenden metanol elde ederken, propan ve bütanın oksidasyonu esnasında ve Fischer-Tropsch reaksiyonunda yan ürün olarak elde edilir. Etilen, karbon monoksit ve hidrojenden okso sentezi ile imalatı cezbedici bir yoldur. n-propanol en çok çözücü ve kimyasal ara madde olarak kullanılır.

Naftalin veya naftalen, kapalı kimyasal formülü C10H8 olan, aromatik hidrokarbondur.

Asetilen (etin), bir tür hidrokarbondur. Üçlü bağ taşır ve formülü C2H2 şeklindedir. Alkin sınıfının ilk üyesidir.
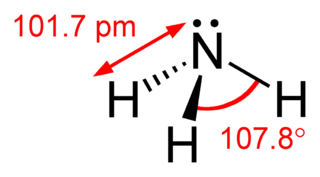
Amonyak, formülü NH3 olan; azot atomu ve hidrojen atomundan oluşan renksiz, keskin ve rahatsız edici kokulu bir bileşiktir. OH- iyonu içermediği hâlde suda zayıf baz özelliği gösterir. Bir amonyak molekülü, bir azot ve üç hidrojen atomundan oluşur. Oda sıcaklığında gaz hâlde bulunan bileşiğin ticari formu sulu çözeltiyi içermektedir.

Formik asit, HCOOH, tek karbonlu karboksilik asittir. Metanoik asit olarak da bilinir. Formik asit, karbonil karbonuna bağlı alkil grubu içermemesiyle en basit karboksilli asit özelliği taşır. Hem aldehit hem de karboksilik asit özelliğine sahiptir.

Kostik ve kostik soda ( ) olarak da bilinen sodyum hidroksit (kostik soda veya sud kostik de denir), NaOH formülüne sahip bir inorganik bileşiktir. Sodyum katyonları Na+ ve hidroksit anyonları OH- içeren beyaz renkli katı bir iyonik bileşiktir.
) olarak da bilinen sodyum hidroksit (kostik soda veya sud kostik de denir), NaOH formülüne sahip bir inorganik bileşiktir. Sodyum katyonları Na+ ve hidroksit anyonları OH- içeren beyaz renkli katı bir iyonik bileşiktir.

Amonyum klorür ya da daha çok bilinen adıyla Nişadır, formülü NH4Cl olan bir kimyasal bileşiktir. Suda yüksek oranda çözünen, beyaz kristallere sahip bir tuzdur. Amonyum klorür çözeltileri hafif asidiktir. Doğada mineral halde bazı volkan bacalarının etrafında bulunan haline sal amonyak denir. Bazı tür meyan ballarında bir aroma maddesi olarak kullanılır. Nişadır, hidroklorik asit ve amonyak arasında gerçekleşen reaksiyonla sonucu oluşur.

Sodyum azotür, NaN3 formüllü inorganik bileşiktir. Bu renksiz tuz çoğu araba hava yastığı sisteminde kullanılan gaz oluşturucusudur. Diğer azotür bileşiklerinin hazırlanabilmesi için de kullanılır. İyonik bir maddede olan sodyum azotür, suda oldukça iyi çözünür ve güçlü bir toksiktir.

Kalsiyum arsenat, Ca3(AsO4)2 formülüne sahip inorganik bileşiktir. Renksiz bir katı, başlangıçta bir pestisit ve mikrop öldürücü madde olarak kullanılmıştır.Kurşun arsenat ile karşılaştırıldığında, suda oldukça çözünür, bu da daha toksik hale getirir. Mineraller Rauenthalit Ca3(AsO4)2·10H2O ve Phaunouxite Ca3(AsO4)2·11H2O, kalsiyum arsenat hidratlarıdır.

Klorometan ya da metil klorür, CH3Cl formülüne sahip bir alkil halojenürdür. Aşırı derecede yanıcı bir gazdır. Önceden soğutucularda kullanılmıştır ancak toksisitesinden dolayı artık tüketici ürünlerinde kullanılmamaktadır. Klorometan ilk olarak Jean-Baptiste Dumas ve Eugene Peligot isimli iki Fransız kimyager tarafından 1835'te metanol, sülfürik asit ve sodyum klorür karışımının kaynatılması ile sentezlenmiştir, bu yöntem günümüzde kullanılana çok benzerdir.

Kloroetan ya da etil klorür etil grubuna bir adet klor atomu bağlanmasıyla oluşan bir organoklorür bileşiğidir. Renksiz yanıcı bir gazdır, soğutulmuş sıvı olarak taşınır. CH3CH2Cl formülüne sahiptir. Bir benzin katkı maddesi olan Tetraetilkurşunun üretiminde etil grubu kaynağı olarak kullanılır. Etilene HCl katılması ile üretilir.
Benzil klorür, C
6H
5CH
2Cl formüllü organik bileşik. Kimyasal tepkimelerde çokça kullanılan renksiz sıvı. Kaynama noktası 179 °C'dir. Suda çözünmez. Etanol, dietil eter, kloroform ve karbon tetraklorürde çözünür.

Baryum klorür, BaCl2 formüllü inorganik bir bileşik'tir. Bu bileşik baryum'un suda-çözünen en yaygın tuzlarından biridir. Diğer baryum tuzlarının çoğu gibi, baryum klorür beyaz toz halinde ve zehirlidir. Alevde sarı-yeşil renk verir. Ayrıca higroskopiktir, ilk önce dihidrat BaCl2(H2O)2' ye dönüşür.
Kloropikrin, şu anda geniş spektrumlu bir antimikrobiyal, fungisit, herbisit, insektisit ve nematisit olarak kullanılan bir kimyasal bileşiktir. Birinci Dünya Savaşı'nda zehirli gaz olarak kullanılmıştır. Kimyasal yapı formülü Cl
3CNO
2'dir.
1,1-Dikloroetan, etiliden klorür olarak da bilinen klorlu bir hidrokarbondur. Kloroform benzeri bir kokuya sahip, renksiz yağımsı bir sıvıdır. Suda kolayca çözünmez ancak çoğu organik çözücüyle karışabilir. 1,2-Dikloroetanın izomeridir.

Klorobenzen, C
6H
5Cl kimyasal formülüne sahip aromatik bir organik bileşiktir. Bu renksiz, yanıcı sıvı, yaygın bir çözücüdür ve diğer kimyasalların üretiminde yaygın olarak kullanılan bir ara maddedir.
1,2-Dikloroetilen (1,2-DCE) ya da 1,2-dikloroeten, C
2H
2Cl
2 moleküler formülüne sahip bir çift organoklorür bileşiğinin adıdır. Her ikisi de hoş kokulu renksiz sıvılardır. Cis-1,2-dikloroetilen veya trans-1,2-dikloroetilen olmak üzere iki geometrik izomerden herhangi biri olarak mevcut olabilir, ancak sıklıkla ikisinin bir karışımı olarak kullanılır. Çoğu cis-trans bileşiğin aksine Z izomeri (cis), E izomerinden (trans) daha stabildir. 1,2-Dikloroetilen çifti, yağlar için çözücü olarak kullanılır.
Morfolin, O(CH
2CH
2)
2NH kimyasal formülüne sahip organik bir kimyasal bileşiktir. Bu halkalı bileşik, hem amin hem de eter fonksiyonel grupları içerir. Amin nedeniyle morfolin bir bazdır; konjuge asidine morfolinyum denir. Örneğin, morfolinin hidroklorik asitle işlenmesi, morfolinyum klorür tuzunu oluşturur. Zayıf, amonyak veya balık benzeri bir kokuya sahip, renksiz bir sıvıdır. Morfolinin adlandırılması, onun morfinin yapısının bir parçası olduğuna inanan Ludwig Knorr'a atfedilir.

Perklorometil merkaptan, CCl3SCl formülüne sahip organosülfür bileşiğidir. Esas olarak boyalar ve fungisitlerin (captan, folpet) üretiminde bir ara madde olarak kullanılır. Ticari numunelersarımsı renkte olmasına rağmen saf bileşik renksiz bir yağdır. Suda çözünmez fakat organik çözücülerde çözünür. Kötü, dayanılmaz, keskin bir kokusu vardır. Perklorometil merkaptan orijinal adıdır, sistematik adı triklorometansülfenil klorür olmalıdır çünkü bileşik bir merkaptan değil, bir sülfenil klorürdür.

Fosforil klorür, POCl
3 formülüne sahip bir sıvıdır. Nemli havada hidrolize olup fosforik asit ve hidrojen klorür dumanı açığa çıkarır. Endüstriyel olarak büyük ölçekte fosfor triklorür ve oksijen veya fosfor pentoksitten üretilir. Esas olarak fosfat esterleri yapmak için kullanılır.


















