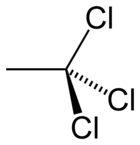
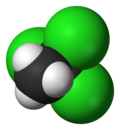
1,1,1-Trikloroetan
| |||
| |||
| Adlandırmalar | |||
|---|---|---|---|
Tercih edilen IUPAC adı 1,1,1-Trikloroetan | |||
Diğer adlar 1,1,1-TCA, Metil kloroform, Solvent 111, R-140a, | |||
| Tanımlayıcılar | |||
CAS numarası | |||
3D model (JSmol) | |||
| ChEBI | |||
| ChEMBL | |||
| ChemSpider | |||
| ECHA InfoCard | 100.000.688 | ||
| EC Numarası |
| ||
| 82076 | |||
IUPHAR/BPS | |||
| KEGG | |||
PubChem CID | |||
| RTECS numarası |
| ||
| UNII | |||
| UN numarası | 2831 | ||
CompTox Bilgi Panosu (EPA) | |||
| |||
| |||
| Özellikler | |||
| Molekül formülü | C2H3Cl3 ya da CH3CCl3 | ||
| Molekül kütlesi | 133,40 g/mol | ||
| Görünüm | renksiz sıvı | ||
| Koku | hafif, kloroform benzeri[1] | ||
| Yoğunluk | 1,32 g/cm3 | ||
| Erime noktası | -33 °C (-27 °F; 240 K) | ||
| Kaynama noktası | 74 °C (165 °F; 347 K) | ||
| Çözünürlük (su içinde) | %0,4 (20°C)[1] 0.480 g/litre at 20 °C[2] | ||
| Buhar basıncı | 100 mmHg (20°C)[1] | ||
| Kırınım dizimi (nD) | 1,437[3] | ||
| Tehlikeler | |||
| İş sağlığı ve güvenliği (OHS/OSH): | |||
| Ana tehlikeler | Ozon tabakasına olumsuz etki eder. Üst solunum yollarını tahriş eder. Gözlerde şiddetli tahrişe ve şişmeye neden olur. | ||
| GHS etiketleme sistemi: | |||
| Piktogramlar |  | ||
| İşaret sözcüğü | Warning | ||
| Tehlike ifadeleri | H332, H420 | ||
| Önlem ifadeleri | P261, P271, P304+P312, P304+P340, P312, P502 | ||
| NFPA 704 (yangın karosu) | |||
| Patlama sınırları | 7.5%-12.5%[1] | ||
| Öldürücü doz veya konsantrasyon (LD, LC): | |||
LD50 (medyan doz) | 9600 mg/kg (oral, sıçan) 6000 mg/kg (oral, fare) 5660 mg/kg (oral, tavşan)[4] | ||
LC50 (medyan konsantrasyon) | 3911 ppm (fare, 2 saat) 18000 ppm (sıçan, 4 saat)[4] | ||
| NIOSH ABD maruz kalma limitleri: | |||
| PEL (izin verilen) | TWA 350 ppm (1900 mg/m3)[1] | ||
| REL (tavsiye edilen) | C 350 ppm (1900 mg/m3) [15 dakika][1] | ||
| IDLH (anında tehlike) | 700 ppm[1] | ||
| Aksi belirtilmediği sürece madde verileri, Standart sıcaklık ve basınç koşullarında belirtilir (25 °C [77 °F], 100 kPa). | |||
Metil kloroform ya da 1,1,1-trikloroetan C2H3Cl3 formülüne sahip bir kloroalkandır. Doğada bulunmamaktadır, sentetik olarak üretilmiştir. Kloroforma benzeyen bir kokuya sahip olan bu renksiz sıvı bir zamanlar çözücü olarak kullanılmaktaydı ancak ozon tabakasına zararlı olduğu keşfedilince kullanımı terk edilmiştir. Montreal Protokolü nedeniyle 1996 tarihinden sonra kullanımı yasaklanmıştır. 1,1,1-Trikloroetan yeterince stabil olmadığından stabilize edilmesi için içine dioksan gibi bazı maddeler katılır.
Üretimi
Büyük ölçekte 1,1,1-Trikloroetan üretmek için çeşitli yöntemler geliştirilmiştir.
Vinil klorür yolu
Başta simetrik 1,2-dikloroetanın 450-620 °C arasında, 450-930 kPa basınç altında bozunması ile elde edilen vinil klorür, ferrik klorür katalizörlüğünde 35 °C'ta hidrojen klorür ile tepkimeye sokularak asimetrik 1,1-dikloroetan elde edilir:
- ClCH
2−CH
2Cl + (yüksek sıcaklık/basınç) → CH
2=CHCl + HCl - CH
2=CHCl + HCl → CH
3−CHCl
2
Burada elde edilen asimetrik dikloroetan, UV ışığı altında ekzotermik bir reaksiyonla 400 °C'ta 1,1,1-trikloroetana klorlanır:[5]
- CH
3−CHCl
2 + Cl
2
(gaz) → CH
3−CCl
3 + HCl
Viniliden klorür yolu
Başka yaygın bir üretim yönteminde viniliden klorür, ferrik klorür eşliğinde oda sıcaklığında ve atmosfer basıncından biraz yüksek basınçta hidrojen klorürle tepkimesinden üretilebilir:[5]
- CH
2=CCl
2 + HCl + FeCl
3 → CH
3−CHCl
2
Etanın klorlanması
Etan klorlanarak metil kloroform üretimi, oluşan yan ürünlerin yüksek miktarı nedeniyle, diğer yöntemler kadar yüksek verimli değildir. Yan ürünlerin arasında değişen miktarlarda ortaya çıkan etanın birçok klorlu türevinin yanı sıra vinil klorür ve viniliden klorür de oluşabilir. Bazı yan ürünler üretim tesislerinde geri dönüştürülerek tekrar işlemlerden geçirilir ve metil kloroform yapımında kullanılır.[5]
Tarihi
1,1,1-Trikloroetan, ilk kez 1838-1840 yılları arasında Fransız kimyager Victor Regnault tarafından keşfedildi.[6][7]
1,1,1-Trikloroetan, 19. yüzyılda anestezide kloroforma alternatif olarak denenen uçucu organoklorürlerden biriydi.[7] 1880'lerde kloroform için güvenli ve güçlü bir ikame olabileceği keşfedildi,[8] ancak o dönem için trikloroetanın üretimi pahalı ve zahmetliydi.[9]
Trikloroetan 1880'de anestezik olarak önerildi. Aynı yıl ilk kez "metil-kloroform" (İngilizce: methyl-chloroform) olarak adlandırıldı. O zamanlar, kloral hidratın narkotik etkilerinin "alkali kanda" kloroforma giden varsayımsal bir metabolik yoldan kaynaklandığı düşünülüyordu. 1,1,1-Trikloroetan, kloral ile yapısal benzerliği ve potansiyel anestezik etkileri açısından incelendi. Ancak, trikloroetan laboratuvar deneylerinde kloroforma herhangi bir dönüşüm göstermedi. Triklorometil grubundan yoksun olan 1,1,2-trikloroetan (CHCl
2CH
2Cl) izomeri, 1,1,1 izomerinden bile daha güçlü anestezik etkiler gösterdi.[10]

Kullanım alanları
1,1,1-Trikloroetan genellikle apolar bir çözücü olarak kabul edilir. Klor atomlarının iyi polarizasyonu nedeniyle hekzan gibi hidrokarbonlarda iyi çözünmeyen organik bileşikler için üstün bir çözücüdür. Birçok organik madde için mükemmel bir çözücüdür ve aynı zamanda klorlu çözücülerin arasında en az toksik olanlardan biridir. Montreal Protokolünden önce çeşitli kullanımları bulunmasına rağmen, trikloroetanın en yaygın ve bilindik kullanımı metal temizliğine yönelikti. Örneğin, 1974 yılında ADB'de kullanılan trikloroetanın %71'i metal temizliğinde, %23'ü kimyasal hammadde olarak ve geri kalan %6'sı diğer çeşitli alanlarda kullanılmaktaydı. Metil kloroform, 1950'lerde düşük sıcaklıklarda buharla temizleme işlemleri için karbon tetraklorüre alternatif olarak piyasaya sürüldü. İlk başlarda metallerin yağlardan temizlenmesinde kullanımı pek yaygınlaşmasa da, 1960'lardan sonra trikloroetilenin (TCE) sağlık ve çevre üzerindeki etkileri hakkındaki endişeler üzerine metil kloroform metal sanayiide daha fazla benimsenmeye başladı. Metil kloroformun kullanımı, üretiminin Montreal Protokolü kapsamında yasakladığı 1996 yılına kadar devam etti. Metil kloroform ayrıca yaygın olarak aerosol sprey formülasyonlarında çözücü ve taşıyıcı olarak kullanıldı. Saç spreyleri, sprey boyalar, fren temizleyiciler, leke çıkarıcılar, fırın temizleyiciler, mobilya cilaları gibi günlük aerosol sprey ürünlerinde bulunmaktaydı. Yasaklanmadan birkaç yıl önce, 1988'de, ABD'de 34,5 bin ton metil kloroform aerosol formülasyonlarında kullanılmaktaydı. Devre kartı üretimi, yapıştırıcılar ve boyalarda kullanıldı.[5]
Aynı zamanda fotoğraf filmi (film/slayt/negatifler vb.) için standart temizleyiciydi. Yaygın olarak bulunan diğer çözücüler emülsiyona ve baza zarar verir ve bu nedenle bu uygulama için uygun değildir. Alternatif olarak kullanılan Forane 141 (1,1-dikloro-1-floroetan) çok daha az etkilidir ve kalıntı bırakma eğilimindedir.
Stabilizatörler
Metil kloroformun; oksijen, ışık, ısı ve su varlığında bozunmaya eğilimi vardır. Bozunma, metaller ve metal tuzları varlığında daha da hızlanabiliyordu ve bozunma ürünleri (özellikle hidrojen klorür) metallere zarar verebiliyordu. Stabilizatör eklenmemiş metil kloroform, alüminyum bir yüzeyle temas ettiğinde yüzey koyulaşır ve ortaya alüminyum klorür, hidrojen klorür, 2,2,3,3-tetraklorobütan ve viniliden klorür gibi bozunmaya ürünleri ortaya çıkardı. Düzgün stabilize edilmemiş metil kloroform da magnezyum varlığında bozunabilir. Bu nedenden ötürü metal temizliğinde kullanılan metil kloroform formülasyonunun %7 kadarı, 1,2-Bütilen oksit, siklohekzen oksit, nitrometan, izobütil alkol, dioksan, diallil amin veya siklik aminler gibi stabilizatörlerden oluşuyordu.[5]
Trikloroetilen (TCE) için kullanılan stabilizatörler (aminler, epoksitler ve piroller gibi), genel olarak metil kloroform için etkili değildi. TCE'nin durumuna benzer olarak, ticari metil kloroform asit toplayıcı ve metal stabilizatörleri içerebiliyordu. Metil kloroform, TCE'nin aksine otooksidasyona karşı dirençliydi ve antioksidanlara gerek görülmüyordu. Buna rağmen metil kloroformun kullanıldığı diğer materyallerin bozunmasını önlemek için kimyasala antioksidan katıldığı da olabiliyordu. 1977 yılındaki metil kloroform formülasyonlarında metil etil keton, trimetilortoformat, aminler, nitriller, trioksan, perkloroetilen, dimetoksietan, nitrometan, ikincil ve üçüncül alkoller gibi kimyasalların kullanıldığı bilinmekteydi. Kendi başına TCE'den daha stabil olmasına rağmen, metallere karşı olan reaktifliğinden dolayı, metal temizliğine yönelik ticari metil kloroformdaki katkı maddelerinin miktarı, aynı amaçla üretilen TCE'ninkinden daha fazlaydı.[5]
Sağlık üzerindeki etkileri
Birçok benzer bileşik kadar toksik olmasa da, solunan veya yutulan 1,1,1-trikloroetan merkezî sinir sistemi baskılayıcısı olarak etki eder ve baş dönmesi, kafa karışıklığı ve yeterince yüksek konsantrasyonlarda bilinç kaybı ve ölüm dâhil olmak üzere sarhoşluk benzeri etkilere neden olabilir.[11]
Çevresel etkileri
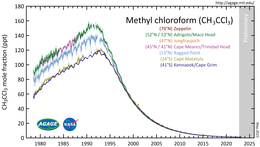

1,1,1-Trikloroetan, karbon dioksite kıyasla 100 yıllık küresel ısınma potansiyeli 169 olan oldukça güçlü bir sera gazıdır.[12] Yine de bu, yaklaşık 5 yıllık nispeten kısa atmosferik ömrü nedeniyle, çözücü olarak yerini aldığı karbon tetraklorürün onda birinden daha azdır.[13]
Montreal Protokolü, 1,1,1-trikloroetanı ozon tabakasının incelmesinden sorumlu bir bileşik olarak hedef aldı ve 1996'dan itibaren üretimini ve kullanımı yasakladı. O zamandan beri, üretimi ve kullanımı dünyanın çoğu yerinde aşamalı olarak durduruldu ve atmosferik konsantrasyonu önemli ölçüde azaldı.[13]
Kaynakça
- ^ a b c d e f g NIOSH Pocket Guide to Chemical Hazards. "#0404". National Institute for Occupational Safety and Health (NIOSH).
- ^ "International Programme On Chemical Safety, Environmental Health Criteria 136". World Health Organization, Geneva. 1990. 14 Temmuz 2001 tarihinde kaynağından arşivlendi. Erişim tarihi: 25 Aralık 2017.
- ^ Timmermans, Jean, Physico-chemical constants of pure organic compounds (1950), p. 242
- ^ a b "Methyl chloroform". Immediately Dangerous to Life or Health Concentrations (IDLH). Ulusal İş Sağlığı ve Güvenliği Enstitüsü (NIOSH).
- ^ a b c d e f Morrison, R. D.; Murphy, B. L. (2015). "Methyl Chloroform". Chlorinated Solvents: A Forensic Evaluation. Birleşik Krallık: Royal Society of Chemistry. ISBN 9781782626077.
- ^ Lyman, Henry W. (1881). W. Wood. s. 209 https://archive.org/details/artificialanesth00lyma/page/209/mode/1up. Eksik ya da boş
|başlık=(yardım) - ^ a b "Forreign Correspondence". The American Practitioner. Cilt 23. Ocak 1881. s. 28.
- ^ "Methyl-Chloroform". Saint Louis Medical and Surgical Journal. 1887.
- ^ Brunton, T. Lauder (1892). An Introduction to Modern Therapeutics. s. 122.
- ^ "On Two New Anaesthetics". The American Journal of Pharmacy. Cilt 53. Mart 1881. ss. 119-120.
- ^ "Toxicological Profile for 1,1,1-Trichloroethane". 9 Mayıs 2008 tarihinde kaynağından arşivlendi. Erişim tarihi: 26 Temmuz 2024.
- ^ Hodnebrog Ø, Aamaas B, Fuglestvedt JS, Marston G, Myhre G, Nielsen CJ, Sandstad M, Shine KP, Wallington TJ (September 2020). "Updated Global Warming Potentials and Radiative Efficiencies of Halocarbons and Other Weak Atmospheric Absorbers". Reviews of Geophysics. 58 (3). ss. e2019RG000691. Bibcode:2020RvGeo..5800691H. doi:10.1029/2019RG000691. PMC 7518032 $2. PMID 33015672.
- ^ a b "Chapter 8, Table 8.A.1". AR5 Climate Change 2013: The Physical Science Basis. s. 733. 2 Şubat 2017 tarihinde kaynağından arşivlendi. Erişim tarihi: 26 Temmuz 2024.