
Periyodik tablo, kimyasal elementlerin sınıflandırılması için geliştirilmiş tablodur. Dilimizde periyodik tablo, periyodik cetvel, periyodik çizelge, elementler tablosu gibi birçok şekilde isimlendirilmiştir. Bu tablo bilinen bütün elementlerin artan atom numaralarına göre sıralanışıdır. Periyodik cetvelden önce de bu yönde çalışmalar yapılmış olmakla birlikte, mucidi genelde Rus kimyager Dmitri Mendeleyev kabul edilir. 1869'da Mendeleyev atomları artan atom ağırlığına göre sıraladığında belli özelliklerin tekrarlandığını fark etti. Özellikleri tekrarlanan elementleri alt alta yerleştirdi ve buna grup adını verdi.

Element, aynı cins atomlardan oluşan ve kimyasal yollarla kendinden daha basit ve farklı maddelere ayrılamayan saf maddelere verilen isimdir.

Atom veya ögecik, bilinen evrendeki tüm maddenin kimyasal ve fiziksel niteliklerini taşıyan en küçük yapı taşıdır. Atom Yunancada "bölünemez" anlamına gelen "atomos"tan türemiştir. Atomus sözcüğünü ortaya atan ilk kişi MÖ 440'lı yıllarda yaşamış Demokritos'tur. Gözle görülmesi imkânsız, çok küçük bir parçacıktır ve sadece taramalı tünelleme mikroskobu vb. ile incelenebilir. Bir atomda, çekirdeği saran negatif yüklü bir elektron bulutu vardır. Çekirdek ise pozitif yüklü protonlar ve yüksüz nötronlardan oluşur. Atomdaki proton sayısı elektron sayısına eşit olduğunda atom elektriksel olarak yüksüzdür. Elektron ve proton sayıları eşit değilse bu parçacık iyon olarak adlandırılır. İyonlar oldukça kararsız yapılardır ve yüksek enerjilerinden kurtulmak için ortamdaki başka iyon ve atomlarla etkileşime girerler.

Elektron dizilimi, atom fiziği ve kuantum kimyasında, bir atom ya da molekülün elektronlarının atomik ya da moleküler orbitallerdeki dağılımıdır. Örneğin Neon atomunun elektron dizilimi 1s2 2s2 2p6 olarak gösterilir.
Elektronegatiflik, kimyada bağ yapımında kullanılan elektronların bağı oluşturan atomlar tarafından çekilme gücüdür. Klor gibi dış enerji seviyeleri hemen hemen tamamen doldurulmuş atomlar güçlü elektronegatiftirler ve kolaylıkla elektron alırlar. Buna karşın sodyum gibi dış seviyeleri hemen hemen boş olan atomlar kolaylıkla elektronlarını verirler ve güçlü elektropozitiftirler. Elektronegatifler ile elektron ilgileri karıştırılmamalıdır.

Proton, atom çekirdeğinde bulunan artı yüklü atomaltı parçacıktır. Elektronlardan farklı olarak atomun ağırlığında hesaba katılacak düzeyde kütleye sahiptirler. Şimdiye kadar Protonların İki yukarı bir aşağı kuarktan oluştuğu kabul edilse de yeni yapılan bilimsel çalışmalarda araştırmacılar protonun kütlesinin yüzde 9'unun kuarkların ağırlığından, yüzde 32'sinin protonun içindeki kuarkların hızlı hareketlerinin meydana getirdiği enerjiden, yüzde 36'sının protonun kütlesiz parçacıkları olan ve kuarkları bir arada tutmaya yardımcı olan gluonların enerjilerinden, geriye kalan yüzde 23'lük bölümünse kuarkların ve gluonların protonun içinde karmaşık şekillerde etkileşimlerde bulunduklarında meydana gelen kuantum etkimelerden oluştuğunu buldular. Evrendeki bütün protonlar 1,6 x 10−19 değerinde pozitif yüke sahiptirler. Bu, atomlardaki çeşitli protonların birbirlerini itmelerini sağlar. Ama aradaki çekim, itmeden 100 kez daha güçlü olduğu için protonlar birbirlerinden ayrılmazlar. Protonun kütlesi elektronunkinden 1836 kat fazladır. Buna karşın, bilinmeyen bir nedenden ötürü elektronun yükü protonunkiyle aynıdır: 1,6 x 10−19 C. Atom içinde her biri (+1) pozitif elektrik yükü taşıyan taneciğe proton denir. Bu yüke yük birimi denir. Protonun yüklü elektronun yüküne eşit fakat ters işaretlidir.Bir protonun yoğunluğu yaklaşık olarak 4 x 1017 Kg/m³ 'tür. (2,5 x 1016 Lb/Ft3)

İyon ya da yerdeş, bir veya daha çok elektron kazanmış ya da yitirmiş bir atomdan oluşmuş elektrik yüklü parçacıktır. Atomlar kararsız yapılarından kurtulmak ve kararlı hale gelebilmek için elektron alırlar ya da kaybederler. Bunun için de başka bir atomla ya da kökle bağ kurarlar.

İyonik bağ, zıt yüklü iyonlar arasındaki elektrostatik kuvvetlere dayanan bir kimyasal bağ türüdür.

Kimyasal bağ, atomların veya iyonların molekülleri, kristalleri ve diğer yapıları oluşturmak üzere birleşmesidir. Bağ, iyonik bağlar'da olduğu gibi zıt yüklü iyonlar arasındaki elektrostatik kuvvetten veya kovalent bağ'larda olduğu gibi elektronların paylaşılmasından veya bu etkilerin bazı kombinasyonlarından kaynaklanabilir. Açıklanan kimyasal bağların farklı mukavemetleri vardır: kovalent, iyonik ve metalik bağlar gibi "güçlü bağlar" veya "birincil bağlar" ve dipol-dipol etkileşimleri, London dağılım kuvveti ve hidrojen bağı gibi "zayıf bağlar" veya "ikincil bağlar" vardır.
İyonlaşma enerjisi ya da iyonizasyon enerjisi, gaz halindeki bir atomun son temel enerji seviyesindeki çekirdek tarafından en az kuvvetle çekilen bir elektronu koparmak için verilmesi gereken en az enerji miktarıdır. Elementlerin elektron alış verişi sonucu oluşturdukları katyon ve anyonların oluşturduğu tepkimelerdir.Asitlerin iyonlaşması demek, kendini oluşturan (+) ve (-) yüklü iyonlarına ayrışması demektir.Asitler, saf haldeyken elektrik akımını iletemeyip sadece suda çözündüklerinde elektrik akımını iletebilirler. Mesela;

Atom çekirdeği, atomun merkezinde yer alan, proton ve nötronlardan oluşan küçük ve yoğun bir bölgedir. Atom çekirdeği 1911 yılında Ernest Rutherford tarafından keşfedildi. Bu keşif, 1909 yılında gerçekleştirilen Geiger-Marsden deneyine dayanmaktadır. Nötronun James Chadwick aracılığıyla 1932 yılında keşfinden sonra, çekirdeğin proton ve nötronlardan oluştuğu modeli Dmitri Ivanenko ve Werner Heisenberg tarafından çabucak geliştirildi. Atomun kütlesinin neredeyse tamamı çekirdek içerisindedir, elektron bulutunun atom kütlesine katkısı oldukça azdır. Proton ve nötronlar çekirdek kuvveti tarafından çekirdeği oluşturmak için birbirlerine bağlanmıştır.

Atom yarıçapı, küre şeklinde olduğu düşünülen atomların büyüklüklerini ölçmekte kullanılan bir niceliktir. Bu nicelik bir atomun çekirdeği ile elektron bulutu arasındaki uzaklığı ifade eder.
Livermoriyum, periyodik tabloda 116 numaralı süper ağır yapay kimyasal elementtir. Sembolü Lv 'dir. Bazı araştırmacılar tarafından eka-polonyum olarak adlandırılmıştır. Geçici olarak ununheksiyum biçiminde kullanılan elementin adı IUPAC tarafından 30 Mayıs 2012 tarihinde kalıcı biçimde livermoriyum olarak değiştirilmiştir. Kaliforniya'daki Lawrence Livermore Ulusal Laboratuvarının adına ithafen livermoriyum denmiştir.
Elektrolit, iyonların hareketi sayesinde elektriksel olarak iletken olan, ancak elektronları iletmeyen ilenler içeren bir ortamdır. Su gibi polar çözücü içinde çözülmüş çoğu çözünür tuzları, asitleri ve bazları içermektedir. Çözünüm sonrasında; madde çözücü içinde eşit olarak dağıtılan katyonlara ve anyonlara ayrılmaktadır. Katı hal elektrolitleri de mevcuttur. Tıpta elektrolit terimi, çözünen maddeyi ifade etmektedir.

Organik kimyada bazı atom halkalarının yapısı beklenenin üstünde kararlıdır. Doymamış bağlar, yalın elektron çiftleri veya boş orbitallerden oluşan konjüge bir halkanın konjüge olmasından beklenecek kararlılıktan daha yüksek bir kararlılık gösterme özelliğine aromatiklik denir. Aromatiklik, halkasal delokalizasyon ve rezonansın bir belirtisi olarak da düşünülebilir.
Kuantum mekaniğine göre atomik orbital, elektronların atom çekirdeği etrafındaki konumunu ve dalga-benzeri özelliklerini tanımlayan bir matematiksel fonksiyondur. Elektronun atom çekirdeği etrafındaki belirli bir bölgede bulunma olasılığı bu fonksiyon aracılığı ile hesaplanabilir. Fizikte atomik, kimyada orbital olarak geçer.
Yan kuantum sayısı, bir yörüngenin kaç orbitale sahip olduğunu belirten sayıdır. Bir yörüngede kaç orbital bulunduğunu hesaplamak için n2 parametresi kullanılır. n, burada "yörünge numarası" veya "Baş kuantum sayısı" adıyla anılır.
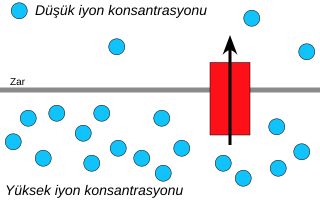
Kemiosmoz; iyonların, elektrokimyasal gradyanı azaltmak için seçici geçirgen bir zardan geçme hareketidir. Hücresel solunumdaki ATP sentezinin gerçekleşmesini sağlayan enerjinin büyük bir kısmı hidrojenlerin yaptığı bu hareketten karşılanır.
Pauling'in kuralları,1929'da Linus Pauling tarafından iyonik bileşiklerin kristal yapılarını tahmin etmek ve rasyonelleştirmek için yayınlanan beş kuraldır.
Atom fiziğinde, etkin nükleer yük, çok elektronlu bir atomda bir elektronun yaşadığı gerçek pozitif (nükleer) yük miktarıdır. "Etkili" terimi, negatif yüklü elektronların koruyucu etkisi, daha yüksek enerjili elektronların, iç katmanın itici etkisi nedeniyle çekirdeğin tam nükleer yükünü deneyimlemesini engellediği için kullanılır. Bir elektronun deneyimlediği etkin nükleer yüke çekirdek yükü de denir. Atomun oksidasyon sayısı ile nükleer yükün gücünü belirlemek mümkündür. Elementlerin fiziksel ve kimyasal özelliklerinin çoğu, elektronik konfigürasyon temelinde açıklanabilir. İyonlaşma enerjilerinin davranışını düşününperiyodik tabloda. İyonizasyon potansiyelinin büyüklüğünün aşağıdaki faktörlere bağlı olduğu bilinmektedir:
- atomun boyutu;
- nükleer yük;
- İç kabukların eleme etkisi ve
- En dıştaki elektronun, içteki elektron tarafından kurulan yük bulutuna nüfuz etme derecesi.











