
Dolmabahçe Camii, Sultan Abdülmecid'in annesi Bezmialem Valide Sultan tarafından başlatılıp ölümü üzerine Sultan Abdülmecid tarafından tamamlanan ve tasarımı Garabet Balyan'a ait olan bir yapıdır.

Bir kimyasal bileşiğin molekül kütlesi, bu bileşiğin bir molekülünün birleşik atom kütle birimi u cinsinden kütlesidir. Bağıl bir değer olduğundan bir maddenin molekül kütlesine yaygın olarak bağıl moleküler kütle denir ve Mr. diye de kısaltılır.

Kimyasal bileşik, kimyasal bağlarla bir arada tutulan birden fazla kimyasal elementin atomlarını içeren birçok özdeş molekülden oluşan kimyasal maddedir. Dolayısıyla tek bir elementin atomlarından oluşan bir molekül bileşik değildir. Bir bileşik, diğer maddelerle etkileşimi içerebilen kimyasal reaksiyonla farklı bir maddeye dönüştürülebilir. Bu süreçte atomlar arasındaki bağlar kırılabilir ve/veya yeni bağlar oluşabilir.
Değerlik kabuğu elektron çifti itmesi kuralları moleküllerin şekillerini tahmin etmede kullanılır ve değerlik elektron çiftlerinin birbirlerini elektrostatik kuvvetle itmesi temeline dayanır. Teorinin yaratıcısı olan bilim adamlarına atfen Gillespie–Nyholm teorisi olarak da adlandırılır. "VSEPR" kısaltması kimi zaman "vespır" olarak da telaffuz edilebilir.
Teoriye göre atomları çevreleyen değerlik elektron çiftleri birbirlerini iterek aralarındaki itme kuvvetini en aza indirirler ve böylece moleküle şeklini verirler. Merkez atoma bağlı atomların sayısı ile bağ yapmamış elektron çiftlerinin sayısının toplamı sterik numarayı verir.
Prizma ya da biçme, genelde en boy ve yükseklik kavramlarına sahip cisimler olarak adlandırılır. Ancak bazı cisimlerin (küre) en ve boyu tam olarak ifade edilememekle çap ve çevre de bu nicelikleri belirtmek için kullanılır.

Moleküler geometri molekülleri oluşturan atomların üç boyutlu uzaydaki dizilişidir. Kimyasal aktiflik, kimyasal polarite, faz, renk, manyetizma, biyolojik aktiflik gibi maddenin birçok özelliğini tanımlar. Atomların birbirleriyle oluşturduğu bağların arasındaki açı molekülün geri kalanıyla bağlantılıdır.

İznik Yeşil Camii, Bursa ili, İznik ilçesinde bulunan Osmanlı mimarisinin ilk örneklerindedir. I. Murat'ın sadrazamı Çandarlı Halil Paşa tarafından yaptırılmıştır. Paşanın 1387'de ölmesi üzerine cami oğlu Çandarlı Ali Paşa tarafından bitirilmiştir.
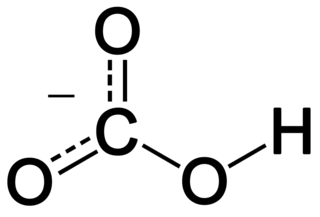
Bikarbonat, inorganik kimyada, (IUPAC-önerilen isim: hidrojen karbonat) karbonik asitin protonsuzlaştırılmasındaki bir ara yapı. HCO3− kimyasal formülene sahip moleküler iyondur.

Kimyada, doğrusal moleküler geometri 180°'lik bir açıya yerleştirilmiş diğer iki atoma bağlanmış merkezi bir atom etrafındaki geometriyi tarif eder. Asetilen (HC≡CH) gibi doğrusal organik moleküller genellikle karbon merkezleri için sp orbital hibridizasyonu teşvik edilerek tarif edilir.
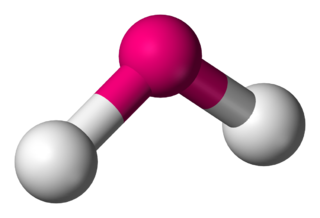
Kimyada, " açısal" ya da "bükülmüş" terimi bazı moleküllere moleküler geometrilerini tanımlamak için kullanılabilir. Oksijen gibi bazı atomlar, Elektron dizilimi nedeniyle hemen hemen her zaman iki (veya daha fazla) kovalent bağını doğrusal olmayan yönlerde ayarlarlar. Su (H2O), analoglarının yanı sıra açısal bir molekül örneğidir. İki hidrojen atomu arasındaki bağ açısı yaklaşık olarak 104,45°'dir. Doğrusal olmayan geometri genel olarak sadece ana grup elementleri içeren diğer üç atomlu molekülleri ve iyonlar için gözlemlenir, belirgin örnekler: Azot dioksit (NO2), kükürt diklorür (SCL2) ve metilen (CH2).

Kimyada, üçgen düzlemsel, merkezde bir atom ve birer üçgenin köşelerinde üç atom olan ve hepsi bir düzlemde çevresel atomlar olarak bulunduğu bir moleküler geometri modelidir. İdeal bir üçgen düzlemsel türde, üç ligand aynıdır ve bütün bağ açıları 120°'dir. Bu türler D3h nokta grubuna aittir. Üç ligandın aynı olmaadığı H2CO gibi moleküller, bu ideal geometri sapma gösterir. Üçgen düzlemsel bir şekle sahip moleküller arasında boron triflorür (BF3), formaldehit (H2CO), fosgen (COCl2) ve kükürt trioksit (SO3) bulunmaktadır. Üçgen düzlem geometrisi olan bazı iyonlar arasında nitrat (NO3-), karbonat (CO3−2) ve guanidinyum (C(NH2)3+)) bulunmaktadır. Organik kimyada, üçgen düzlemsel olarak karbon merkezlerine üç bağlı atomun bulunduğu moleküller çoğunlukla sp2 hibridizasyona sahip olarak tarif edilmiştir.

Kimyada üçgen piramit, apekste bir atomun ve dört yüzlüyü andıran üçgen temelin köşelerinde üç atomun bulunduğu moleküler geometridir (dörtyüzlü moleküler geometri ile karıştırılmamalıdır). Köşelerdeki üç atomun hepsi aynı olduğunda, molekül C3v nokta grubuna aittir. Üçgen piramit geometrisi olan bazı moleküller ve iyonlar; azot grubu hidritler (XH3), ksenon trioksit (XeO3), klorat iyonu ClO3- ve sülfit iyonu SO3−2. Organik kimyada, üçgen piramit geometriye sahip moleküller bazen sp3 hibridize olarak açıklanmaktadır. AXE yöntemi için Vsepr teori sınıflandırması AX3E1'dir.
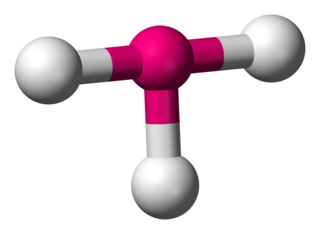
Kimyada, T-şeklindeki moleküler geometri, merkezi bir atomun üç liganda sahip olduğu bazı moleküllerin yapılarını açıklar. Normalde, üç koordineli bileşikler üçgen düzlemsel veya piramidal geometrileri kullanır. T-şekilli moleküllerin örnekleri arasında, halojen triflorürler vardır, örneğin ClF3.
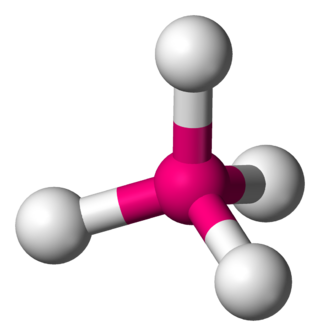
Dörtyüzlü veya tetrahedral molekül geometrisi, merkezi atomun, dört yüzlünün ortasında, dört köşede ise sübstitüentlerin yer aldığı molekül geometrisidir. Bağ açıları, dört sübstitüent aynı olduğunda (örn. metan CH4 ya da daha ağır analogları) cos−1 (-⅓) = 109,4712206 ...° ≈ 109.5° olur. Metan veya diğer simetrik yüzlü moleküller Td nokta grubuna aittir, ama dörtyüzlü moleküller genellikle düşük simetriye sahiptir. Tetrahedral moleküller kiral olabilir.
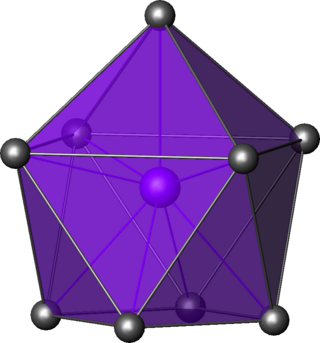
Kimyada, kepli kare antiprizmatik moleküler geometri, bir jiro-uzatılmış kare piramidin köşelerini tanımlayan dokuz atomun, atom gruplarının veya ligandların merkezi bir atomun etrafına yerleştirildiği bileşiklerin şeklini tanımlar.

Kimyada, çift kepli üçgen prizmatik moleküler geometri, sekiz atom, atom grupları veya ligand gruplarının, çift-taraflı bir üçgen prizmanın köşelerini tanımlayan merkezi bir atomun etrafına yerleştirildiği bileşiklerin şeklini açıklar. Bu şekil, C2v olan simetri ile birlikte, okta-koordine geçiş metali kompleksleri için kare antiprizma ve onikiyüzlü ile birlikte üç genel biçimlerinden bir tanesidir.

Kimyada, onikiyüzlü moleküler geometri, sekiz atomun, atom gruplarının veya ligandların bir snub disfenojeninin köşelerini tanımlayan merkezi bir atomun etrafına yerleştirildiği bileşiklerin şeklini tarif eder. Bu şekil D2d simetriye sahiptir ve kare antiprizma ve çift kepli üçgen prizma ile birlikte oktakoordinat geçiş metali kompleksleri için üç ortak şekilden biridir.

Kare düzlemsel moleküler geometri, bazı bileşiklerde görülen ve molekülleri oluşturan atomların, merkezdeki bir atomun çevresinde bir kare oluşturacak şekilde bağlandığı moleküler geometri çeşididir. Trans- ve cis-PtCl2(NH3)2 bileşiklerinde gözlemlediği yapının ardından Alfred Werner tarafından ortaya atılmıştır.

Geometride adını Sakız Adalı Hipokrat'tan sonra alan Hipokrat ayı, iki çemberden oluşan yaylarla sınırlanmış bir aydır, daha küçük olanın çapı, daha büyük çember üzerinde dik bir açıyı kapsayan bir kirişe sahiptir.

Kimyada, oktahedral moleküler geometri, bir oktahedronun köşelerini tanımlayan, merkezi bir atom etrafında simetrik olarak düzenlenmiş altı atomlu bileşiklerin veya atom gruplarının veya ligandların şeklini tanımlar. Oktahedronun sekiz yüzü vardır, dolayısıyla octa ön ekini alır. Oktahedron, Platonik katılardan biridir, ancak oktahedral moleküller tipik olarak merkezlerinde bir atom içerir ve ligand atomları arasında bağ yoktur. Mükemmel bir oktahedron Oh nokta grubuna aittir. Oktahedral bileşiklerin örnekleri arasında kükürt hekzaflorür SF6 ve molibden hekzakarbonil Mo (CO)6 gösterilebilir. "Oktahedral" terimi, kimyagerler tarafından, merkezi atoma olan bağların geometrisine odaklanarak ve ligandların kendi aralarındaki farklılıkları dikkate almadan biraz gevşek bir şekilde kullanılır. Örneğin, N-H bağlarının oryantasyonu nedeniyle matematiksel anlamda oktahedral olmayan [Co(NH3)6]3+, oktahedral olarak adlandırılır.


















